Публикации в СМИ
Порфирии (болезни порфириновые) — наследственные или приобретённые (как результат воздействия химических агентов) дефекты ферментов, участвующих в биосинтезе гема. Порфирии классифицируют в зависимости от первичной локализации нарушения синтеза порфиринов:
• Эритропоэтическая порфирия обусловлена нарушением синтеза порфиринов эритробластами костного мозга и проявляется главным образом кожной фотосенсибилизацией (вследствие активации УФО повышенного отложения порфиринов в коже).
• Печёночная порфирия обусловлена нарушением синтеза порфиринов в печени и проявляется главным образом острыми неврологическими нарушениями (приступы артериальной гипертензии, колики в животе, психозы и невропатии) без кожной фотосенсибилизации. Во время приступа в плазме и моче повышается концентрация предшественников порфирина — -аминолевулиновой кислоты и порфобилиногена.
• Смешанные варианты.
Факторы риска • Приём ГК, пероральных контрацептивов и некоторых других ЛС (например, барбитуратов и сульфаниламидов) • Злоупотребление алкоголем • Голодание • Инфекции • Генетическая предрасположенность (см. ниже).
Биосинтез гема. Различают 7 ферментов, участвующих в биосинтезе гема (первый и последние 3 расположены в митохондриях, остальные — в цитозоле).
• d -Аминолевулинат синтетаза (КФ 2.3.1.37) катализирует конденсацию глицина (активируемого пиридоксаль фосфатом и сукцинил-КоA) с образованием d -аминолевулината.
• d -Аминолевулинат дегидратаза (КФ 4.2.1.24) катализирует конденсацию 2 молекул d -аминолевулината с образованием порфобилиногена. 4 молекулы порфобилиногена образуют уропорфироген III в двух последовательных реакциях, катализируемых тетрапиррольной гидроксиметилбилан синтетазой (также известной как порфобилиноген дезаминаза или уропорфироген I синтетаза) и уропорфироген III синтетазой. Гидроксиметилбилан синтетаза катализирует замыкание 4 молекул порфобилиногена по типу «голова в хвост» путём последовательного дезаминирования с образованием тетрапиррольного гидроксиметилбилана. Уропорфироген III синтетаза катализирует перестройку и быструю циклизацию гидроксиметилбилана с образованием уропорфирогена III.
• Пятый фермент, уропорфироген декарбоксилаза (КФ 4.1.1.37, уропорфироген III декарбоксилаза), катализирует последовательное удаление 4 карбоксильных групп с ацетилированной стороны цепей уропорфирогена III с образованием копропорфириногена III. Это соединение в дальнейшем поступает в митохондрии, где копропорфириноген оксидаза (шестой фермент) катализирует декарбоксилирование 2 из 4 пропионильных групп с образованием 2 винильных групп протопорфириногена IX.
• Далее протопорфириноген оксидаза (КФ 1.3.3.4) окисляет протопорфириноген IX до протопорфирина IX путём отщепления 6 атомов водорода. Продукт реакции — порфирин (окисленная форма), в отличие от тетрапиррольных предшественников (порфириногенов) — восстановленных форм.
• В итоге двухвалентный ион железа инкорпорируется в протопорфирин IX с образованием гема (реакцию катализирует восьмой фермент, феррохелатаза [КФ 4.99.1.1], также известный как гем синтетаза).
Генетические типы
• Эритропоэтические порфирии •• Порфирия врождённая эритропоэтическая (*263700, 10q25.2–q26.3, дефект гена UROS, r ) — увеличение образования порфирина эритроидными клетками в костном мозге вследствие недостаточности уропорфироген III косинтетазы. Клинические проявления: фотосенсибилизация, гипертрихоз, геморрагический синдром (за счёт тромбоцитопении), неонатальная желтуха, гепатоспленомегалия, покраснение зубов, задержка физического и психического развития. Лабораторные исследования: гемолитическая анемия, тромбоцитопения, гематурия, обнаружение в плазме, эритроцитах, моче и кале уропорфирина I и копропорфирина I; снижение активности уропорфироген III косинтетазы (с увеличением образования протопорфирина III). Лечение: гемотрансфузии, спленэктомия, b -каротин, антибактериальная терапия сопутствующих инфекционных осложнений. Синонимы: болезнь Гюнтера, врождённая порфирия (устар.), уропорфирия эритропоэтическая •• Эритропоэтическая протопорфирия (*177000, 18q21.3, дефекты генов FECH, FCE, Â или r ) вследствие частичной недостаточности феррохелатазы. Наиболее частая эритропоэтическая порфирия и вторая по частоте порфирия (после поздней кожной порфирии) Клинические проявления: фоточувствительный дерматит, холестаз с желтухой, гемолитическая анемия, полиневропатии (возможны парезы), начало заболевания — обычно до 10-летнего возраста. Лабораторные исследования: повышение содержания протопорфиринов в жёлчи, фекалиях (но не в моче), снижение активности феррохелатазы. Лечение: b -каротин, спленэктомия (при значительной спленомегалии), гемотрансфузии •• Наследственная сидеробластная анемия (см. Анемии сидеробластные).
• Печёночные порфирии •• Порфирия вследствие недостаточности d -аминолевулинат дегидратазы (*125270, 9q34, дефект гена ALAD, r ) с повышением уровня d -аминолевулиновой кислоты •• Порфирия острая перемежающаяся вследствие недостаточности гидроксиметилбилан синтетазы, порфобилиноген дезаминазы и уропорфироген синтетазы (*176000, 11q23.3, дефекты генов HMBS, PBGD, UPS, Â ). В моче также повышено содержание d -аминолевулиновой кислоты, что, вероятно, свидетельствует о сопутствующей недостаточности d -аминолевулинат дегидратазы. Преобладающий пол — женский. Лечение симптоматическое. При приступе: •• Глюкоза в/в 400 г/сут •• Гематин в/в медленно в дозе 1–4 мг/кг/сут в течение 3–14 сут. Синонимы: острая интермиттирующая порфирия, острая порфирия. Примечание. Ван Гог страдал от приступов острой перемежающейся порфирии, провоцируемых голоданием и злоупотреблением абсента •• Наследственная копропорфирия (*121300, 3q12, дефект гена CPO, Â ) вследствие недостаточности копропорфириноген оксидазы. Клинические проявления: боли в животе, запор, гепатоспленомегалия, желтуха, кожная фотосенсибилизация, неврологическая симптоматика, гемолитическая анемия. Лабораторные исследования: избыточное содержание копропорфирина III в моче и кале, повышена активность синтетазы 5-аминолевулиновой кислоты (КФ 2.3.1.37); во время приступа в моче возрастает содержание порфобилиногена и 5-аминолевулиновой кислоты.
• Порфирия кожная поздняя (*176100, 1p34, дефект гена UROD, Â ) — наиболее частая форма порфирии, обусловленная недостаточностью уропорфироген декарбоксилазы либо в печени (тип I, спорадический, гепатокожная порфирия, 176090, Â ), либо в других тканях (тип II, семейная, в т.ч. гепатоэритропоэтическая порфирия), проявляющаяся у взрослых фоточувствительным дерматитом в сочетании с повышенной экскрецией уропорфирина с мочой. У больных повышен риск развития рака печени. Лечение — повторные флеботомии. Синонимы: симптоматическая порфирия, гематопорфирия хроническая (устар.), порфиринопатия, эпидермолиз буллёзный порфирический.
• Порфирия смешанная (#176200, 1q21-q23, мутация гена протопорфириноген оксидазы PPOX [600923], Â ) характеризуется фотосенсибилизацией кожи, гиперпигментацией, гипертрихозом, болями в животе, запорами, тахикардией, артериальной гипертензией, разнообразной неврологической симптоматикой и увеличением экскреции прото- и копропорфирина с калом. Лечение — как при острой перемежающейся порфирии.
• Порфирия, тип Честер (*176010, 11q23.1, дефект гена PORC, Â ), — разновидность порфирии, клинически характеризующаяся острой неврологической симптоматикой без кожной фотосенсибилизации. Лабораторные исследования: недостаточность эритроцитарной порфобилиноген дезаминазы (как при острой перемежающейся порфирии) и протопорфириноген оксидазы (как при смешанной порфирии). Примечание. Честер, семейство в Англии, в котором впервые выявлен данный тип порфирии.
МКБ-10 • E80 Нарушения обмена порфирина и билирубина
Код вставки на сайт
Порфирия
Порфирии (болезни порфириновые) — наследственные или приобретённые (как результат воздействия химических агентов) дефекты ферментов, участвующих в биосинтезе гема. Порфирии классифицируют в зависимости от первичной локализации нарушения синтеза порфиринов:
• Эритропоэтическая порфирия обусловлена нарушением синтеза порфиринов эритробластами костного мозга и проявляется главным образом кожной фотосенсибилизацией (вследствие активации УФО повышенного отложения порфиринов в коже).
• Печёночная порфирия обусловлена нарушением синтеза порфиринов в печени и проявляется главным образом острыми неврологическими нарушениями (приступы артериальной гипертензии, колики в животе, психозы и невропатии) без кожной фотосенсибилизации. Во время приступа в плазме и моче повышается концентрация предшественников порфирина — -аминолевулиновой кислоты и порфобилиногена.
• Смешанные варианты.
Факторы риска • Приём ГК, пероральных контрацептивов и некоторых других ЛС (например, барбитуратов и сульфаниламидов) • Злоупотребление алкоголем • Голодание • Инфекции • Генетическая предрасположенность (см. ниже).
Биосинтез гема. Различают 7 ферментов, участвующих в биосинтезе гема (первый и последние 3 расположены в митохондриях, остальные — в цитозоле).
• d -Аминолевулинат синтетаза (КФ 2.3.1.37) катализирует конденсацию глицина (активируемого пиридоксаль фосфатом и сукцинил-КоA) с образованием d -аминолевулината.
• d -Аминолевулинат дегидратаза (КФ 4.2.1.24) катализирует конденсацию 2 молекул d -аминолевулината с образованием порфобилиногена. 4 молекулы порфобилиногена образуют уропорфироген III в двух последовательных реакциях, катализируемых тетрапиррольной гидроксиметилбилан синтетазой (также известной как порфобилиноген дезаминаза или уропорфироген I синтетаза) и уропорфироген III синтетазой. Гидроксиметилбилан синтетаза катализирует замыкание 4 молекул порфобилиногена по типу «голова в хвост» путём последовательного дезаминирования с образованием тетрапиррольного гидроксиметилбилана. Уропорфироген III синтетаза катализирует перестройку и быструю циклизацию гидроксиметилбилана с образованием уропорфирогена III.
• Пятый фермент, уропорфироген декарбоксилаза (КФ 4.1.1.37, уропорфироген III декарбоксилаза), катализирует последовательное удаление 4 карбоксильных групп с ацетилированной стороны цепей уропорфирогена III с образованием копропорфириногена III. Это соединение в дальнейшем поступает в митохондрии, где копропорфириноген оксидаза (шестой фермент) катализирует декарбоксилирование 2 из 4 пропионильных групп с образованием 2 винильных групп протопорфириногена IX.
• Далее протопорфириноген оксидаза (КФ 1.3.3.4) окисляет протопорфириноген IX до протопорфирина IX путём отщепления 6 атомов водорода. Продукт реакции — порфирин (окисленная форма), в отличие от тетрапиррольных предшественников (порфириногенов) — восстановленных форм.
• В итоге двухвалентный ион железа инкорпорируется в протопорфирин IX с образованием гема (реакцию катализирует восьмой фермент, феррохелатаза [КФ 4.99.1.1], также известный как гем синтетаза).
Генетические типы
• Эритропоэтические порфирии •• Порфирия врождённая эритропоэтическая (*263700, 10q25.2–q26.3, дефект гена UROS, r ) — увеличение образования порфирина эритроидными клетками в костном мозге вследствие недостаточности уропорфироген III косинтетазы. Клинические проявления: фотосенсибилизация, гипертрихоз, геморрагический синдром (за счёт тромбоцитопении), неонатальная желтуха, гепатоспленомегалия, покраснение зубов, задержка физического и психического развития. Лабораторные исследования: гемолитическая анемия, тромбоцитопения, гематурия, обнаружение в плазме, эритроцитах, моче и кале уропорфирина I и копропорфирина I; снижение активности уропорфироген III косинтетазы (с увеличением образования протопорфирина III). Лечение: гемотрансфузии, спленэктомия, b -каротин, антибактериальная терапия сопутствующих инфекционных осложнений. Синонимы: болезнь Гюнтера, врождённая порфирия (устар.), уропорфирия эритропоэтическая •• Эритропоэтическая протопорфирия (*177000, 18q21.3, дефекты генов FECH, FCE, Â или r ) вследствие частичной недостаточности феррохелатазы. Наиболее частая эритропоэтическая порфирия и вторая по частоте порфирия (после поздней кожной порфирии) Клинические проявления: фоточувствительный дерматит, холестаз с желтухой, гемолитическая анемия, полиневропатии (возможны парезы), начало заболевания — обычно до 10-летнего возраста. Лабораторные исследования: повышение содержания протопорфиринов в жёлчи, фекалиях (но не в моче), снижение активности феррохелатазы. Лечение: b -каротин, спленэктомия (при значительной спленомегалии), гемотрансфузии •• Наследственная сидеробластная анемия (см. Анемии сидеробластные).
• Печёночные порфирии •• Порфирия вследствие недостаточности d -аминолевулинат дегидратазы (*125270, 9q34, дефект гена ALAD, r ) с повышением уровня d -аминолевулиновой кислоты •• Порфирия острая перемежающаяся вследствие недостаточности гидроксиметилбилан синтетазы, порфобилиноген дезаминазы и уропорфироген синтетазы (*176000, 11q23.3, дефекты генов HMBS, PBGD, UPS, Â ). В моче также повышено содержание d -аминолевулиновой кислоты, что, вероятно, свидетельствует о сопутствующей недостаточности d -аминолевулинат дегидратазы. Преобладающий пол — женский. Лечение симптоматическое. При приступе: •• Глюкоза в/в 400 г/сут •• Гематин в/в медленно в дозе 1–4 мг/кг/сут в течение 3–14 сут. Синонимы: острая интермиттирующая порфирия, острая порфирия. Примечание. Ван Гог страдал от приступов острой перемежающейся порфирии, провоцируемых голоданием и злоупотреблением абсента •• Наследственная копропорфирия (*121300, 3q12, дефект гена CPO, Â ) вследствие недостаточности копропорфириноген оксидазы. Клинические проявления: боли в животе, запор, гепатоспленомегалия, желтуха, кожная фотосенсибилизация, неврологическая симптоматика, гемолитическая анемия. Лабораторные исследования: избыточное содержание копропорфирина III в моче и кале, повышена активность синтетазы 5-аминолевулиновой кислоты (КФ 2.3.1.37); во время приступа в моче возрастает содержание порфобилиногена и 5-аминолевулиновой кислоты.
• Порфирия кожная поздняя (*176100, 1p34, дефект гена UROD, Â ) — наиболее частая форма порфирии, обусловленная недостаточностью уропорфироген декарбоксилазы либо в печени (тип I, спорадический, гепатокожная порфирия, 176090, Â ), либо в других тканях (тип II, семейная, в т.ч. гепатоэритропоэтическая порфирия), проявляющаяся у взрослых фоточувствительным дерматитом в сочетании с повышенной экскрецией уропорфирина с мочой. У больных повышен риск развития рака печени. Лечение — повторные флеботомии. Синонимы: симптоматическая порфирия, гематопорфирия хроническая (устар.), порфиринопатия, эпидермолиз буллёзный порфирический.
• Порфирия смешанная (#176200, 1q21-q23, мутация гена протопорфириноген оксидазы PPOX [600923], Â ) характеризуется фотосенсибилизацией кожи, гиперпигментацией, гипертрихозом, болями в животе, запорами, тахикардией, артериальной гипертензией, разнообразной неврологической симптоматикой и увеличением экскреции прото- и копропорфирина с калом. Лечение — как при острой перемежающейся порфирии.
• Порфирия, тип Честер (*176010, 11q23.1, дефект гена PORC, Â ), — разновидность порфирии, клинически характеризующаяся острой неврологической симптоматикой без кожной фотосенсибилизации. Лабораторные исследования: недостаточность эритроцитарной порфобилиноген дезаминазы (как при острой перемежающейся порфирии) и протопорфириноген оксидазы (как при смешанной порфирии). Примечание. Честер, семейство в Англии, в котором впервые выявлен данный тип порфирии.
Что такое порфирия: симптомы, диагностика и лечение. Острая перемежающаяся порфирия: симптомы, диагностика, лечение
Острая перемежающаяся порфирия (пирролопорфирия, шведская порфирия) впервые была описана Waldenstrom в 1937 г. В основе заболевания, наследующегося по аутосомно-доминантному типу, лежат мутации гена, который кодирует порфобилиногендеаминазу.
Частота острой перемежающейся порфирии в большинстве регионов составляет 1 случай на 10 000 населения.
Молекулярные основы и патогенез острой перемежающейся порфирии
Ген, кодирующий порфобилиногендеаминазу, расположен на 11-й хромосоме. В настоящее время идентифицировано более 100 различных мутаций этого гена. Снижение активности порфобилиногендеаминазы, степень которой сильно варьирует, выявляется в печени, эритроцитах и других тканях. Обычно активность порфобилиногендеаминазы у гетерозигот составляет 50% от нормы, у гомозигот — не более 17%.
В связи с нарушениями функции порфобилиногендеаминазы вторично индуцируется АЛК-синтетаза. Это приводит к накоплению АЛК, обладающей нейротоксическим действием. Развитие неврологических изменений обусловлено также: а) снижением синтеза гема в нервных клетках; б) накоплением нейротоксических доз триптофана и серотонина, метаболизм которых нарушается в клетке, обедненной гемом.
У большинства гетерозигот клинические признаки заболевания отсутствуют, однако провоцирующие факторы могут способствовать возникновению биохимических и клинических расстройств. Наиболее часто пусковыми факторами являются стероидные гормоны (экзогенные и эндогенные), а также различные медикаменты. Половые гормоны индуцируют печеночную АЛК-синтетазу и способствуют манифестации болезни.
Значение половых гормонов подтверждают случаи дебюта заболевания в пубертатном периоде или сразу же после его окончания.
Медикаменты, способствующие индукции острой порфирии:
а) Опасные в плане развития острой порфирии: барбитураты, гризеофульвин, даназол, дапсон, диклофенак, дифенилгидантон, изопропилмепробамат, карбамазепин, карбромал, мепробамат, мефенитон, новобиоцин, пиразолоновые препараты, прогестины, сульфаниламиды, толбутамид, хлорохин (делагил), хлорпропамид, этанол
б) Потенциально опасные в плане развития острой порфирии: алкилирующие агенты, бемегрид, гидралазин, кетамин, клоназепам, клонидин, колистин, метилдофа, метоклопрамид, нитразепам, нифедипин, нортриптилин, пентазоцин, пиразинамид, рифампицин, спиронолактон, теофиллин, феноксибензамин, хлорамфеникол, эритромицин
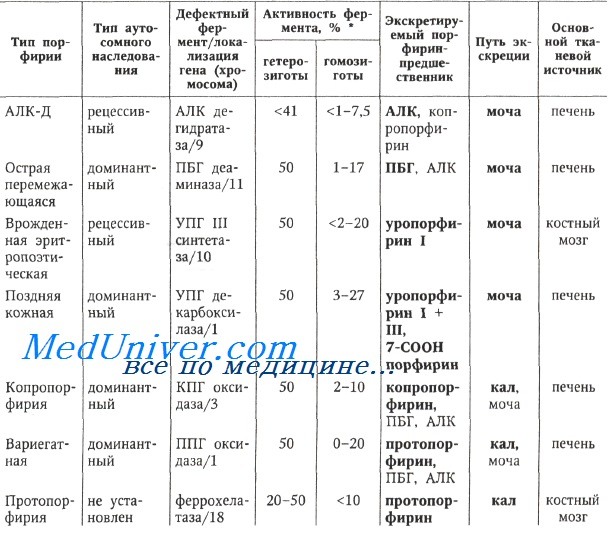
Генетические и метаболические нарушения при порфириях Примечание. 1) * — процент от значения нормальной активности фермента; 2) основной метаболит и путь экскреции выделены жирным шрифтом; 3) сокращения: АЛК — 5-аминолевулиновая кислота, ПБГ — порфобилиноген, УПГ — уропорфириноген, КПГ — копропорфириноген, ППГ — протопорфириноген.
Клиническая картина острой перемежающейся порфирии
Клиническая картина острой перемежающейся порфирии выражается в острых атаках, связанных с нарушением внутренних органов и поражением нервной системы. Выраженность симптомов вариабельна и может различаться даже у близнецов.
Остро возникающая нейропатия часто манифестирует резкими болями в животе, различными по характеру и локализации; в последующем развиваются запоры. Живот мягкий при пальпации, симптомов раздражения брюшины нет. Характерны тахикардия и изменения артериального давления (гипертензия или гипотензия).
Реже (при затянувшихся атаках) возникает периферическая моторная нейропатия, характеризующаяся слабостью в конечностях, чаще верхних. При прогрессировании возможно развитие вялого тетрапареза, бульварных расстройств, нарушений дыхательной мускулатуры, клонико-тонических судорог. Часто возникают психические расстройства, спектр которых варьирует от эмоциональной лабильности до острого психоза.
У половины больных наблюдается стойкая артериальная гипертензия и хроническая почечная недостаточность.

Данные лабораторных исследований острой перемежающейся порфирии
В анализе крови изменений обычно не выявляется, однако в ряде случаев в период атаки может наблюдаться лейкоцитоз — признак, требующий внимания ввиду возможности развития осложнений («острый живот»).
При биохимическом исследовании в моче определяется увеличение концентрации порфобилиногена, в меньшей степени — АЛК. В норме суточная экскреция порфобилиногена и АЛК не превышает 4 мг. В период атаки экскреция порфобилиногена увеличивается до 20-200 мг. При ремиссии заболевания экскреция порфобилиногена и АЛК существенно уменьшается, но редко нормализуется.
Важный диагностический критерий острой перемежающейся порфирии — повышение активности порфобилиногендеаминазы в эритроцитах.
Этот метод особенно важен, когда концентрация порфобилиногена и АЛК в моче в период ремиссии в пределах нормы. У 10% больных концентрация перечисленных ферментов в эритроцитах не снижается, что обусловлено гетерогенностью мутаций гена порфобилиногендеаминазы.
Характерных изменений при инструментальных исследованиях ЦНС (электроэнцефалография, компьютерная и магнитно-резонансная томография) не выявляется.
Профилактика и лечение острой перемежающейся порфирии
При установленном диагнозе главное значение имеет профилактика атак заболевания. Необходимо исключить прием потенциально опасных медикаментов, список которых должен быть у пациента. Женщинам, у которых атаки связаны с менструальным циклом, для подавления овуляции назначаются оральные контрацептивы.
При атаке пациенты должны госпитализироваться в стационар. По возможности необходимо исключить провоцирующие факторы. Для купирования болевого синдрома используются ненаркотические и наркотические анальгетики. Проводится инфузионная терапия, коррекция электролитных расстройств. При тяжелом течении показаны внутривенные инфузии гематина (растворимая форма хлорида гема).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
– Вернуться в раздел “гематология”
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Острая перемежающаяся порфирия
Острая перемежающаяся порфирия (ОПП) – тяжелое наследственное заболевание, характеризующееся нарушением синтеза порфиринов и накоплением их предшественников, оказывающих токсическое действие на различные органы и системы. Клинически проявляется сильной болью в животе, тошнотой, рвотой, тахикардией, гипертензией, полинейропатиями и психическими нарушениями. Диагноз ставится на основании определения повышенного содержания порфиринов и их предшественников в моче, снижения активности фермента порфобилиногендезаминазы в крови и ДНК-диагностики. Лечение заключается в подавлении образования порфиринов и симптоматической терапии.
МКБ-10

Общие сведения
Острая перемежающаяся порфирия (пироллопорфирия) – редкое генетическое заболевание с аутосомно-доминантным типом наследования, обусловленное дефицитом фермента, участвующего в синтезе порфиринов. Порфирия – термин греческого происхождения, «porphyreis» означает «багряный, пурпурный», именно такой цвет приобретает моча при ОПП. «Перемежающаяся» подразумевает приступообразное течение. ОПП относится к группе острых печеночных порфирий и является самой тяжелой из них. Впервые болезнь была описана в 1889 году. В России первое сообщение о больном перемежающейся порфирией сделали врачи А.Беюл и И.Гельман в 1928 году. Средняя распространенность по всему миру составляет от 5 до 10 на 100000 человек. Наиболее часто данная патология встречается среди лиц скандинавского и англосаксонского происхождения – в Швеции 1:1000, в Англии 1:30000. Женщины страдают в 4-5 раз чаще мужчин.

Причины ОПП
В основе заболевания лежит генетически обусловленная неполноценность фермента порфобилиногендезаминазы (гидроксиметилбилансинтазы), участвующей в образовании порфиринов. Мутация расположена в гене PBGD на хромосоме 11 (локус 11q24.1-24.2). Порфирины – это большая группа органических соединений, которые являются составной частью белков, связывающих и переносящих кислород (гемоглобин, миоглобин), а также каталаз, расщепляющих перекись водорода, и цитохромов, обеспечивающих нейтрализацию ксенобиотиков (лекарства, алкоголь, яды). Синтез порфиринов осуществляется в костном мозге, печени, нейронах, эритроцитах. Дефицит порфобилиногендезаминазы при данном заболевании наблюдается главным образом в печени, а также в клетках нервной системы и эритроцитах. В результате недостаточной активности фермента происходит торможение образования порфиринов на уровне их предшественников – дельта-аминолевуленовой кислоты (ДАЛК) и порфобилиногена (ПБГ), которые являются токсичными для многих органов и систем.
Однако наличие неполноценного фермента не всегда приводит к развитию порфирии. Важную роль играют провоцирующие факторы, которые ускоряют выработку предшественников порфиринов. Такие факторы называются провоцирующими печеночными порфириногенами. Ими являются алкоголь, вирусные и бактериальные инфекции, стресс, хирургические операции, гипогликемия, голодание, колебания гормонального фона у женщин (менструация, беременность), воздействие тяжелых металлов (свинец, ртуть, висмут). Особое место отводится лекарственным препаратам, которые чаще всего вызывают манифестацию и обострение заболевания. Наиболее выраженным порфириногенным действием обладают препараты, активно метаболизирующиеся системой цитохрома P-450 – барбитураты, эстрогены, анальгин, парацетамол, гризеофульвин, сульфаниламиды, фенитоин, хлорамфеникол, карбамазепин, метилдопа.
Патогенез
В результате неполноценности фермента под действием провоцирующих факторов накапливаются промежуточные продукты метаболизма порфиринов, оказывающие свои повреждающие действия. Они блокируют натрий-калиевую АТФ-азу, тем самым изменяют метаболизм АТФ и медиаторов в нервных клетках. В результате этого развиваются демиелинизация и аксональная дегенерация нервных волокон. Эти патологические изменения больше выражены в периферической нервной системе, чем в центральной. Дистрофия в вегетативных ганглиях приводит к нарушению сосудистого тонуса и регуляции деятельности внутренних органов. Поражение абдоминальных сплетений вызывает спазм сосудов брыжейки и нарушение моторики желудка и кишечника. Вследствие ослабления активности блуждающего нерва усиливается влияние симпатической нервной системы на сердце и сосуды. Повреждение нервной системы также обусловлено возникающим дефицитом порфиринов в нейронах.
Предшественники порфиринов стимулируют выработку в гипоталамусе антидиуретического гормона. Возникает уменьшение диуреза, задержка жидкости, снижение осмолярности плазмы крови. Данное явление носит название синдром неадекватной секреции антидиуретического гормона (синдром Пархона – гидропексический синдром). Точный механизм развития этого синдрома при порфирии до сих пор неизвестен.
Классификация
В зависимости от наличия или отсутствия клинических проявлений, степени их выраженности, а также обнаружения специфических биохимических изменений в лабораторных исследованиях (повышение уровня общих порфиринов, ПБГ и ДАЛК в моче, снижение активности порфобилиногендезаминазы в эритроцитах) различают следующие формы острой перемежающейся порфирии:
- Скрытое носительство мутантного гена. Симптоматика и биохимические изменения отсутствуют. Выявляется лишь снижение уровня эритроцитарной порфобилиногендезаминазы.
- Здоровое носительство дефектного гена. Наблюдаются минимальные биохимические изменения при отсутствии клинических проявлений.
- Латентная форма. Выявляется стертая симптоматика без типичных острых приступов болезни и выраженные нарушения порфиринового обмена.
- Манифестная форма. Отмечается яркая клиническая картина, протекающая в виде приступов. Приступы могут иметь постоянную выраженность или, наоборот, с каждым разом усиливаться. Может развиться острейшая форма (часто возникает при беременности) с грубыми неврологическими нарушениями и летальным исходом. Отмечаются выраженные биохимические отклонения порфиринового обмена.
Симптомы ОПП
Клинические проявления разнообразны. Чаще всего они возникают в молодом возрасте (около 20 лет). При латентной форме порфирии наблюдается следующая симптоматика – нарушение сна, склонность к артериальной гипертензии, учащенное сердцебиение, незначительные боли или неприятные ощущения в животе, снижение сухожильных рефлексов, мышечная слабость, психологические изменения личности.
При манифестной форме клиника развивается в виде острых атак. Продолжительность атаки составляет от 2 до 10 недель с рецидивами через 1-2 года. В начале приступа наиболее типичны проявления со стороны желудочно-кишечного тракта: интенсивные острые боли в животе, тошнота, рвота, вздутие, задержка стула. Боли имеют коликообразный характер, локализуются в разных отделах живота и бывают настолько сильными, что пациенты часто попадают в хирургический стационар с подозрением на острый аппендицит или перфорацию язвы желудка. Также повышается температура, увеличивается артериальное давление, вплоть до гипертонического криза, учащается сердцебиение. Характерным является розовая или красно-бурая окраска мочи.
Клиника поражения нервной системы присоединяется на 7-10 день приступа. Возникают разлитые боли по всему телу, снижается чувствительность на разных участках тела, выпадают сухожильные и кожные рефлексы. Появляются слабость и ограничение движения в конечностях (парез), более выраженные в проксимальных отделах – в плечах и бедрах. Иногда развивается полный паралич конечностей. В тяжелых случаях в патологический процесс вовлекаются черепно-мозговые нервы, что сопровождается двоением в глазах (диплопией), асимметрией лица, невнятной речью (дизартрией), нарушением глотания и поперхиванием (дисфагией).
Возможны судорожные припадки и психические нарушения – бессонница, эмоциональная лабильность, депрессивное состояние, неадекватное поведение, истерические припадки, зрительные и слуховые галлюцинации. Вследствие повышенной выработки антидиуретического гормона уменьшается мочеотделение, что приводит к водной интоксикации (гипоосмолярная гипергидратация), характеризующейся снижением аппетита, вялостью, адинамией, тремором, мышечными судорогами.
Осложнения
Наиболее тяжелые осложнения перемежающейся порфирии обусловлены полинейропатией. При параличе диафрагмы и межреберных мышц возникает острая дыхательная недостаточность, требующая проведения искусственной вентиляции легких. При слабости мышц глотки часть пищи может попасть в дыхательные пути и вызвать аспирационную пневмонию. В парализованных конечностях замедляется ток крови, что создает благоприятные условия для тромбообразования. Более редкие осложнения порфирии связаны с повышенным образованием антидиуретического гормона. Это отек головного мозга и рабдомиолиз (разрушение скелетных мышц). При рабдомиолизе из поврежденных мышечных клеток высвобождается миоглобин и калий, которые могут привести к острой почечной недостаточности и жизнеугрожающим нарушениям ритма сердца.
Диагностика
Пациентов с ОПП курирует врач-гематолог. Постановка диагноза перемежающейся порфирии представляет сложную задачу. Необходимо учитывать возраст пациента, время возникновения симптомов (например, лютеиновая фаза менструального цикла у женщин), наличие связи начала заболевания с провоцирующими факторами. Очень важно уточнять, какие лекарственные препараты принимал больной до развития приступа. Основная роль в распознавании перемежающейся порфирии отводится лабораторным методам:
- Исследование мочи. В общем анализе мочи выявляется повышенная относительная плотность, розовый или красно-бурый цвет мочи. Часто такую окраску моча приобретает только при длительном нахождении на свету. Существует специальный скрининговый тест с реактивом Эрлиха: при добавлении реактива к моче она в течение 5 минут становится красной. Этот анализ считается тестом первой линии, его обязательно следует проводить всем пациентам, как только у них заподозрена порфирия. При положительном результате выполняется количественное определение содержания в моче порфиринов, ДАЛК и ПБГ – при перемежающейся порфирии они повышены.
- Исследование крови. В биохимическом анализе часто обнаруживаются гипогликемия, снижение уровня натрия и осмолярности плазмы. В эритроцитах отмечается сниженная активность порфобилиногендезаминазы. При молекулярно-генетической диагностике выявляется мутация гена PBGD. Определение активности фермента и ДНК-диагностика в основном применяются при латентных и скрытых формах острой перемежающейся порфирии или при сомнительных результатах предыдущих анализов.
Дифференциальный диагноз следует проводить с другими видами острых порфирий, демиелинизирующими заболеваниями (рассеянный склероз, синдром Гийена-Барре), отравлением свинцом, острыми абдоминальными хирургическими патологиями (аппендицит, кишечная непроходимость, холецистит, панкреатит, перфорация язвы желудка или двенадцатиперстной кишки), эпилепсией, психиатрическими болезнями. В дифференциальной диагностике принимают участие невролог, хирург, психиатр.
Лечение ОПП
Пациенты с манифестной и даже латентной формой подлежат лечению в гематологическом стационаре. При развитии выраженной неврологической симптоматики обязательна госпитализация в отделение реанимации и интенсивной терапии. Важно устранить все факторы, провоцирующие обострение заболевания. В первую очередь это касается приема лекарственных средств.
Этиотропной терапии не существует. Основная роль отводится патогенетическому лечению. Для этого применяются препараты, блокирующие образование токсичных предшественников порфиринов и, тем самым, уменьшающие их патологическое действие. К ним относятся большие дозы глюкозы, гема аргинат, сандостатин, аденил-5-монофосфат. Для ускорения регенерации миелиновой оболочки в нервных волокнах назначаются витамины группы В, для профилактики тромбообразования – антикоагулянты. Также используются антигипертензивные, анальгетические, противорвотные, слабительные, седативные препараты.
Если атаки порфирии являются менструалозависимыми и возникают часто (2-3 раза в год), необходимо подавление овуляции. С этой целью применяют агонисты гонадотропин-рилизинг гормона (Гозерелин). Беременность является неблагоприятным фактором и ассоциирована с молниеносным течением перемежающейся порфирии, высокой частотой летальных исходов. При развитии приступа в I и II триместре рекомендуется прерывание беременности, в III триместре проводится экстренное оперативное родоразрешение.
Прогноз и профилактика
Острая перемежающаяся порфирия – это тяжелое заболевание с неблагоприятным прогнозом и достаточно высоким уровнем летальности (15-20%). Самая частая причина смерти – паралич дыхательной мускулатуры вследствие полинейропатии. Очень важно своевременно диагностировать болезнь и начать специфическую терапию. Профилактика заключается в соблюдении высокоуглеводной диеты и избегании всех провоцирующих факторов, которые могут вызвать обострение – стрессов, инфекций, голодания, приема лекарственных средств и алкоголя. При наличии детей у пациентки с порфирией от новой беременности лучше отказаться. Всем родственникам больного порфирией для выявления скрытых или латентных форм заболевания необходимо проводить молекулярно-генетическую диагностику, определять уровень эритроцитарной порфобилиногендезаминазы и количество порфиринов в моче.
1. Диагностика и лечение острых порфирий. Клинические рекомендации национального гематологического сообщества/ под ред. Я.С. Пустовойт, С.К. Кравченко, Р.Г. Шмакова, В.Г. Савченко. – 2018.
2. Лабораторная диагностика острой перемежающейся порфирии/ Карпова И.В., Сурин В.Л., Тагиев А.Ф., Пивник А.В.// Проблемы гематологии и переливания крови. – 1998 – №1.
3. Острая порфирия с полиневропатией и положительным эффектом лечения глюкозой/ Котов С.В., Сидорова О.П.// Медицинская генетика. – 2016 – №7.
4. Заболевания внутренних органов при манифестных и латентных нарушениях порфиринового обмена: Моногр./Б.Н.Кривошеев и др.
Острая перемежающаяся порфирия
Острая перемежающаяся порфирия – генетически детерминированное заболевание, обусловленное поражением центральной нервной системы, реже – периферической нервной системы, периодическими болями в области живота, повышением артериального давления и выделением мочи розового цвета в связи с большим количеством в ней предшественника порфиринов.
Что провоцирует / Причины Острой перемежающейся порфирии:
Заболевание является генетически детерминированным, передается по аутосомно-доминантному типу.
Чаще болезнь поражает молодых женщин, девушек и провоцируется беременностью, родами. Также возможно развитие заболевания вследствие приема ряда лекарств, таких как барбитураты, сульфаниламидные препараты, анальгин. Наиболее часто обострения отмечаются после операций, особенно если для премедикации использовался тиопентал натрия.
Патогенез (что происходит?) во время Острой перемежающейся порфирии:
В основе болезни лежат нарушение активности фермента уропорфириноген I-синтазы, а также повышение активности синтазы 6-аминолевулиновой кислоты.
Клинические проявления болезни характеризуются накоплением в нервной клетке токсического вещества 8-аминолевулиновой кислоты. Данное соединение концентрируется в гипоталамусе и тормозит активность мозговой натрий-калий-зависимой аденозинфосфатазы, что приводит к нарушению транспорта ионов через мембраны и нарушает функцию нерва.
В дальнейшем развиваются демиелинизация нервов, аксональная нейропатия, что и обусловливает все клинические проявления болезни.
Симптомы Острой перемежающейся порфирии:
Наиболее характерным признаком острой перемежающейся порфирии являются боли в животе. Иногда сильным болям предшествует задержка менструаций. Нередко больных оперируют, но не находят причины боли.
При острой порфирии поражается нервная система по типу тяжелого полиневрита. Он начинается с болей в конечностях, затруднений в движениях, связанных как с болью, так и с симметричными двигательными нарушениями, прежде всего в мышцах конечностей. Если в патологический процесс вовлекаются мышцы запястья, лодыжки, кисти, то могут развиться почти необратимые деформации. При прогрессировании процесса возникает парез в четырех конечностях, в дальнейшем возможны паралич дыхательной мускулатуры и смерть.
Также в процесс вовлекается ЦНС, в результате поражения которой появляются судороги, эпилептиформные припадки, бред, галлюцинации.
У большинства больных повышается артериальное давление, возможна выраженная артериальная гипертония с повышением как систолического, так и диастолического давления.
Врач должен отменить прием некоторых, на первый взгляд, безобидных лекарств, таких как валокордин, белласпон, беллоид, теофедрин, содержащих фенобарбитал, что может обострять болезнь. Обострение данной формы порфирии также наступает под влиянием женских половых гормонов, противогрибковых препаратов (гризеофульвина).
Тяжелые неврологические расстройства часто являются причиной летального исхода, однако в некоторых случаях неврологическая симптоматика идет на убыль, в дальнейшем наступает ремиссия. В связи с такой характерной клинической картиной заболевания его назвали острой перемежающейся порфирией.
Следует отметить, что далеко не у всех носителей патологического гена болезнь проявляется клинически. Нередко у родственников больных, особенно у мужчин, есть биохимические признаки болезни, однако нет и не было никаких клинических симптомов. Это латентная форма острой перемежающейся порфирии. У таких людей при воздействии неблагоприятных факторов может наступить тяжелое обострение.
Диагностика Острой перемежающейся порфирии:
Диагностика острой перемежающейся порфирии основывается на обнаружении в моче у больных предшественников синтеза порфиринов (так называемого порфобилиногена), а также 6-аминолевулиновой кислоты.
Дифференциальная диагностика острой перемежающейся порфирии проводится с другими, более редкими, формами порфирии (наследственной копропорфирией, вариегатной порфирией), а также со свинцовым отравлением.
При свинцовом отравлении характерны боли в животе, полиневрит. Однако свинцовое отравление в отличие от острой порфирии сопровождается гипохромной анемией с базофильной пунктацией эритроцитов и высоким содержанием железа сыворотки. Для острой порфирии анемия не характерна. У женщин, страдающих острой порфирией и меноррагиями, возможна хроническая постгеморрагическая железодефицитная анемия, сопровождающаяся низким содержанием железа сыворотки крови.
Лечение Острой перемежающейся порфирии:
Прежде всего следует исключить из употребления все препараты, приводящие к обострению болезни. Не следует назначать больным анальгин, транквилизаторы. При сильных болях показаны наркотические средства, аминазин. При резкой тахикардии, значительном повышении артериального давления целесообразно применять индерал или обзидан, при выраженных запорах – прозерин.
Ряд лекарственных средств (в первую очередь глюкоза), используемых при острой перемежающейся порфирии, направлен на уменьшение выработки порфиринов. Рекомендуется диета с высоким содержанием углеводов, внутривенно вводят концентрированные растворы глюкозы (до 200 г/сут.).
Значительный эффект в тяжелых случаях дает введение гематина, однако препарат иногда вызывает опасные реакции.
В тяжелых случаях острой порфирии, при нарушении дыхания больные нуждаются в длительной управляемой вентиляции легких.
В случае положительной динамики, а также при заметном улучшении состояния больных в качестве восстановительной терапии применяют массаж, лечебную гимнастику.
В ремиссии необходима профилактика обострений, прежде всего исключение средств, вызывающих обострения.
Прогноз в случае поражения нервной системы достаточно серьезный, особенно при использовании искусственной вентиляции легких.
Если заболевание протекает без тяжелых нарушений, прогноз достаточно хороший. Нередко удается добиться ремиссии у больных с тяжелыми тетрапарезами, психическими нарушениями. Необходимо обследовать родственников больных для выявления биохимических признаков порфирии. Всем больным с латентной формой порфирии следует избегать лекарств и химикатов, вызывающих обострение порфирии.
К каким докторам следует обращаться если у Вас Острая перемежающаяся порфирия:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Острой перемежающейся порфирии, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору – клиника Eurolab всегда к Вашим услугам! Лучшие врачи осмотрят Вас, изучат внешние признаки и помогут определить болезнь по симптомам, проконсультируют Вас и окажут необходимую помощь и поставят диагноз. Вы также можете вызвать врача на дом. Клиника Eurolab открыта для Вас круглосуточно.
Как обратиться в клинику:
Телефон нашей клиники в Киеве: (+38 044) 206-20-00 (многоканальный). Секретарь клиники подберет Вам удобный день и час визита к врачу. Наши координаты и схема проезда указаны здесь. Посмотрите детальнее о всех услугах клиники на ее персональной странице.
Если Вами ранее были выполнены какие-либо исследования, обязательно возьмите их результаты на консультацию к врачу. Если исследования выполнены не были, мы сделаем все необходимое в нашей клинике или у наших коллег в других клиниках.
У Вас ? Необходимо очень тщательно подходить к состоянию Вашего здоровья в целом. Люди уделяют недостаточно внимания симптомам заболеваний и не осознают, что эти болезни могут быть жизненно опасными. Есть много болезней, которые по началу никак не проявляют себя в нашем организме, но в итоге оказывается, что, к сожалению, их уже лечить слишком поздно. Каждое заболевание имеет свои определенные признаки, характерные внешние проявления – так называемые симптомы болезни. Определение симптомов – первый шаг в диагностике заболеваний в целом. Для этого просто необходимо по несколько раз в год проходить обследование у врача, чтобы не только предотвратить страшную болезнь, но и поддерживать здоровый дух в теле и организме в целом.
Если Вы хотите задать вопрос врачу – воспользуйтесь разделом онлайн консультации, возможно Вы найдете там ответы на свои вопросы и прочитаете советы по уходу за собой. Если Вас интересуют отзывы о клиниках и врачах – попробуйте найти нужную Вам информацию в разделе Вся медицина. Также зарегистрируйтесь на медицинском портале Eurolab, чтобы быть постоянно в курсе последних новостей и обновлений информации на сайте, которые будут автоматически высылаться Вам на почту.
Другие заболевания из группы Болезни крови, кроветворных органов и отдельные нарушения, вовлекающие иммунный механизм:
Если Вас интересуют еще какие-нибудь виды болезней и группы заболеваний человека или у Вас есть какие-либо другие вопросы и предложения – напишите нам, мы обязательно постараемся Вам помочь.
Диагностика и лечение острых порфирий
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ДИАГНОСТИКА И ЛЕЧЕНИЕ ОСТРЫХ ПОРФИРИЙ
Москва 2018 г.
Порфирии представляют собой группу заболеваний, состоящую из семи нозологических форм. Причинами их возникновения являются генетически обусловленные нарушения активности различных ферментов в цепи биосинтеза гема (Рисунок 1, Приложения). Это приводит к нарушению обмена порфиринов, имеющему свои особенности при каждой форме порфирии и определяющему их клинические проявления. Начало изучения нарушений порфиринового обмена относится к 1841г., когда Scherer доказал, что красный цвет мочи больных обусловлен наличием в ней определѐнных пигментов, а не присутствием молекул гемоглобина. Fisher в 1930г. получил Нобелевскую премию за работу по изучению промежуточных продуктов гема и в 1934 году опубликовал книгу «Химия пирролов» [6]. Схема биосинтеза гема была описана в 50-е годы прошлого столетия.
В дальнейшем были идентифицированы все восемь ферментов в этом цикле [5]. Установлено, что каждая нозологическая форма порфирий связана с дефектом активности одного из ферментов (кроме синтетазы дельта-аминолевулиновой кислоты (-АЛК)), закодированного в одном гене.

Автоматизация клиники: быстро и недорого!
– Подключено 300 клиник из 4 стран
– 800 RUB / 4500 KZT / 27 BYN – 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место – 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Порфирии подразделяются на эритропоэтические и печѐночные в зависимости от ткани, где происходит преимущественное нарушение метаболизма порфиринов (см. классификация I) [10]. Вместе с тем, порфирии могут подразделяться на формы с поражением кожных покровов и острые, провоцируемые формы (см. классификация II).
– Поздняя кожная порфирия
Острые формы порфирий характеризуются яркой неврологической и вегетативно-сосудистой симптоматикой, в основе которой лежит полинейропатия. При порфирии, обусловленной дефицитом дегидратазы δ-аминолевулиновой кислоты и острой перемежающейся порфирии (ОПП) нет кожных проявлений. Это объясняется тем, что у них активными метаболитами являются предшественники порфиринов (δ-АЛК и порфобилиноген (ПБГ)), которые не имеют сродства к тканям дермы.
При снижении активности ферментов поздних этапов биосинтеза гема происходит накопление собственно порфиринов, избыток которых в дерме приводит к фототоксическим реакциям. Вследствие этого клиника кожных поражений характерна для таких острых порфирий как: наследственная копропорфирия (НКП) и вариегатная порфирия (ВП), а также поздней кожной порфирии (ПКП) и эритропоэтических порфирий.
Этиология и патогенез
Развитие различных форм порфирий связано с нарушениями цикла биосинтеза гема и имеет общие черты. В основе развития каждой формы порфирии лежит генетически обусловленное снижение или отсутствие активности определѐнного фермента в цепи биосинтеза гема (рисунок). Гены ферментов расположены на разных хромосомах и не имеют групповой сцепленности. Снижение активности фермента до 50% от нормы может не иметь клинических проявлений.
При ОП реализовать генетическое носительство и спровоцировать клиническую манифестацию заболевания могут:
-лекарственные препараты (НПВС, барбитураты, цефалоспорины сульфаниламиды и др. список которых представлен в приложении)
Перечисленные факторы приводят к повышенному потреблению конечного продукта цикла биосинтеза – гема (например, активация системы цитохрома Р-450) [10], либо оказывают непосредственное стимулирующее воздействие на активность первого фермента цикла биосинтеза – синтетазы -АЛК, что приводит к повышению еѐ активности (например действие прогестерона) [7], в результате чего ускоряется синтез всех промежуточных продуктов метаболизма порфиринов. На этапе участия дефектного фермента начинается избыточное накопление метаболитов в токсических концентрациях, что приводит к обострению заболевания. При ОП избыточное накопление -АЛК и ПБГ в тканях приводит к сегментарной демиелинизации нервных волокон с нарушением нервной проводимости. Токсическому воздействию подвержены все отделы нервной системы человека.
Периферическая сенсорно-моторная полинейропатия является следствием вторичной демиелинизации нервных волокон.
Вовлечение вегетативной нервной системы имеет следующий патогенез: – поражение абдоминальных вегетативных сплетений сопровождается спазмом сосудов брыжейки и нарушением моторики кишечника.
– ослабление активности n. vagus приводит к преимущественному влиянию на сердечно-сосудистую систему симпатического отдела; этому также способствует 10-ти кратное увеличением экскреции катехоламинов и нарушение функции барорецепторов артериальных сосудов.
Нарушение функции центральной нервной системы является следствием токсического воздействия предшественников порфиринов на нейроны головного мозга и развития длительного спазма артериол, гипонатриемии и гипергидратации, что приводит к тяжѐлым энцефалопатиям.
Поздняя кожная порфирия (ПКП) и эритропоэтические порфирии имеют хроническое течение с периодами обострений, которые могут вызвать:
Повышенная светочувствительность кожных покровов связана с фотохимическими реакциями, спровоцированными порфиринами. Избыток порфиринов в коже подвергается активному воздействию спектра солнечного излучения с длинами волн 400 – 410 нм, что приводит к образованию реактивных частиц, например, супероксид аниона, активирующего ксантин-оксидазу, и других метаболитов, повреждающих клетки базальной мембраны. Повторные атаки приводят к развитию нескольких слоѐв базальных мембран и образованию пласта кровеносных сосудов в поверхностных слоях дермы. Реактивные кислородсодержащие частицы также могут приводить к высвобождению гистамина из тучных клеток, усиливая явления фототоксичности.
Изменения кожи. Уропорфириноген – основной метаболит при поздней кожной порфирии стимулирует синтез фибробластами коллагена. При эритропоэтической протопорфирии жирорастворимый протопорфириноген откладывается в стенке сосудов дермы, приводя к их утолщению.
Пигментирование кожи и гипертрихоз наблюдаются в периорбитальных областях при поздней кожной порфирии и эритропоэтических порфириях, однако, механизм этих изменений до конца не изучен.
Эпидемиология
Порфирии не являются эндемичными заболеваниями и с одинаковой частотой встречаются среди населения всех континентов. Частота встречаемости острых форм порфирий (ОП) по различным оценкам составляет 7-12 случаев на 100 тысяч здоровых людей. В то же время частота бессимптомного носительства генетических дефектов, приводящих к ОП, составляет ~ 50-100 случаев на 100000 человек.
Клиническая картина
Cимптомы, течение
-эритема, волдыри на открытых участках кожи.
Первый приступ острых порфирий может развиться в возрасте старше 14-16 лет, значительно чаще у женщин. Начало заболевания острое, реже подострое. После воздействия порфириногенных факторов появляются боли в животе, конечностях, пояснице, тошнота, рвота. К концу второй недели заболевания появляется мышечная слабость, переходящая в парезы и параличи. Характерны тахикардия (до 110-130 артериальная гипертензия (до 180/100), выделение мочи с красноватым оттенком, неадекватное поведение и галлюцинации. При отсутствии лечения в течение 20-40 дней у больных могут развиться бульбарные нарушения и паралич дыхательной мускулатуры. В анализах крови нередко выявляется гипонатриемия.
Диагностика
Лабораторная диагностика острых порфирий, кроме порфирии обусловленной дефицитом дегидратазы –АЛК основывается на определении в моче избытка порфобилиногена с помощью:
– качественного скрининг-теста свежего образца мочи больного с использованием реактива Эрлиха по методу Watson-Schwartz. При наличии в моче избытка ПБГ образуется окрашенный продукт розово-красного цвета;
– количественного определения содержания ПБГ в моче (норма не превышает 2 мг/л).
При порфирии, обусловленной дефицитом дегидратазы-АЛК в моче, определяется высокая концентрация дельта-аминолевулиновой кислоты при нормальном содержании ПБГ.
Диагноз острой порфирии устанавливается на основании характерной клинической картины и высокого содержания ПБГ или -АЛК в моче [1,17].
Дифференциальный диагноз между ОПП и ВП или НКП основывается при измерении содержания общих порфиринов в кале [1,17]. В норме концентрация порфиринов в кале менее 200 нмоль/г сухого веса. Нормальная концентрация общих порфиринов в кале подтверждает диагноз ОПП. Повышение концентрации в несколько раз свидетельствует в пользу НКП или ВП. При исследовании плазмы спектрофлюориметрическим методом можно дифференцировать НКП от ВП.
Следующим этапом диагностики является определение активности ферментов в клетках крови. Это позволяет подтвердить диагноз у больных с клиническими проявлениями заболеваний и выявить бессимптомных носителей. Несмотря на распространѐнность и удобство диагностики бессимптомного носительства порфирий путѐм оценки активности специфического фермента в клетках, этот метод не является абсолютно достоверным [8,6].
Поэтому заключительным этапом диагностики порфирий у больных и, в особенности, у бессимптомных носителей является проведение ДНК- анализа [2].
Причиной поражения кожных покровов может быть повышенная светочувствительность, как следствие одной из форм порфирий. Тем не менее, следует провести дифференциальную диагностику кожной порфирии с другими дерматологическими заболеваниями.
– определение общих порфиринов в плазме и исследование спектра ее поглощения при флюоресцентной спектроскопии;
Для подтверждения диагноза ЭПП следует провести дополнительный тест – определение общих порфиринов в эритроцитах. При повышенной их концентрации следует измерить соотношение свободного и Zn-связанного протопорфиринов. В случае значительного превышения концентрации свободного протопорфирина подтверждается диагноз ЭПП.
Если результаты всех перечисленных тестов у пациента с активными кожными нарушениями будут нормальными, то диагноз порфирии будет маловероятным..
В случае же получения хотя бы одного или нескольких положительных результатов подтверждается диагноз кожной порфирии, форма которой определяется с помощью диагностических тестов.
Дифференциальный диагноз
– соматизация и синдром хронической усталости
Первичный этап диагностики, на практике, является самым сложным и ответственным для врача. Вариативность течения и симптоматики ОП (особенно при атипичном и моносимптомном вариантах развития) создают значительные трудности в своевременной постановке этого диагноза, нередко уводя врача в сторону ошибочных предположений. Выполнение же скрининг теста на наличие избытка ПБГ в моче всем обращающимся без анализа первичных жалоб нерационально с точки зрения временных и материальных затрат. Опытным путѐм, подтверждѐнным статистическими данными, выделены характерные для ранних сроков течения и специфичные для ОП симптомы. Разработана шкала, содержащая данные анамнеза и симптомы как характерные для клинического течения острых порфирий, так и наиболее часто ложно приписываемых ОП. Скрининг имеющихся у пациентов симптомов и сопоставление этих симптомов с симптоматикой, представленной в таблице (приложение 1)*, позволяет по сумме баллов судить о степени вероятности наличия порфирии у больного. Такой подход позволяет минимизировать число ятрогений, связанных с назначением пациентам с неустановленным диагнозом порфириногенных препаратов.
*В шкале представлены симптомы, встречающиеся при острых порфириях, которым присвоено определенное количество баллов, имеющих как положительные, так и отрицательные значения в зависимости от частоты их встречаемости при острой порфирии. Эти баллы суммируются, и если сумма баллов составляет менее 5 – диагноз острой порфирии маловероятен, если от 5 до 15 баллов – диагноз порфирии возможен, если более 15 баллов, то диагноз острой порфирии высоко вероятен.
Поражение кожных покровов при порфириях следует дифференцировать с прочими дерматологическими заболеваниями.
Лечение
1. Острые порфирии, цель лечения – предупреждение атак заболевания и развития необратимых изменений нервной системы.
Профилактика развития приступов ОП предусматривает ограничение воздействия на организм провоцирующих факторов, а именно:
– приѐма лекарственных препаратов с повышенной порфириногенной активностью, инсоляции развития бактериальных и вирусных инфекции (особенно HCV, HBV, CMV), состояния гипогликемии
– у женщин с доказанной связью между наступлением menses и частыми приступами – предупреждение менструаций.
Если менструальные циклы часто (три и более раз в год) провоцируют атаки ОП, репродуктивную функцию необходимо подавлять, для чего используют оральные контрацептивы – Ригевидон, Овидон; ГнРГ- Золадекс, синарел; андрогены – сустанон, андриол; овариоэктомия в отдельных случаях. Отмена овариосупрессии производится после достижения длительного бесприступного (несколько месяцев и более) течения заболевания.
Лечение начинают при наличии нескольких симптомов ОП (см. выше) и повышении показателей порфиринового обмена (по сравнению с предыдущими данными в динамике). При развитии острого приступа необходимо немедленное начало патогенетической терапии для подавления избыточного биосинтеза порфиринов:
2. Обеспечение избыточного поступления в орагнизм углеводов (200-600гр сухого вещ-ва глюкозы). 40%-1000мл в/в капельно в сутки, ежедневно, 2-4 недели [4].
3. Сандостатин в дозе 100-500 мкг/сут., подкожно, ежедневно на протяжении от 4-х недель до 6 месяцев в сочетании с плазмаферезами 6-10 сеансов [13].
4. Рибоксин 2%-10мл в разведении на 100-200 мл 0.9% раствора NaCl, в/в капельно 1-2 раза в сутки, ежедневно 2-4 недели.
Порфирия
Порфирии — группа генетически обусловленных патологий, проявляющихся на фоне нарушения синтеза гема (промежуточного продукта метаболизма гемоглобина) и накопления его токсичных соединений в организме человека. Симптоматика заболеваний разнообразна: пациенты могут сталкиваться со светочувствительностью, высыпаниями на коже, хроническими болями в животе, частичным или полным параличом, острыми психозами. Диагностика метаболического расстройства осуществляется посредством молекулярно-генетических тестов и лабораторных анализов биоматериалов, полученных врачами от ребенка или взрослого. Медикаментозная терапия направлена на снижение концентрации токсических метаболитов в крови пациента. Хирургические вмешательства выполняются при осложненном течении патологии.
Общая информация
Порфириновая болезнь диагностируется сравнительно редко: российские врачи выявляют не более 12 случаев на 100 тысяч человек. Различные формы патологии получают распространение в отдельных регионах Земли. Так, признаки поздней кожной порфирии часто выявляется у жителей Южной Африки (1 случай на 800 человек). Острый перемежающийся тип заболевания характерен для жителей Северной Европы (1 случай на 1000 человек). Мужчины и женщины одинаково часто страдают от различных форм синтеза гема.
Причины развития
Основным фактором, провоцирующим развитие заболевания, становятся генетические мутации в организме носителя. Единственным исключением остается поздняя кожная порфирия — ее происхождение связано с патологиями печени или длительными интоксикациями человеческого организма солями тяжелых металлов.
Порфириновая болезнь относится к наследуемым метаболическим расстройствам. Отдельные симптомы порфирии или приступы сопровождающих ее психозов могут проявиться в любом возрасте. Специфический набор признаков патологии формируется после преодоления пациентом пубертатного возраста.
Синтез гема состоит из восьми последовательных этапов, протекающих под действием ферментов. Выработка сложных белковых соединений кодируется определенным геном. Порфириновая болезнь приводит к образованию ферментативных дефектов. Разные формы заболевания развиваются на фоне повреждения различных генетических кодов. Гем состоит из порфиринов, объединенных с железом. Продуцирование этих соединений выполняется тканями печени и костного мозга. На основании гема формируются гемоглобин. Нарушение его синтеза приводит к образованию токсичных метаболитов, скапливающихся в тканях человеческого организма.
Провоцирующими факторами манифестации порфириновой болезни становятся:
- избыточная инсоляция;
- недостаточное питание и скудный рацион;
- систематические стрессы;
- чрезмерное употребление алкоголя;
- вирусные и бактериальные инфекции;
- хронические интоксикации солями тяжелых металлов.
В отдельных случаях обострение патологии происходит из-за приема пациентами антибиотиков, антиконвульсантов, нестероидных противовоспалительных средств, пероральных контрацептивов.
Этиология
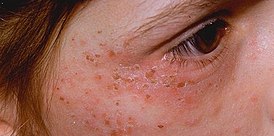
Нарушение химического состава ферментов, участвующих в продуцировании гема, приводит к формированию токсичных для человека метаболитов. Хронические формы порфирии характеризуются накоплением в тканях протопорфирина, копропорфирина и уропорфирина. Острые типы заболевания развиваются на фоне повышенной концентрации в крови порфобилиногена и дельта-аминолевулиновой кислоты (ДАЛК).
Накопление порфиринов в кожных покровах детей и взрослых происходит под действием ультрафиолета. Побочным эффектом этого процесса становится окисление липидов. Под действием солнечного света погибают клетки кожи. Копропорфирин провоцирует усиление пигментации дермы и усиленный рост волос. Отложение протопорфирина в печени становится причиной закупорки желчных протоков. Уропорфирины приводят к ускоренной деструкции эритроцитов в селезенке. ДАЛК и порфобилиноген накапливаются в нервных тканях и запускают процесс дегенерации аксонов.
Виды патологии
Врачи используют несколько типологий порфириновой болезни, основанных на клинической симптоматике, локализации нарушений метаболизма порфиринов или вовлеченных тканей. Наиболее часто гематологи выделяют три формы патологии: эритропоэтическую, острую печеночную и хроническую печеночную.
Эритропоэтический тип заболевания характеризуется поражением кожных покровов под действием солнечных лучей. Данная форма патологии рассматривается врачами как наиболее тяжелая.
Острые печеночные виды порфириновой болезни характеризуются приступообразным течением. Основной мишенью токсичных метаболитов гемоглобина становится нервная система. В редких случаях заболевание осложняется светочувствительностью.
Хронические печеночные болезни часто сопровождаются появлением поздней кожной порфирии. ПКП может оказаться наследственной или приобретенной патологией. Врачи рассматривают ее как наиболее благоприятный для лечения вид порфириновой болезни.
Симптомы
Ранние симптомы порфирии неспецифичны. Сроки дебюта рассмотренных выше форм заболевания различны: эритропический тип проявляется в 3–5 лет, острый печеночный — в 14–16 лет, хронический печеночный — после 40 лет. Вслед за манифестацией патологии пациенты сталкиваются со специфической симптоматикой.
Острые симптомы включают боли в животе, задержку стула, резкое повышение частоты сердечных сокращений, рост артериального давления, изменения окраски мочи. Пациент страдает от снижения чувствительности конечностей, ощущения ломоты в костях и суставах. Появляется мышечная слабость, в тяжелых случаях — паралич.
Позднее развиваются судорожные припадки, бред и галлюцинации.
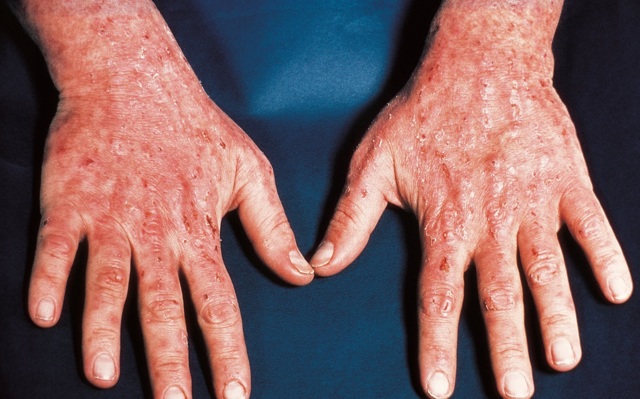
ПКП характеризуется формированием участков гиперпигментации кожных покровов под воздействием солнечного света. Высыпания землистого или бронзового цвета возникают на лице, шее, ушных раковинах и кистях рук. При осложненном течении патологии пациент сталкивается с гипертрихозом: избыточный рост волос локализуется на лобно-височной области лица. На коже появляются пузыри-пустулы с жидким содержимым. Вскрывшийся очаг образует эрозию, после заживления которой образуется атрофический рубец.
Эритропоэтическая форма порфириновой болезни провоцирует развитие у пациента более выраженных признаков светочувствительности в сравнении с ПКП. Ребенок или взрослый испытывает сильную боль при попадании на кожу прямых солнечных лучей. Очаги эрозии занимают значительную площадь и приводят к формированию грубых рубцов, меняющих внешность человека. Рубцовая ткань снижает подвижность локтевых и коленных суставов. Моча пациента обретает красный или розовый оттенок, эмаль зубов становится красно-коричневой. Кожные покровы лица и тыльной поверхности кистей грубеют и утолщаются.
Диагностические мероприятия
Диагностика порфирии выполняется гематологом. Врач осматривает ребенка или взрослого и включает в анамнез все симптомы, которые могут указывать на нарушения в процессе синтеза гема. Пациенту предстоит ответить на вопросы о принимаемых медикаментах, режиме питания, перенесенных инфекционных заболеваниях. Девушек врач расспрашивает о стабильности менструального цикла, беременностях и абортах.

Следующим этапом диагностики становятся лабораторные тесты. Пациентам назначаются:
-
и биохимический анализы крови;
- проба Эрлиха;
- исследование концентрации ферментов в крови;
- ПЦР-тесты на гепатит;
- молекулярно-генетические исследования.
При наличии соответствующих показаний ребенок или взрослый посещает консультацию дерматолога, нефролога и гастроэнтеролога. Дифференциальная диагностика позволяет врачам исключить из анамнеза пациента неврологические и психиатрические патологии.
Терапевтический курс
Лечение острой и эритропоэтической порфирии требует госпитализации пациента. Лица, страдающие ПКП, могут проходить терапию в амбулаторных условиях. Современная медицина не располагает средствами, позволяющими полностью устранить нарушения в обмене порфиринов. Усилия врачей направлены на устранение симптомов заболевания и факторов, провоцирующих его обострения.
При острых формах патологии ребенку или взрослому назначаются производные аденозинтрифосфата, подавляющие синтез токсичного порфобилиногена. Дальнейшее лечение предусматривает прием пациентом больших дох глюкозы и переход на высокоуглеводную диету.
Эритропоэтический тип заболевания почти не поддается лечению. Основной терапевтической мерой становится ограничение пребывания пациента под солнечными лучами. Эрозии следует обрабатывать антисептическими средствами для предупреждения инфекционных поражений кожных покровов. Выраженный гемолиз (разрешение эритроцитов) становится показанием к удалению селезенки. В отдельных случаях пациентам показана трансплантация костного мозга.
При поздней кожной порфирии мужчинам и женщинам назначается плазмаферез и медикаментозная терапия. Применяемые препараты призваны снизить уровень всасывания порфиринов в ЖКТ.
Прогноз
Порфириновая болезнь относится к патологиям с неблагоприятным прогнозом. Пациенты с эритропоэтическим типом расстройства проживают 25–30 лет после постановки диагноза и начала лечения. Причиной смерти в 85% случаев становятся вторичные инфекции, развившиеся на фоне ослабления иммунитета человека. Острые порфирии завершаются летальным исходом в 15–20% клинически регистрируемых случаев. Смерть пациента наступает в результате паралича дыхательных мышц.
ПКП остается сравнительно благоприятной формой порфириновой болезни. Мужчинам и женщинам рекомендуется избегать провоцирующих осложнения факторов: скудного рациона, стрессов, избыточной инсоляции.
Диагностика и лечение порфирии в Москве
АО «Медицина» (клиника академика Ройтберга) обладает всем необходимым оборудованием для диагностики и лечения расстройств синтеза гема у детей и взрослых. Прием пациентов осуществляется в современном диагностическом комплексе, построенном с учетом последних достижений медицины.
Вопросы и ответы
Какой врач лечит порфириновую болезнь?
Лечение патологии осуществляется гематологом. При осложненном течении заболевания пациенту могут потребоваться консультации с другими врачами — иммунологом, терапевтом, нефрологом или гастроэнтерологом.
Передается ли порфирия от носителя к здоровому человеку?
Передача патологии от носителя к здоровому человеку невозможна. Заболевание наследуется детьми от родителей или приобретается под действием факторов риска.
Существует ли комплекс профилактических мер, позволяющих предупредить расстройство синтеза гема?
Современная медицина не располагает средствами для профилактики данной патологии. Носителям заболевания, планирующим рождение детей, следует посетить генетика. Врач изучит анамнезы потенциальных родителей и назначит паре необходимые анализы. Результаты лабораторных исследований позволят оценить вероятность развития порфириновой болезни у ребенка.
Подводные камни в диагностике острой перемежающейся порфирии: описание клинического случая

Острая перемежающаяся порфирия — это редкое заболевание с аутосомно-доминантным типом наследования, вызванное дефицитом фермента гидроксиметилбилан-синтазы. Распознавание острых нейровисцеральных атак может быть затруднено из-за неспецифического характера симптомов.
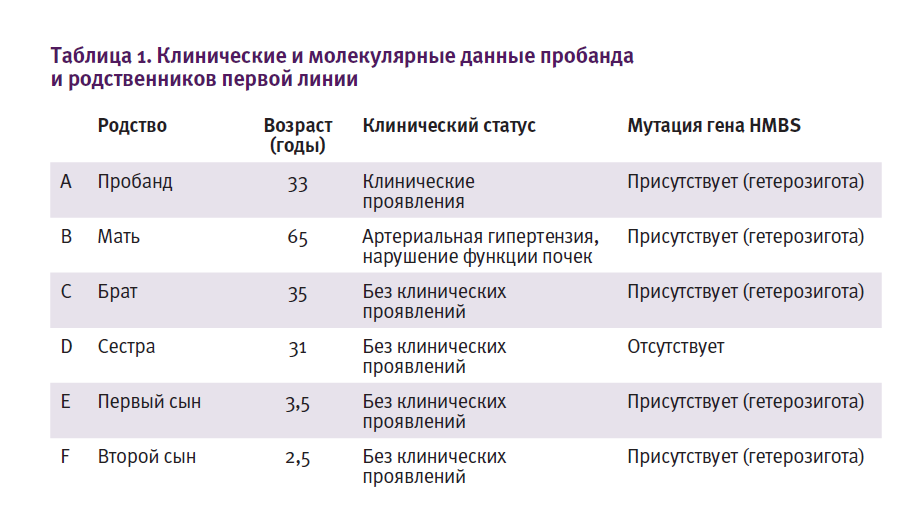
Описание случая. В статье описывается клинический случай 33-летнего пациента, у которого отмечались рецидивирующие эпизоды сильной боли в животе, тошноты, рвоты, запора и онемения обеих нижних конечностей. Эти неспецифические нейровисцеральные приступы стали причиной ошибочных диагнозов острого аппендицита, синусовой тахикардии, камней в почках, острого лекарственного интерстициального нефрита и двух эпизодов частичной кишечной непроходимости. Шестой острый приступ вызвал подозрение на острую порфирию. Проба Уотсона-Шварца была положительной на порфобилиноген в моче. Анализ мутаций путем секвенирования ДНК, выделенной у пробанда, выявил ранее определенную миссенс-мутацию c.517C→ T, кодирующую p.R173W в гене HMBS , что подтверждает диагноз острой перемежающейся порфирии. Мутация также была выявлена у четырех из пяти членов семьи, которым был проведен таргетный мутационный анализ.
Заключение. Наиболее часто клиническая картина острой перемежающейся
порфирии характеризуется болью в животе с нейровисцеральными проявлениями, которые также наблюдаются при некоторых других соматических, психиатрических и хирургических патологиях. В связи с этим данное заболевание часто диагностируют неправильно, что приводит к неверному лечению и развитию тяжелых осложнений. Следовательно, для диагностики важны высокий уровень настороженности, а также осведомленность об основных лабораторных исследованиях. Точный диагноз
позволяет реализовать стратегии по предотвращению острых приступов, а также выполнить генетическое тестирование и провести консультирование членов семьи, относящихся к группе риска.
Сокращения
ОПП — острая перемежающаяся порфирия; ALA — аминолевулиновая кислота; ИМТ — индекс массы тела; ДНК — дезоксирибонуклеиновая кислота; HMBS — гидроксиметилбилансинтаза; PBG — порфобилиноген;
PBGD — порфобилиноген деаминаза; ПЦР — полимеразная цепная реакция.
Общие сведения
Острая перемежающаяся порфирия (ОПП) является острой порфирией с аутосомно-доминантным типом наследования. Заболевание вызвано
мутациями в гене, кодирующем гидроксиметилбилан-синтазу.
(HMBS) — третий фермент в пути биосинтеза гема. Название этого фермента используется как синоним порфобилиногендеаминазы (PBGD)[1]. На сегодняшний день выявлено более 400 мутаций в гене HMBS [2]. Наиболее частый клинический симптом — острая сильная боль в животе. При острых приступах у пациентов наблюдаются нейровисцеральные симптомы, включая рвоту, диарею, запоры, мышечную слабость, онемение, недержание или задержку мочи, сердцебиение, тремор и судороги, а также изменения поведения, такие как раздражительность, бессонница и эмоциональная лабильность.
Клинический случай
33-летний пациент поступил в специализированный госпиталь с перемежающимися болями в животе, тошнотой, рвотой, запором и онемением обеих нижних конечностей на протяжении 3-х дней. Он получал консервативное лечение в хирургическом отделении по поводу частичной кишечной непроходимости и ожидал диагностической лапароскопии. У пациента развилась спутанность сознания, также у него обнаружилась системная гипертензия, и его перевели в терапевтическое отделение для дальнейшего лечения. Пациент не страдает сахарным диабетом, артериальной гипертензии ранее не отмечалось. В анамнезе применение безрецептурных анальгетиков в течение 6 недель.
На протяжении 2-х последних лет были аналогичные нейровисцеральные приступы, потребовавшие пяти неотложных госпитализаций с постановкой различных клинических диагнозов. Шестой острый приступ вызвал подозрение на острую порфирию. Во время первого приступа в январе 2013 года был диагностирован аппендицит. Поскольку после операции симптомы ухудшились, было проведено экстренное лапароскопическое исследование.
Однако диагностическая лапароскопия не выявила причин, объясняющих
ухудшение симптомов. Второй приступ протекал в форме синусовой
тахикардии, и пациент начал получать бета-адреноблокаторы. Третий приступ, сопровождавшийся лихорадкой, был расценен как почечная колика и купирован консервативным лечением. Четвертый приступ был осложнен транзиторной гипонатриемией и преходящим повышением уровня креатинина в сыворотке. Врачи связывали эти осложнения с интерстициальным нефритом на основании того факта, что пациент принимал 50 мг диклофенака натрия два раза в сутки в течение 6 недель по назначению врача общей практики. Еще один приступ, произошедший в 2015 году, лечили как частичную кишечную непроходимость. Была выполнена диагностическая лапароскопия. Во всех этих случаях результаты ультразвукового исследования и диагностической лапароскопии не подтвердили хирургическую патологию. При осмотре пациент имел астеническое телосложение (ИМТ = 20 кг/м2), был бледным. Артериальное давление, измеренное на плечевой артерии, составило 160/90 мм рт. ст. На брюшной стенке имелись шрамы от предыдущих операций, в остальном без особенностей. Мышечная сила составила 4/5 во всех четырех конечностях (движение в полном объеме при действии силы тяжести и при небольшом внешнем противодействии).
Лабораторные исследования, проведенные во время этой госпитализации, выявили тяжелую гипонатриемию 115 ммоль/л (136-145)** с осмоляльностью сыворотки 255 мОс-моль/кг (275-295) и осмоляльностью мочи 460 мОсмоль/кг (50-1200). Концентрация креатинина в сыворотке составила 106 мкмоль/л (80-115) при уровне мочевины в крови 20 мг/дл (6-20). Концентрация гемоглобина составляла 8,2 г/дл (13,5-17,5), анемия была нормохромная и нормоцитарная. Уровень общего холестерина составлял 282 мг/дл (5-95-й центиль; 142-258) с фракцией ЛПНП 225 мг/дл (5-95-й центиль; 78-185). Уровень сывороточного ферритина составлял 646 нг/мл (20-250). Анализ газов артериальной крови указывал на метаболический ацидоз. На эхокардиограмме отмечались признаки гипертрофии левого желудочка. Результаты рентгенографии брюшной полости и УЗИ брюшной полости были без особенностей. Концентрация свинца в крови составляла 3 мкг/дл (<5). Образец мочи, взятый во время острого приступа, был отправлен для биохимического анализа. При
отстаивании образец мочи постепенно становился темно-коричневым. Проба Уотсона-Шварца была положительной на порфобилиноген (PBG) в моче (рис. 1). Спектрофотометрия мочи на содержание общего уровня порфиринов показала «пик Соре». Общий уровень порфиринов в моче, рассчитанный с использованием скорректированной по Аллену абсорбции в образце мочи, составил 5505,5 нмоль/л (<300).

Генетические исследования проводились в зарубежной лаборатории. Полный анализ гена HMBS был выполнен с помощью ПЦР-амплификации выделенной ДНК с последующим экзон-специфическим анализом методом удлинения
праймеров для всех экзонов, границ экзонов/интронов и промоторных областей.
Анализ генов выявил ранее зарегистрированную миссенс-мутацию c.517C→T, кодирующую p.R173W в гене HMBS. Анализ целевых мутаций проводили путем ПЦР-амплификации выделенной ДНК с последующим анализом методом удлинения аллель-специфического праймера у пяти родственников
первой линии. Четыре из них были гетерозиготными по одной и той же
мутации гена HMBS (рис. 2 и табл.1).

Поскольку аргинат гема в Шри-Ланке недоступен, пациент получал только симптоматическое лечение. Углеводная нагрузка с внутривенным введением декстрозы и пероральным приемом углеводов была единственно возможным вариантом. Была проверена безопасность всех лекарственных препаратов, использованных для симптоматического лечения, на предмет риска острых
порфирий. Пациент был выписан из отделения, когда симптомы постепенно улучшились в течение 6 дней, для продолжения амбулаторного лечения. Оценить ответ на лечение не представлялось возможным из-за недоступности в Шри-Ланке количественных тестов для измерения аминолевулиновой кислоты (ALA) и PBG в моче.
Пациента проинформировали о факторах, провоцирующих развитие острой порфирии. Ему была предоставлена диагностическая карточка с информацией о лекарственных препаратах, применения которых следует избегать. Пациент
наблюдался в клинике с регулярным контролем функции почек, уровня гемоглобина и артериального давления. Наблюдение за пациентом в течение 1 года после постановки диагноза показало, что он перенес два легких приступа, которые не требовали стационарного лечения.
Исследования нервной проводимости не выполнялись, поскольку в интервалах между острыми приступами неврологических симптомов не наблюдалось. Родственникам, унаследовавшим мутацию HMBS, у которых не отмечалось клинических проявлений, также было рекомендовано избегать триггеров острых приступов, таких как определенные лекарственные препараты, голодание, алкоголь и гормоны. Брат пробанда получил консультацию относительно риска того, что его дети унаследуют мутацию HMBS, и рекомендацию выполнить генетическое исследование целевой мутации у обоих детей.
Обсуждение и выводы
Несмотря на то что ОПП является наиболее распространенным типом
острой печеночной порфирии, предполагаемая распространенность этого заболевания в странах Европы составляет 5,4 на 1 миллион [5]. Данные о распространенности этого заболевания в Шри-Ланке отсутствуют. Обзор литературы не выявил каких-либо предыдущих сообщений о случаях пациентов с ОПП, подтвержденной генетическим анализом, из Шри-Ланки.
Поскольку порфирии встречаются редко, клиницисты нечасто сталкиваются с этими расстройствами, а учебная программа медицинских школ уделяет им очень мало внимания. Проба Уотсона-Шварца является скрининг-тестом для анализа мочи на PBG. 2 мл мочи смешивают с равным количеством реактива Эрлиха. Если присутствует PBG, он образует комплекс порфобилиноген-реактив Эрлиха — красный хромоген, который обычно нерастворим в хлороформе и N-бутаноле. При добавлении хлороформа PBG экстрагируется и придает красный цвет верхнему водному слою, тогда как комплекс уробилиноген-реактив Эрлиха экстрагируется в слой хлороформа. Поскольку у пациентов при острых приступах выделяются большие количества PBG, ложноотрицательные результаты во время острого приступа редки. Спектрофотометрия подкисленной мочи — это полуколичественный метод, который можно использовать в качестве скринингового теста для определения общего уровня порфиринов в моче. Все порфирины имеют полосу поглощения
при длине волны около 400 нм. Хотя в Шри-Ланке сложные методы не являются широкодоступными, простые надежные лабораторные тесты весьма эффективны для постановки диагноза порфирии [6], [7]. На сегодняшний день количественные тесты для определения уровней PBG, ALA, уропорфирина и копропорфирина, а также генетические исследования на порфирию в Шри-Ланке недоступны.
Окончательный диагноз порфирии следует устанавливать в зарубежной лаборатории. Молекулярно-диагностические исследования эффективны не только для биохимического подтверждения ОПП, но и для выявления членов семьи, подверженных риску [8]. По оценкам, пенетрантность острых приступов составляет примерно 1% у гетерозигот с вероятными патогенными вариантами HMBS [9]. Ранее сообщалось о мутации R173W в Швеции, России,
Испании, Великобритании, Японии и Китае. Мутация R173W по сравнению с другими распространенными мутациями может иметь более высокую клиническую пенетрантность и повышенный риск проявления заболевания. Эта миссенс-мутация представляет собой замену C-T в нуклеотиде 517 в экзоне 10. Превращение аргинина в триптофан в мутантном белке приводит к снижению активности фермента. Несмотря на то что активность PBGD в эритроцитах может быть использована в качестве показателя тяжести заболевания, у некоторых пациентов с острыми приступами его уровни могут быть нормальными [10]-[16]. Наиболее эффективным методом лечения острых
приступов является внутривенное введение аргината гема, который доступен в Европе и многих других странах мира, но не в Шри-Ланке.
Необходимо устранение провоцирующих факторов. При легких приступах может оказаться эффективной нагрузка углеводами. При проведении терапии необходимо контролировать уровни выделения ALA и PBG с мочой, чтобы оценить ответ. Поддерживающее лечение включает наркотические анальгетики, противорвотные средства, анксиолитики, восстановление и контроль баланса жидкости и психологическую поддержку. Стратегии борьбы с рецидивирующими острыми приступами подразумевают устранение потенциальных триггерных факторов и профилактические инфузии гемина [17, 18]. Однако данный пациент столкнулся с такими проблемами, как отсутствие аргината гема для неотложной терапии и профилактики, а также отсутствие контроля за ответом на лечение путем количественного измерения уровней ALA и PBG из-за недоступности и чрезмерно высокой стоимости этих средств. Поэтому длительное разрешение симптомов у этого пациента не представляется возможным. У пациентов с острой перемежающейся порфирией обычно отмечаются острые приступы с нейровисцеральными проявлениями, которые также наблюдаются при некоторых других соматических, психиатрических и хирургических патологиях. Таким образом, пациенты с порфирией, включая острые порфирии, потенциально могут столкнуться с проблемой недостаточной и неправильно диагностики, что значительно увеличивает время между появлением симптомов и подтвержденным диагнозом, приводит к неверному лечению и потенциально серьезным необратимым инвалидизирующим последствиям и даже вплоть до
Ошибочные клинические диагнозы у пациентов с острой порфирией могут стать причиной осложнений из-за возможного назначения порфирогенных препаратов [19]. При постановке неправильного хирургического диагноза проводятся ненужные хирургические вмешательства, такие как аппендэктомия и диагностическая лапароскопия.
Зарегистрированы сообщения о случаях ОПП с психозом в виде единственного клинического проявления [20]. У пациентов с ОПП, которым
поставлен психиатрический диагноз, могут возникнуть осложнения из-за некоторых антипсихотических средств, которые способны значительно ухудшить симптомы пациента с острой порфирией. Следовательно, для надлежащего установления диагноза важны высокий уровень настороженности, а также осведомленность о лабораторных исследованиях первой линии. Точный диагноз у пациента с ОПП позволяет реализовать стратегии по предотвращению острых приступов, а также провести скрининг и генетическое консультирование членов семьи, относящихся к группе риска.


