Карцинома толстой кишки
Карцинома толстой кишки — это злокачественная опухоль, которая развивается из эпителиальных клеток слизистой оболочки толстого кишечника. На ее долю приходится около 95% всех случаев рака данной локализации.
Причиной развития карциномы толстой кишки является злокачественная трансформация клеток ее эпителия, в результате чего они начинают бесконтрольно размножаться. Что служит причиной такой трансформации до конца неизвестно, и на этот вопрос предстоит ответить в будущем. Пока можно только говорить о факторах риска, увеличивающих вероятность развития злокачественных новообразований толстой кишки. К ним относят:
- Аденоматозные полипы. Карциномы практически никогда не развиваются на здоровом эпителии. Им всегда предшествуют доброкачественные гиперплазии ткани, коими и являются полипы. Следует отметить, что не каждый полип превратится в рак. Здесь также есть группы риска. Наиболее склонны к малигнизации аденоматозные полипы размером более 1 см, располагающиеся на широком основании. Другие виды полипов тоже способны к злокачественной трансформации, но случается это реже.
- Гастрономические особенности. Одним из основных факторов способствующих развитию колоректального рака является нерациональное питание, а именно переедание, употребление большого количества жиров животного происхождения, жареных, соленых, острых, копченых и маринованных блюд.
- Возраст старше 50 лет. Рак толстой кишки редко диагностируется у людей младше 40, но при увеличении возраста, количество больных возрастает.
- Наследственная предрасположенность. Около 5% карцином толстой кишки имеет семейный характер и развивается на фоне наследственных заболеваний — наследственного неполипозного рака толстой кишки или семейного аденоматозного полипоза.
- Наличие хронических заболеваний толстого кишечника — болезнь Крона или неспецифический язвенный колит.
- Первичные и вторичные иммунодефициты.
Таким образом, в группу риска входят следующие категории лиц:
- Люди старше 50 лет.
- Люди с хроническими заболеваниями толстого кишечника — полипы, неспецифический язвенный колит, болезнь Крона.
- Люди, не придерживающиеся принципов здорового питания.
- Люди, злоупотребляющие алкоголем.
Классификация и симптомы
С точки зрения гистологического строения, выделяют следующие виды карцином толстой кишки:
- Тубулярная аденокарцинома. Она образована специфическими трубчатыми структурами. Характеризуется небольшими размерами и нечеткостью контуров и границ.
- Муцинозная аденокарцинома. Ее характерным признаком является продуцирование большого количества слизи. Она может занимать более половины объема злокачественной клетки, что хорошо видно во время морфологического исследования. Этот вид карциномы относится к низкодифференцированным формам рака, поэтому он отличается агрессивным течением и неблагоприятным прогнозом.
- Перстневидноклеточная аденокарцинома. Этот вид рака также имеет высокую степень злокачественности. На ранних стадиях диагностируется редко, поскольку не имеет выраженных проявлений даже при обследовании с помощью колоноскопии. Выявляется в 1-2% случаев всех карцином толстой кишки.
Стадии карциномы толстой кишки
1 стадия — опухоль не выходит за пределы слизистой оболочки толстой кишки.
2 стадия — карцинома прорастает стенку кишки по всей толщине.
3 стадия — опухоль выходит за пределы кишечной стенки в брюшную полость или полость малого таза, либо имеются метастазы в регионарные лимфатические узлы.
4 стадия — опухоль распространяется по серозной оболочке брюшной полости (канцероматоз брюшины), либо дает метастазы во внутренние органы.
Симптомы
Симптомы рака толстой кишки начинают проявляться, когда опухоль достигает значительных размеров. Сначала это неспецифические проявления:
- Повышенная утомляемость.
- Похудение.
- Нарушение аппетита.
- Явления диспепсии — вздутие живота, запоры, диареи.
По мере роста опухоли присоединяются более специфичные симптомы. Например, при изъязвлении стенок слизистых покровов характерны скрытые кровотечения. Они не определяются визуально, но их можно обнаружить с помощью проведения специального теста — анализ кала на скрытую кровь. Этот тест используется в некоторых странах для скрининга колоректального рака. Косвенным признаком скрытого кровотечения является развитие хронической анемии.
- Новообразования больших размеров могут осложняться распадом опухоли с развитием внутрикишечных кровотечений, основным признаком которых является кровь в кале.
- При локализации опухоли в верхних и средних отделах кишечника возникает мелена — полужидкий кашицеобразный черный стул, его еще называют дегтеобразным стулом. Он возникает из-за ферментации крови в толстом кишечнике.
- При распаде опухолей прямой кишки возникает выделение крови из заднего прохода или обнаруживаются примеси алой крови в кале.
- На фоне кровопотери развивается анемия — падение уровня гемоглобина, головокружение, слабость, бледность кожи.
Кишечная непроходимость
Кишечная непроходимость развивается из-за обтурации просвета кишки опухолью. Симптоматика будет определяться местом расположения новообразования. Правый отдел толстого кишечника имеет широкий просвет, поэтому непроходимость развивается редко и в основном на терминальных стадиях. Левый отдел толстой кишки имеет более узкий просвет, а кишечное содержимое в нем более плотное. Поэтому возникновение кишечной непроходимости в этом случае является частым признаком. При этом пациенты отмечают отсутствие стула, схваткообразные боли в животе, вздутие живота, резкое ухудшение состояние.
В ряде случаев непроходимость имеет компенсированный характер. Периодически развиваются запоры, которые через некоторое время сменяются зловонными поносами, которые связаны с тем, что кишечная микрофлора запускает процессы гниения и брожения, разжижающие плотные каловые массы. Рано или поздно частичная кишечная непроходимость становится полной и требует лечения в условиях стационара.
Метастазирование карциномы толстой кишки
Карцинома толстого кишечника может давать метастазы несколькими способами:
- Лимфогенный. С помощью лимфы злокачественные клетки сначала достигают регионарных лимфатических узлов, а потом разносятся более отдаленные группы, в частности могут поражаться надключичные лимфоузлы.
- Гематогенный путь. Он реализуется посредством тока крови. Как известно, раковые опухоли имеют обильную сосудистую сеть, причем внутренней выстилкой сосудов являются сами раковые клетки, они отрываются и мигрируют с током крови по всему организму. При колоректальном раке чаще всего поражается печень и легкие, при низкодифференцированных опухолях могут быть метастазы в костный мозг.
- Контактный путь. При прорастании рака за пределы стенки кишки, злокачественные клетки могут имплантироваться в соседние органы и ткани: печень, брюшину, параректальную клетчатку и др.
Диагностика новообразований толстой кишки
Для обнаружения рака толстой кишки проводится колоноскопия — осмотр всей поверхности толстой кишки посредством гибкой фиброскопической трубки. С ее помощью можно визуализировать новообразование, уточнить его размеры и взять биопсию. Для обнаружения опухоли терминальных отделов кишечника допустимо проводить ректороманоскопию или ректосигмоскопию — осмотр прямой и сигмовидной кишки. После постановки диагноза все равно необходима колоноскопия, поскольку есть вероятность нахождения синхронных злокачественных опухолей в других отделах кишечника. Если колоноскопия на дооперационном этапе невозможна, ее проводят после операции.
Материал, полученный с помощью биопсии, отправляется в лабораторию для морфологического и молекулярно-генетического исследования. Только после получения результата проводится планирование лечения.
Для уточнения стадии распространения заболевания, проводят дополнительные методы исследования, которые позволят более точно определить размеры опухоли, ее взаимоотношение с другими органами, а также выявить метастазы в лимфатические узлы и внутренние органы:
- КТ.
- МРТ.
- Рентген грудной клетки.
- УЗИ органов брюшной полости.
Для поиска микрометастазов и метастазов в костный мозг используется ПЭТ-КТ, в основе которых лежит применение радиоактивных препаратов, которые в повышенных количествах накапливаются злокачественными клетками и хорошо визуализируются на снимках.

Из лабораторных методов исследования применяют:
- Общий анализ крови — при колоректальном раке часто развиваются анемии.
- Анализ кала на скрытую кровь — позволяет заподозрить наличие скрытого кровотечения, источником которого часто является колоректальный рак.
- Определение онкомаркеров. Наиболее специфичен для КРР раково-эмбриональный антиген.
Скрининг рака толстой кишки
Скрининг рака толстой кишки направлен на обнаружение опухоли у лиц из группы риска, которые не предъявляют жалоб и считают себя здоровыми. Разные страны, в зависимости от своих финансовых возможностей, предлагают следующие программы:
- Анализ кала на скрытую кровь. Это метод позволяет заподозрить наличие кровоточащих опухолей с изъязвленной поверхностью. Недостатком метода является относительно низкая чувствительность и специфичность. Во-первых, методика работает только в отношении кровоточащих опухолей. Другие новообразования, с неповрежденной поверхностью, которая обычно бывает на ранних стадиях, таким методом не обнаруживаются. Вторым моментом является то, что тест может дать положительный результат при наличии других заболеваний ЖКТ, сопроводающихся скрытыми кровотечениями и незначительной кровоточивостью. Сюда относят доброкачественные полипы, воспалительные заболевания толстой кишки, язвы желудка и 12-перстной кишки и даже пародонтит, при котором развивается повышенная кровоточивость десен. Если у пациента обнаруживается положительный тест на скрытую кровь, его направляют на дальнейшее обследование.
- Колоноскопия. Тотальная колоноскопия является золотым стандартом раннего обнаружения рака толстой кишки и, что самое главное, предраковых заболеваний. Как мы знаем, в подавляющем количестве случаев колоректальный рак развивается из имеющихся полипов. Если их своевременно удалить, заболевание удастся предотвратить. Малигнизация полипов происходит в течение многих лет, поэтому колоноскопию рекомендуют делать хотя бы 1 раз в 3 года, начиная с 50-летнего возраста.
Лечение карциномы толстой кишки
Хирургическое вмешательство
Оптимальным методом лечения рака толстой кишки является его радикальное хирургическое удаление. Радикальность операции должна подтверждаться срочным гистологическим исследованием на предмет наличия злокачественных клеток в краях отсечения. Если опухоль проросла в соседние органы, производят их резекцию единым блоком. Одномоментно производят удаление регионарных лимфатических узлов.
Если опухоль находится в нерезектабельном состоянии, проводят паллиативные вмешательства, направленные на проедотвращение развития кишечной непроходимости. С этой целью накладывают обходные анастомозы, производят стентирование опухоли или накладывают колостому — приводящий отдел кишки выводят на переднюю брюшную стенку. После этого пациента переводят на химиотерапевтическое лечение.
Химиотерапия
Химиотерапия при раке толстой кишки применяется в рамках комбинированного лечения, а также используется как самостоятельный метод лечения при нерезектабельных опухолях и/или при наличии отдаленных метастазов. При комбинированном лечении, ХТ может использоваться в адъювантных и неоадъювантных режимах.
Адъювантная ХТ показана в следующих случаях:
- Распространение опухоли за пределы кишечной стенки.
- Наличие регионарных метастазов.
- Наличие злокачественных клеток в краях отсечения опухоли.
- Низкодифференцированные формы рака.
Неоадъювантная химиотерапия может применяться при некоторых нерезектабельных формах рака для перевода их в операбельное состояние. Примером может служить применение химиолучевой терапии при местно-распространенном раке прямой кишки.
Таргетная терапия при карциноме толстой кишки
Таргетная терапия воздействует на молекулярные мишени, которые отвечают за ключевые процессы жизнедеятельности злокачественных клеток. Для рака толстой кишки такими мишенями является эпидермальный фактор роста EGFR и сосудистый фактор роста.
Контакт лиганда с EGFR запускает химические процессы, отвечающие за рост и размножение. Если блокировать этот рецептор, передача сигнала станет невозможной и процесс размножения опухолевых клеток прекратится. Существует много препаратов, блокирующих EGFR. При колоректальном раке используется два — цетуксимаб и панитумумаб. Их назначение улучшает ответ опухоли на терапию цитостатиками и пролонгирует время до прогрессирования патологии.
Однако данное лечение не подходит пациентам с наличием мутации в генах KRAS, поскольку в этом случае синтезируется белок, являющийся промежуточным звеном в передаче молекулярного сигнала от EGFR к ядру клетки, поэтому блокада этого рецептора не имеет смысла, она неэффективна.
Еще одной мишенью для действия таргетной терапии является сосудистый фактор роста. Как известно, злокачественные опухоли обильно кровоснабжаются за счет активного роста кровеносных сосудов. Стимулирует этот процесс сосудистый фактор роста. Если блокировать его действие, опухоль лишится полноценного кровоснабжения и потеряет способность к гематогенному метастазированию. Препаратом, оказывающим такой эффект, является бевацизумаб.
Лучевая терапия при раке толстой кишки
Лучевая терапия при колоректальном раке имеет ограниченное применение и используется только в рамках химиолучевой терапии рака прямой кишки. В качестве паллиативного лечения она может применяться при наличии отдаленных метастазов.
Прогноз и выживаемость при карциноме толстой кишки
Прогноз при раке толстой кишки зависит от стадии заболевания, гистологического типа опухоли и возможности проведения радикального лечения. Наилучшие показатели пятилетней выживаемости у рака 1-2 стадии, у них она составляет 95 и 70% соответственно. При проведении радикального лечения 3 стадии, 5-летняя выживаемость достигает 50%, при невозможности его проведения пятилетний рубеж переживают только 10% больных.
Профилактика карциномы толстой кишки
Рак толстой кишки можно предотвратить. Снижают риск развития КРР следующие мероприятия:
- Сбалансированное питание с достаточным количеством в рационе пищевых волокон и клетчатки. Ими богаты овощи, фрукты, зерновые каши.
- Снижение употребления канцерогенных продуктов — животные жиры, жареные, копченые, маринованные блюда, фаст фуд и т. д.
- Достаточное употребление жидкости.
- Достаточная физическая активность.
Помимо этого, необходимо своевременное лечение заболеваний кишечника, в том числе удаление полипов.
Синдром Линча – наследственный неполипозный колоректальный рак

Кандидат медицинских наук. Член Ассоциации проктологов России. Научный сотрудник кафедры хирургических болезней. Стаж +7 лет. Принимает в Университетской клинике. Цена приема 2000 руб.
- Запись опубликована: 22.07.2020
- Время чтения: 1 mins read
Синдром Линча, также известный как синдром наследственного неполипозного колоректального рака (HNPCC), был впервые описан более 100 лет назад. Это наиболее распространенный из признанных наследственных синдромов рака толстой и прямой кишки.
Что представляет собой синдром Линча
Синдром Линча, который часто называют неполипозным кишечным раком – это наследственное заболевание, повышающее риск развития многих видов рака, особенно колоректального – рака толстой и прямой кишки.
Риск приобретения колоректального рака при плохой наследственности составляет от 20 до 80%. Кроме него, люди с синдромом Линча имеют риск развития следующих видов онкологических опухолей:
- желудка, от 1 до 13%;
- мочевыводящих путей – от 1 до 18%;
- гепатобилиарного тракта – печени и желчных протоков, от 1 до 4%;
- тонкой кишки – от 1 до 6%;
- поджелудочной железы – от 1 до 6%;
- головного мозга или ЦНС от 1 до 3%.
Кроме того, женщины с этим заболеванием имеют высокий риск развития рака яичников – от 1 до 38% и слизистой оболочки матки или эндометрия – от 15 до 60%. В целом, женщины с синдромом Линча имеют более высокий общий риск развития рака, чем мужчины с этим заболеванием, из-за этих видов злокачественных новообразований женской репродуктивной системы.
Люди с синдромом Линча обычно заболевают раком в возрасте сорока или пятидесяти лет, однако, риск присутствует в течение всей жизни – так называемый пожизненный риск. Средний возраст наиболее распространенных типов рака при синдроме Линча:
- колоректального – 44 года (у членов семей по амстердамским критериям);
- эндометрия – 46 лет.
Страдающие синдромом Линча иногда имеют доброкачественные опухоли в толстой кишке, называемые полипами. Причем они хоть и встречаются в более молодом возрасте, но не в большем количестве, чем в общей популяции.
Синдром Линча
Симптомы синдрома Линча
Многие больные с раком прямой или толстой кишки никаких симптомов на ранних стадиях заболевания не испытывают. Симптомы могут не появиться довольно долго, пока болезнь не перейдет в позднюю стадию. Только регулярное обследование, определение и понимание факторов риска поможет защититься от этой патологии, распознать ее на ранней стадии и оказать эффективную медицинскую помощь.
Симптомы рака толстой и рака прямой кишки похожи на проявления многих других заболеваний толстой кишки. Общие симптомы включают в себя следующее:
- кровь в кале;
- необъяснимая диарея;
- длительный период запора;
- спазмы в животе;
- уменьшение размера или калибра стула;
- вздутие живота, полнота, распирание;
- необъяснимая потеря веса;
- вялость и рвота.
Причины развития синдрома Линча
У людей с синдромом Линча обнаружены изменения в генах MLH1, MSH2, Msh6 и PMS2 или гене EPCAM. MLH1, MSH2, Msh6 и PMS2 гены участвуют в устранении ошибок, которые возникают, когда ДНК копируется в ходе подготовки к делению клеток – процессе, называемом репликацией ДНК.
Поскольку эти гены работают вместе, чтобы исправить ошибки ДНК, они известны как гены восстановления несоответствия (MMR). Мутации в любом из этих генов препятствуют правильному восстановлению ошибок репликации ДНК. Поскольку аномальные клетки продолжают делиться, накопленные ошибки могут привести к неконтролируемому росту клеток и, возможно, к злокачественной опухоли.
Более опасны мутации в гене MLH1 или MSH2, поскольку они имеют более высокий риск (от 70 до 80%) развития пожизненного рака, тогда как мутации в гене MSH6 или PMS2 имеют более низкий риск (от 25 до 60%).
Мутации в гене EPCAM также приводят к нарушению репарации ДНК, хотя сам ген не участвует в этом процессе. Ген EPCAM находится рядом с геном MSH2 в хромосоме 2, и некоторые мутации гена EPCAM приводят к выключению гена MSH2 (инактивации). В результате роль гена MSH2 в репарации ДНК нарушается, что может привести к накопленным ошибкам ДНК и развитию рака.
Хотя мутации в этих генах предрасполагают к раку, раковые опухоли развиваются не у всех людей с этими мутациями.
Симптомы неполипозного рака кишечника
Как наследуется синдром Линча
Риск рака при синдроме Линча наследуется по аутосомно-доминантному типу. Это означает, что одной наследственной копии измененного гена в каждой клетке достаточно, чтобы увеличить его развитие.
Важно отметить, что люди с мутацией имеют повышенный риск рака. Однако, он возникает не у всех людей, даже если они наследуют мутации в этих генах.
Шанс унаследовать эти мутации в 50% наблюдается:
- у детей родителей с данной мутацией;
- у братьев, сестер, родителей человека с этой мутацией.
Отрицательный тест, полученный при генетическом исследовании (мутация не обнаружена) снижает риск рака, но он остается выше средних показателей для этой группы, чем для популяции в целом.
Диагностика синдрома Линча
Ранняя диагностика имеет решающее значение для раннего выявления и лечения рака толстой и прямой кишки. График регулярных проверок зависит от истории семьи и истории болезни.
У лиц с риском синдрома Линча обычно существует семейный анамнез двух последовательных поколений колоректального рака. Или они имеют по крайней мере одно поколение с раком прямой кишки и одно поколение с полипами. Лица обоего пола в группе риска нуждаются в обязательном обследовании толстой кишки. Женщины также должны проходить ежегодные обследования эндометрия и яичников.
Диагноз синдрома Линча ставится при идентификации мутаций следующих генов: MLH1, MSH2, MSH6, PMS2 и EPCAM.
Для определения категории лиц, которые нуждаются в генетическом тестировании используются:
- Амстердамские критерии;
- пересмотренные руководящие принципы Bethesda .
Пересмотренные руководящие принципы Bethesda :
- Диагностированный колоректальный рак у лиц до 50 лет;
- Установленный рак эндометрия до 50 лет;
- Развивающийся рак (колоректальный, эндометрия или другого типа, ассоциированного с синдромом Линча*), обнаруженный при тестировании образца опухоли методами микросателлитного тестирования на нестабильность (MSI) и иммуногистохимическое тестирование (IHC). * Категория включает колоректальный рак , рак эндометрия , рак яичников , рак желудка , рак тонкой кишки , рак мочеточника или почечной лоханки , рак мочевого пузыря , рак желчных протоков , рак поджелудочной железы или аденомы сальных желез кожи ;
- Присутствующий синхронный. метахронный колоректальный рак или ассоциированный с синдромом у лиц любого возраста;
- Установленный колоректальный рак у 1 или более родственников первой линии * или другой тип ассоциированной с синдромом Линча злокачественной опухоли, которая развивается также до 50 лет. * Определение “ родственники первой степени ” включает родителей , братьев и сестер , а также детей .
- Колоректальный рак у 2 и более родственников первой или второй линии с другим раком , связанным с синдромом Линча *. *Определение “ Родственники второй степени ” включают теть , дядь , бабушек и дедушек , внуков , племянников и племянниц .
Определение синдрома Линча все еще развивается . У многих людей может быть синдром Линча, даже если они и члены их семьи не попадают под критерии и руководящие принципы для генетической диагностики.
Окончательное решение о необходимости объема и характера исследований принадлежит специалистам.
Диагностические процедуры для синдрома Линча включают в себя целый ряд исследований.
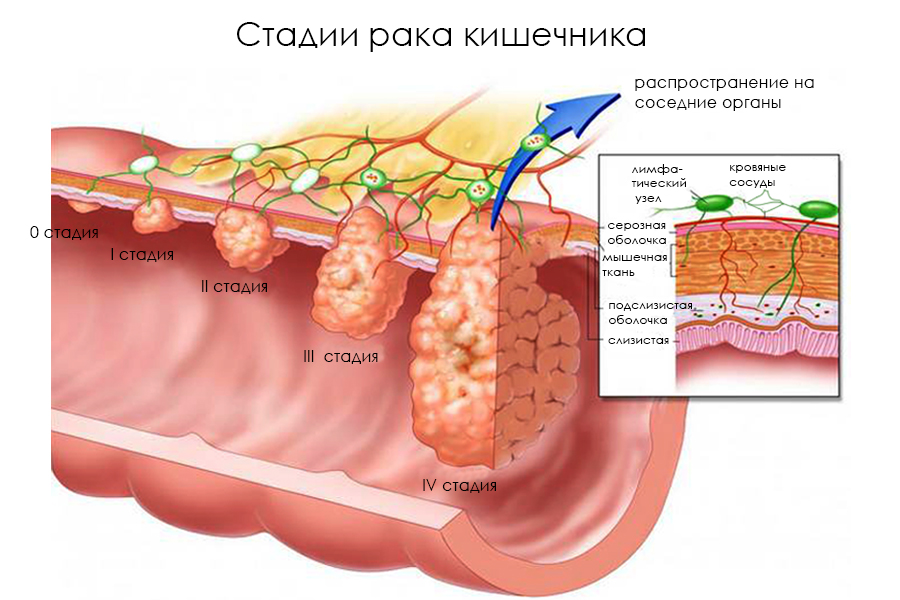
Рак кишечника – стадии развития
Генетическое тестирование
Мутации или изменения в одном из пяти различных генов ответственны за большинство случаев синдрома Линча. Если у человека есть семейный анамнез синдрома Линча, ему рекомендуется пройти генетический тест, чтобы определить, есть ли конкретно у него риск развития рака.
Генетический тест выполняется путем исследования образца крови. Если тест подтверждает, что есть мутация гена, пациент должен выполнять ежегодные колоноскопии и регулярно проходить скрининг. Если мутации не обнаружено, но семейная история присутствует, объем исследований определяется проктологом-онкологом, поскольку мутации идентифицируются не всегда, и риск рака остается выше среднего.
Скрининговое тестирование
Микросателлитное тестирование на нестабильность (MSI) и иммуногистохимическое тестирование (IHC) используются в качестве скринингового теста. Они нужны для определения вероятности того, что рак вызван одним из генов синдрома Линча.
Исследуется опухолевая ткань. От результатов этих исследований зависит, следует ли рассматривать более конкретное генетическое тестирование. Если получены положительные результаты, выполняется генетическое исследование на мутации.
Колоноскопия
Колоноскопия является предпочтительным методом для диагностики многих проктологических заболеваний. Это лучший способ обнаружить полипы или рак, с помощью которого проктолог осматривает весь толстый кишечник и проводит забор образца ткани для дальнейшего исследования.
Лечение синдрома Линча
Цель лечения синдрома Линча – удаление полипов и любых раковых образований. Объем и тип хирургического вмешательства зависит от результатов обследования и подбирается индивидуально. Иногда достаточно удаления полипов с помощью эндоскопии. В других случаях рекомендуется более масштабная операция.
Хирургические варианты лечения синдрома Линча включают в себя следующее:
Тотальная проктоколэктомия с илеостомой Брука
Во время этой процедуры вся толстая кишка и прямая кишка удаляются. Хирург выполнит илеостому, которая выводит тонкую кишку через брюшную стенку. Эта процедура обычно необходима, когда происходит следующее:
- Инвазивный рак встречается в прямой кишке.
- Анальный сфинктер не функционирует.
- Сфинктерная мышца слабая.
Илеостома может быть временной или постоянной.
Колэктомия с илеоректостомией
Во время этой процедуры хирург удаляет толстую кишку, но сохраняет всю или большую часть прямой кишки. Затем прикрепляет тонкую кишку к верхней части прямой кишки. Это менее сложная операция, чем полная проктоколэктомия, и она предназначена для сохранения функции кишечника. Однако, поскольку прямая кишка не удалена, могут развиться полипы и рак.
Восстановительная проктоколэктомия
Во время этой процедуры удаляется вся толстая кишка и большая часть прямой. Подвздошная кишка (конец тонкой кишки) прикрепляется к прямой кишке с созданием “резервуара”. Проводится в два этапа.
Преимущество этой процедуры заключается в том, что поддерживается проходимость и протяжение кишечника, при этом врач удаляет всю подверженную риску слизистую оболочку толстой кишки.
Общие рекомендации по скринингу и снижению риска при синдроме Линча
Американское общество клинической онкологии ASCO рекомендует следующий скрининг для людей с синдромом Линча. Важно обсудить эти варианты с проктологом, так как патологии у каждого пациента индивидуальны:
- Колоноскопия проводится каждые 1-2 года, начиная с возраста от 20 до 25 лет, или на 5 лет моложе самого раннего возраста при постановке диагноза в семье, в зависимости от того, что наступит раньше.
- ФГДС каждые 3-5 лет, в дополнение к тестированию на инфекцию Helicobacter pylori на базовом обследовании с лечением, если результат положительный.
- Ежегодный общий осмотр кожи тела на опухоли.
- Назначение ежедневного приема аспирина, по результатам исследований. Аспирин снижает риск КРР и, возможно, других видов злокачественных опухолей при синдроме Линча.
Скрининг для женщин (в дополнение к вышеперечисленному):
- Ежегодное обследование малого таза: УЗИ малого таза, биопсия эндометрия в возрасте после 30 лет.
- Женщинам, которые больше не планируют рождение детей, предлагается рассмотреть возможность проведения профилактической операции – удаления матки и яичников .
Скрининговые методы на злокачественные опухоли репродуктивной системы у женщин с синдромом Линча высокую эффективность пока не доказали.
Варианты ежегодных скрининговых (профилактических) осмотров меняются с течением времени по мере развития новых технологий и получения новых знаний о синдроме Линча и других его формах.
Наследственная неполипозная колоректальная карцинома ( Наследственный неполипозный колоректальный рак )
Наследственная неполипозная колоректальная карцинома – это наследственно обусловленная форма колоректального рака. Передается по аутосомно-доминантному типу. Чаще поражает проксимальные отделы толстого кишечника. Возможно одновременное или практически одновременное развитие нескольких злокачественных опухолей. Проявляется болями, нарушениями стула и явлениями кишечной непроходимости. Диагноз устанавливается на основании семейного анамнеза, клинической симптоматики и данных дополнительных исследований (колоноскопии, биопсии, генетических тестов). Лечение оперативное – радикальное или паллиативное.
МКБ-10
Общие сведения
Наследственная неполипозная колоректальная карцинома (ННКРК) – злокачественная опухоль толстой кишки, обусловленная наследственной мутацией. Составляет от 3 до 8% случаев колоректального рака. Относится к наследственным формам рака. Риск развития болезни в течение жизни при установленной мутации – около 80%. Злокачественная опухоль толстого кишечника нередко возникает в возрасте до 50 лет, то есть, на 10-15 лет раньше, чем в среднем по популяции. У пациентов с наследственной неполипозной колоректальной карциномой также отмечается повышенная вероятность развития рака яичников, рака эндометрия, рака тонкого кишечника, рака желудка, рака почек и рака поджелудочной железы. Суммарный риск развития злокачественных опухолей в течение жизни составляет более 90%. Лечение осуществляют специалисты в сфере клинической онкологии, проктологии и абдоминальной хирургии.

Причины развития ННКРК
Причиной развития данной патологии обычно являются мутации генов репарации неспаренных оснований ДНК. В норме репарация позволяет многократно уменьшить ошибки синтеза ДНК. Комплекс белков, отвечающих за репарацию, удаляет ошибочные участки дезоксирибонуклеиновой кислоты, а затем «восстанавливает пробелы». При мутации генов, отвечающих за этот процесс, возникают многочисленные некорректируемые ошибки ДНК. Клетки становятся менее стабильными.
Наличие подобных мутаций подтверждается при проведении генетических исследований. Вместе с тем, существуют клинические критерии, позволяющие обоснованно заподозрить наличие наследственной неполипозной колоректальной карциномы. Вероятность развития наследственного колоректального рака при выявлении данных критериев может варьировать из-за различия генетических поломок и разного уровня нестабильности клеток. К числу критериев относят:
- Наличие трех и более близких родственников с колоректальным раком, подтвержденным в ходе гистологического исследования. Один из трех родственников должен иметь первую степень родства с двумя другими. Наряду с колоректальным раком, учитывается наличие рака почки, тонкого кишечника и других органов, поражающихся при ННКРК.
- Развитие заболевания у представителей двух поколений.
- Хотя бы одно из новообразований было обнаружено у больного, не достигшего возраста 50 лет.
Для более точного прогнозирования специалисты-онкологи выделяют три группы пациентов с учетом склонности к развитию наследственной неполипозной колоректальной карциномы: группу низкого, среднего и высокого риска. В группу низкого риска входит большинство представителей популяции. У членов этой группы рак толстого кишечника в семейном анамнезе отсутствует либо выявляется у родственников не первой степени родства или у родственников первой степени родства в возрасте старше 45 лет. В группе среднего риска находятся больные, имеющие одного родственника первой степени родства, заболевшего колоректальным раком в возрасте младше 45 лет, либо двух родственников первой степени родства, заболевших в любом возрасте.
Группа высокого риска включает в себя членов семьи пациента с установленной наследственной неполипозной колоректальной карциномой и различными полипозными синдромами. Кроме того, в эту группу входят больные, у которых в семейном анамнезе выявляется три и более случаев рака толстого кишечника в пределах материнской или отцовской линии (у родителя, дедушки, бабушки, тети, дяди, сестры, брата, племянника и племянницы) либо два и более случаев рака толстого кишечника в пределах одной линии при условии, что хотя бы у одного родственника рак был множественным либо был диагностирован в возрасте до 45 лет.
Вероятность появления детей, страдающих наследственной неполипозной колоректальной карциномой при подтвержденном заболевании у одного из родителей, составляет 50%. Генетические исследования в период внутриутробного развития ребенка возможны, но на практике такую диагностику осуществляют очень редко из-за ее низкой практической значимости. Имеющаяся мутация может никак не проявиться в течение жизни (неполная пенетрантность гена) либо проявляться с различной степенью тяжести и в разном возрасте (вариабельная экспрессивность гена), поэтому оценить последствия наличия такого гена для ребенка заранее невозможно.
Симптомы ННКРК
Клиническая симптоматика соответствует классическому колоректальному раку. Отличительными особенностями являются более молодой возраст пациентов и преимущественное поражение проксимальных отделов толстого кишечника. Из-за высокого расположения наследственной неполипозной колоректальной карциномы кровь в кале визуально обычно не определяется, при значительной кровопотере возможен темный стул, при повторяющихся кровотечениях – анемия, проявляющаяся слабостью, головокружениями, бледностью кожных покровов и изменениями в анализе периферической крови.
При наследственной неполипозной колоректальной карциноме могут возникать явления кишечной непроходимости. Вначале кишечная непроходимость частичная, проявляется метеоризмом, задержкой стула и резкими схваткообразными болями, повторяющимися через 10-15 минут. При дальнейшем росте опухоли могут наблюдаться состояния, требующие экстренного хирургического вмешательства. Карциномы достаточно большого размера удается выявить при пальпации живота. При прогрессировании заболевания обнаруживаются общие признаки онкологического поражения: снижение аппетита, потеря веса вплоть до кахексии, слабость, гипертермия и т. д.
Диагностика
При постановке диагноза учитывается семейный анамнез, клинические проявления и данные дополнительных исследований. Больных направляют на колоноскопию, в процессе исследования осуществляют эндоскопическую биопсию опухолевой ткани. При подозрении на наличие наследственной неполипозной колоректальной карциномы наряду со стандартным морфологическим изучением материала выполняют исследование на микросателлитную изменчивость. При высоком уровне микросателлитной изменчивости проводят специальные генетические тесты.
Больным с наследственной неполипозной колоректальной карциномой назначают анализ кала на скрытую кровь, анализ периферической крови для выявления анемии и биохимический анализ крови для оценки функций печени. Для обнаружения метастазов и первичных опухолей другой локализации, возникающих при данной патологии, больных направляют на комплексное обследование, которое включает в себя гастроскопию, УЗИ органов малого таза, цитологическое исследование аспирата эндометрия, УЗИ брюшной полости, УЗИ забрюшинного пространства, рентгенографию грудной клетки, сцинтиграфию всего скелета и другие исследования.
Лечение ННКРК
Лечение хирургическое. С учетом высокого риска развития новых опухолей обычно осуществляют субтотальное удаление толстого кишечника с созданием илеоректального анастомоза. При вовлечении лимфатических узлов выполняют лимфаденэктомию. При наличии отдаленных метастазов проводят паллиативные оперативные вмешательства, направленные на устранение явлений кишечной непроходимости. Прогноз более благоприятный по сравнению с ненаследственными формами колоректального рака.
Прогноз и профилактика
Профилактика развития наследственной неполипозной колоректальной карциномы включает в себя регулярные обследования. Ближайшим родственникам пациентов с уже диагностированной ННКРК рекомендуют раз в два года проводить колоноскопию после 20 лет и раз в год – после 40 лет. Кроме того, им следует регулярно сдавать анализы мочи, а при появлении патологических изменений проходить обследование для исключения опухолей почек и мочеточников. Женщинам необходимо ежегодно обследоваться у гинеколога для исключения рака яичников и рака эндометрия. В некоторых случаях показана профилактическая пангистерэктомия. Дальним родственникам больных наследственной неполипозной колоректальной карциномой советуют провести генетическое исследование.
Тактика ведения пациентов с колоректальным раком
Колоректальный рак – злокачественная опухоль толстого кишечника. Новообразование может локализоваться в ободочной, сигмовидной или прямой кишке. По распространённости колоректальный рак занимает второе место после рака лёгких среди всех локализаций злокачественных опухолей.
Для ранней диагностики заболевания онкологи Юсуповской больницы применяют все современные диагностические методы, проводят тест на колоректальный рак. NADAL тест на комплекс гемоглобин-гаптоглобин (тест-кассета) является визуальным иммуноферментным двойным экспресс-тестом для качественного обнаружения гемоглобина человека и комплекса гемоглобин-гаптоглобин в пробах кала.
Врачи клиники онкологии проводят мультидисциплинарное лечение колоректального рака:
Выполняют радикальные и паллиативные оперативные вмешательства;
Назначают эффективнейшие противоопухолевые препараты, которые обладают минимальным спектром побочных эффектов;
Проводят лучевую терапию с помощью новейших радиотерапевтических установок ведущих мировых производителей.
Медицинский персонал осуществляет профессиональный уход за пациентами после операции. В случае формирования стомы проводят гигиенический уход за противоестественным анусом, обучают пациентов и их родственников правильно пользоваться калоприёмником. Пациенты в терминальной стадии колоректального рака получают паллиативную медицинскую помощь.

По механизму развития различают наследственный семейный неполипозный, наследственный при семейном аденоматозе и спорадический (ненаследственный) колоректальный рак. По характеру роста разграничивают экзофитную, эндофитную и смешанную (блюдцеобразную) форму рака толстого кишечника, которая характеризуется сочетанием двух предыдущих форм.
Экзофитный колоректальный рак растёт преимущественно в просвет толстого кишечника. Он представляет собой легкоранимую опухоль, имеющую значительные размеры. Часто осложняется кровотечением, но редко перекрывает просвет кишки. Локализуется преимущественно в правых, более широких отделах толстого кишечника.
Эндофитный колоректальный рак распространяется в основном в толще стенки кишки. Опухоль сравнительно быстро вызывает сужение её просвета и задержку каловых масс. Располагается преимущественно в левых, более узких отделах толстого кишечника.
По гистологической структуре различают аденогенный и плоскоклеточный рак толстого кишечника. Аденогенная злокачественная опухоль представляет собой аденокарциному высокой, средней или низкой степени дифференцировки. Чем ниже дифференцировка, тем агрессивнее раковый процесс. Особенной агрессивностью отличаются следующие гистологические типы колоректального рака:
Колоректальный рак гематогенным путём метастазирует в печень, лимфогенным – в яичники, лёгкое и по брюшине. По количеству выделяют одиночные и первично-множественные карциномы толстого кишечника.
Современная классификация, предложенная Международным противораковым союзом для определения стадии колоректального рака, включает обозначение распространения опухолевого процесса буквами (Т – tumor, опухоль, N – nodus, узел, M – metastasis, метастазы).
Онкологи Юсуповской больницы используют следующую характеристику колоректального рака:
Tis (рак на месте – эпителиальное новообразование или опухоль с инвазией в слизистую оболочку;
Т1 – новообразование инфильтрирует стенку кишки до подслизистого слоя и занимает менее половины её окружности;
Т2 – опухоль инфильтрирует мышечный слой и занимает более половины окружности кишки;
Т3 – новообразование инфильтрирует все слои кишечной стенки;
Тх – опухоль прорастает висцеральную брюшину или распространяется на соседние ткани и органы.
N0 характеризуется отсутствием метастазов в регионарных лимфоузлах. N1 свидетельствует о наличии метастазов в лимфоузлы первого порядка. При стадии N2 метастазы выявляют в лимфоузлах первого и второго порядка. Обозначение Nх используют в том случае, когда нет достаточных данных для подтверждения наличия регионарных метастазов в лимфоузлы.
В зависимости от наличия и распространения метастазов выделяют следующие варианты течения колоректального рака:
М0 – нет отдаленных метастазов;
M1 – имеются отдаленные метастазы;
Мх – недостаточно данных для установления отдалённых метастазов.
Колоректальный рак часто поражает печёночный и селезёночный изгибы толстой кишки или ректосигмоидный угол, где наблюдается задержка каловых масс.
Причины и механизмы развития заболевания
Колоректальный рак занимает лидирующие позиции по заболеваемости и смертности от злокачественных опухолей в России. Развитие молекулярной биологии привело к расшифровке механизмов образования и прогрессирования опухоли. Данные процессы требуют аккумуляции генетических и эпигенетических изменений в опухолевой клетке. Происходит накоплением мутаций в генах, которые контролируют рост и дифференцировку эпителиальных клеток. Это приводит к их генетической нестабильности.
Один из вариантов генетических изменений – микросателлитная нестабильность при колоректальном раке. Она характеризуется нарушением механизма репарации (особой функции клеток, заключающейся в способности исправлять химические повреждения и разрывы неспаренных оснований ДНК). Это приводит к тому, что мутации в геноме клетки накапливаются с большей скоростью, чем в нормальном состоянии.
При семейном аденоматозном полипозе возникают мутации генов, которые повреждают ДНК клеток с образованием микросателлитов. У больных с наследственными формами колоректального рака установлено наличие генных дефектов в различных хромосомах. При наследственных формах заболевания выявлены структурные изменения нуклеотидов. При спорадическом (ненаследственном) колоректальном раке наследственная предрасположенность является причиной заболевания у 18% пациентов.
Возможен непосредственный переход нормальной клетки к аденокарциноме. Чаще этот процесс развивается последовательно: сначала снижается дифференцировка колоноцитов, затем формируются доброкачественные новообразования (аденоматозные, аденопапилломатозные), потом они перерождаются в раковую опухоль.
В развитии колоректального рака определённую роль играют экзогенные и эндогенные факторы, в том числе нутритивные, функциональные нарушения толстого кишечника (хронический запор). К нутритивным факторам риска развития колоректального рака относят:
Употребления большого количества красного мяса (говядины, свинины, баранины);
Избыток в рационе пищевых жиров;
Преобладание рафинированных продуктов, лишённых растительной клетчатки;
Систематическое употребление алкоголя.
Важный фактор риска развития колоректального рака – хронические идиопатические воспалительные заболевания толстой кишки: гранулематозный и язвенный колит. Определённую роль играет дисбиоз толстого кишечника высоких степеней. Аденоматозные полипы почти неизбежно трансформируются в колоректальный рак. Малигнизация возникает в разное время в течение 13–15 лет. Причиной спорадического колоректального рака могут быть нарушения в клетках желудочно-кишечного тракта, способных к выработке и накоплению биогенных аминов и пептидных гормонов.
Симптомы
Поздняя диагностика колоректального рака связана со значительным интервалом между началом заболевания и его симптомами. Первыми признаками колоректального рака являются:
Примесь крови в кале;
Задержка опорожнения кишечника.
Колоректальный рак в дальнейшем проявляется следующими симптомами:
Диспепсическими – тошнотой, рвотой, потерей аппетита, чувством вздутия и тяжести в эпигастральной области, болью в животе;
Энтероколитическим – вздутием живота, урчанием, болью в области заднего прохода, в животе, усиливающейся перед дефекацией;
Токсико-анемической – признаками малокровия (бледностью кожных покровов, быстрой утомляемостью, постоянной слабостью) и повышением температуры тела.
Большое значение для появления признаков заболевания имеет место локализации опухоли. Расположенные в более широких отделах толстой кишки новообразования длительное время протекают бессимптомно. При расположении новообразования в узком отделе кишечника (левой части толстой кишки) первые симптомы появляются рано, так как растущая опухоль вызывает частичную или полную непроходимость кишечника. При развитии злокачественной опухоли в прямой кишке или нижнем отделе толстого кишечника появляются прожилки крови в кале, боль в животе, усиливающаяся перед дефекацией, а также во время стула.
Даже при наличии этих симптомов 50% пациентов обращаются за медицинской помощью только спустя 6 месяцев, а 22% – через год. Только в 37% случаев врачи общей практики устанавливают правильный диагноз во время обращения. Онкологи Юсуповской больницы начинают проводить комплексное обследование пациентов на предмет наличия колоректального рака при наличии следующих симптомов заболевания:
Задержки эвакуаторной функции толстого кишечника (хронического запора);
Признаков кишечного кровотечения или скрытой крови в кале;
Тенезмов (ложных позывов на дефекацию).
Боли в животе – поздний симптом колоректального рака у женщин и мужчин. Болевой синдром развивается в случае перифокального воспалительного процесса, кишечной непроходимости или прорастании раковой опухоли в соседние ткани. Новообразование иногда можно прощупать через брюшные покровы или при пальцевом исследовании прямой кишки. Вследствие скрытых или явных кишечных кровотечений развиваются признаки анемии:
Бледность кожных покровов;
Ломкость ногтей и волос;
Уменьшение количества эритроцитов в периферической крови;
Снижение уровня гемоглобина.
При канцероматозе и наличии отдалённых метастазов отмечается резкое снижение массы тела, похудение. При частичной кишечной непроходимости и выраженной интоксикации появляются следующие симптомы:
Отвращение к пище;
Тошнота и рвота;
Чувство тяжести и переполнения;
Упорные запоры, изредка сменяющиеся поносами;
Если колоректальный рак поражает сигмовидную ободочную и прямую кишку, в кале обнаруживают примесь крови, иногда слизь и гной. При акте дефекации у пациентов появляется ощущение наличия инородного тела, неполного опорожнения прямой кишки.
При объективном обследовании на поздних стадиях колоректального рака онкологи выявляют бледность кожных покровов и видимых слизистых оболочек, увеличение объёма живота. При прощупывании отрезков толстого кишечника определяется опухолевое образование. Если имеют место метастазы в печень, она увеличивается в размерах, становится плотной, бугристой. Увеличиваются паховые лимфатические узлы.
Диагностика
Пальцевое исследование прямой кишки в коленно-локтевом положении пациента в 25% случаев позволяет прощупать опухоль в дистальных отделах кишки. Она имеет вид плотного образования, которое суживает просвет кишки. Врач определяет протяжённость поражения, подвижность или неподвижность опухоли, состояние тазовых лимфатических узлов и клетчатки таза. Может обнаружить кровь на перчатке. При прогрессирующем сужении кишки появляется приступообразная боль в брюшной полости, симптомы частичной обтурационной кишечной непроходимости.
Помимо клинического обследования, онкологи Юсуповской больницы в диагностике колоректального рака используют различные лабораторные и инструментальные методы. Ранний диагноз (в стадии Tis и T1N0M0) может быть установлен у 2–3% бессимптомных больных только во время случайной ректороманоскопии. С помощью теста на скрытую (оккультную) кровь в кале проводят скрининг колоректального рака. Чтобы подготовиться к исследованию, пациенту рекомендуют исключить из пищевого рациона продукты, содержащие пероксидазу (мясо, редис, турнепс), препараты железа и аскорбиновую кислоту. Кал в течение трёх дней собирают в специальную коробку.
Второй метод скрининга колоректального рака – иммунохимический тест на скрытую кровь в кале. Исследование проводят методом гемагглютинации с утилизированными антителами к глобину человеческого гемоглобина. Метод не реагирует на присутствие нечеловеческой пероксидазы. Она содержится в овощах и фруктах. Перед сбором биологического материала пациенту не нужно соблюдать диету. Это упрощает исследование.
Применяются и другие лабораторные методы диагностики колоректального рака:
Определение темпа клеточной пролиферации путем изучения некоторых ядерных белков;
Определение фекального кальпротектина;
Иммунологический тест с определением раково-эмбрионального (онкофетального) антигена (РЭА) и онкомаркера СА19–9.
В диагностике колоректального рака онкологи Юсуповской больницы используют следующие инструментальные методы:
Гибкую (на волоконной оптике) и жёсткую ректороманоскопию, позволяющую обнаружить опухоль в нижних отделах толстого кишечника, установить её расположение, протяженность, характер роста, сделать прицельную биопсию для гистологического исследования (вместо биоптата можно взять с поверхности опухоли мазки-отпечатки с помощью поролонового тампона для цитологического изучения на предметном стекле);
Колонофиброскопию – выполняется однократно с временным промежутком в 5 лет, сочетается с прицельной биопсией;
Виртуальную колоноскопию – предполагает проведение компьютерной томографии с анализом трансформированного изображения, напоминающего таковое, полученное оптическим колоноскопом;
Трансабдоминальную и эндоскопическую ультрасонографию – неинвазивный метод, с помощью которого выявляют наличие объёмного образования в брюшной полости, метастазы в лимфоузлах и печени, распространение опухоли в окружающие органы;
Компьютерную томографию – позволяет уточнить степень инвазии опухоли, наличие метастазов в печень и регионарные лимфоузлы;
Ирригоскопию и ирригографию – позволяют определить локализацию и протяжённость ракового поражения, распад опухоли, прорастание в соседние органы, наличие осложнений (свищей, абсцессов, кишечной непроходимости, перфорации).
Для диагностики колоректального рака используют двойное контрастирование и многопроекционное рентгенологическое исследование.
Лечение
Онкологи проводят комплексное лечение колоректального рака: оперативные вмешательства, лучевую и химиотерапию. Часто их комбинируют друг с другом для достижения большего эффекта. Хирурги-онкологи Юсуповской больницы виртуозно владеют техникой выполнения всех известных сегодня оперативных вмешательств, которые проводятся по поводу колоректального рака. Радикальная операция заключается в удалении первичной опухоли с лимфатическими узлами. Суть оперативного вмешательства заключается в резекции пораженного сегмента толстой кишки (новообразования, брыжейки и вовлечённых в опухолевый процесс тканей или органа). Чтобы избежать осложнений, проводят тщательную предоперационную подготовку.
Хирурги индивидуально выбирают вид операции каждому пациенту:
Левостороннюю или правостороннюю гемиколэктомию с наложением трансверзоректального анастомоза;
Субтотальную резекцию ободочной кишки;
Сигмоидэктомию с десцендоректальным анастомозом.
При раке прямой кишки проводят брюшно-промежностную экстирпацию, осуществляют меры по созданию искусственного запирательного аппарата из гладкомышечного лоскута стенки низведенной кишки в области промежностной колостомы или производят брюшно-анальную резекцию кишки и формируют колоанальный анастомоз.
При II–III стадиях колоректального рака хирургическое лечение сочетают с адъювантной химиотерапией и лучевой терапией. Они снижают риск рецидива и развития опухолей другой локализации. Для подавления роста опухоли используют 5-фторурацил внутривенно, внутриартериально и ректально, лейковорин. Для уменьшения их токсического действия пациентам назначают интерферон-а2a. В качестве химиотерапевтических препаратов второго ряда применяют кселоду, томудекс, элоксатин. Химиотерапию сочетают с приёмом фолиевой кислоты и иммуномодуляторов.
Колоректальный рак достаточно устойчив к действию цитостатиков. Относительно хорошую противоопухолевую активность в отношении него проявляют препараты иринотекан, оксалиплатин, ралтитрексид и капецитабин. Их комбинации действуют эффективнее и увеличивают шансы пациентов на продление жизни.
При раке ободочной кишки с метастазами в регионарные лимфоузлы после операции для предотвращения рецидивов назначают адъювантную химиотерапию (стандартная схема — фторурацил и лейковарин). Еще лучше будут результаты, если сочетать химиотерапию с лучевой терапией. При метастазах колоректального рака в другие органы (печень, легкие) химиотерапия носит паллиативный характер, лишь облегчая состояние пациента.
Таргетная терапия – целенаправленная атака на патологические очаги с минимальным повреждением живых тканей и органов, которые находятся рядом с новообразованием. Благодаря специальному молекулярному тесту врачи определяют тип мутации клеток. Под него подбирают определённый биологический препарат. Он будет «целиться» только в мутировавшие клетки и не затронет здоровые. Такой метод позволяет остановить развитие колоректального рака.
По стандартам лечения колоректального рака перед операцией проводится короткий курс лучевой терапии. При этом могут быть использованы наружный и внутренний (брахитерапия) способы облучения опухоли.
Результаты лечения колоректального рака во многом определяются стадией, на которой начато лечение, и комбинацией доступных методов лечения. Сочетание хирургической операции с лучевой терапией при раке прямой кишки снижает риск рецидивов в 2 раза и увеличивает 5-летнюю выживаемость пациентов на 20%.
Для того чтобы пройти диагностику при подозрении на колоректальный рак, записывайтесь на приём к онкологу, позвонив по номеру телефона Юсуповской больницы. При выявлении опухоли врачи клиники онкологии выполнят операцию, проведут адекватную терапию инновационными методами. Ранняя диагностика колоректального рака увеличивает шансы на выздоровление.
X Международная студенческая научная конференция Студенческий научный форум – 2018

Онкология кишечника занимает 3 место в мире по сложности диагностики и лечения. Наследственный неполипозный рак кишечника(ННРК)является одним из наиболее часто встречающихся новообразований у человека. По крайней мере, у 50% индивидуумов в западных популяциях к 70 годам развиваются колоректальные опухоли, и приблизительно у 10% из них, в конечном счете, развивается колоректальный рак. Наследственный неполипозный рак кишечника встречается с частотой 2-5 на 1000, что составляет приблизительно 3-8% колоректального рака.
Цель: изучить проблему наследственно неполипозного рака кишечника
Изучить причины возникновения ННРК. Описать риск наследования, клинические признаки. Методы диагностики. Особенности ННРК. Первые признаки.
Наследственный неполипозный рак кишечника (ННРК) (MIM №120435) — генетически разнородный аутосомно-доминантный синдром предрасположенности к раку, часто вызывается мутациями в генах репарации неспаренных оснований ДНК. Наследственный неполипозный рак кишечника (ННРК) встречается с частотой 2-5 на 1000, что составляет приблизительно 3-8% колоректального рака.
Патогенез наследственного неполипозного рака кишечника.
При большинстве колоректальных опухолей, включая САП, кариотип опухоли прогрессивно становится все более анеуплоидным. Приблизительно 13-15% колоректальных опухолей не имеет такой хромосомной нестабильности, но имеет инсерцию или делецию в повторяющихся последовательностях (микросателлитная нестабильность). Микросателлитную нестабильность обнаруживают в 85-90% опухолей при наследственном неполипозном раке кишечника. В соответствии с этим наблюдением, приблизительно 70% семей наследственным неполипозным раком кишечника с карциномами, имеющими микросателлитную нестабильность, наследуют мутации в одном из шести генов репарации неспаренных оснований ДНК: MSH2, MSH6, MLH1, MLH3, PMS1 или PMS2. Репарация ДНК в неспаренных основаниях уменьшает ошибки репликации в 1000 раз. Ошибки синтеза ДНК вызывают неправильное спаривание нитей и деформируют двойную спираль ДНК. Комплекс белков репарации организует разные ферменты для восстановления повреждений. Используя вырезание длинных участков, этот комплекс удаляет ошибочный фрагмент вновь синтезированной нити ДНК и затем вновь синтезирует его. Чтобы вызывать микросателлитную нестабильность, должны потерять свою функцию оба аллеля гена репарации ДНК. Высокая частота соматической утраты функции второго аллеля приводит к тому, что наследственный неполипозный рак кишечника наследуется как аутосомно-доминантная болезнь приблизительно с 80% пенетрантностью. Соматическая утрата функции может происходить за счет потери гетерозиготности, внутригенных мутаций или гиперметилирования. При наследственном неполипозном раке кишечника количество мутантных микросателлитных локусов нарастает по мере перехода из аденомы в карциному. Инактивация генов, содержащих микросателлитные последовательности, может играть ключевую роль в развитии рака. Например, микросателлитная нестабильность порождает мутации типа сдвига рамки в гене рецептора фактора роста II (TGFBR2). Мутации в гене TGFBR2 приводят к утрате экспрессии белка TGF(3RII, и, поскольку система TGFP тормозит рост эпителиальных клеток толстого кишечника, переходу к неуправляемому росту. В поддержание концепции о роли гена TGFBR2 при наследственном неполипозном раке кишечника описана одна семья без мутаций в генах репарации ДНК, но с наследуемой мутацией в гене TGFBR2. Мутации гена TGFBR2 встречаются на ранних этапах наследственного неполипозного рака кишечника и могут содействовать росту аденом.
Фенотип и развитие наследственного неполипозного рака кишечника.
Хотя у больных ННРК число полипов аналогично общей популяции, они развиваются в более молодом возрасте. Средний возраст установки диагноза колоректальной аденокарциномы меньше 50 лет, т.е. на 10-15 лет раньше, чем в общей популяции. Больные наследственным неполипозным раком кишечника (ННРК) и известной унаследованной мутацией имеют 80% риск развития колоректальной опухоли в течение всей жизни. От 60 до 70% аденом и карцином при наследственном неполипозном раке кишечника (ННРК) развивается между селезеночным углом и илеоцекальным соединением, в то время как большинство спорадических колоректальных опухолей (а также опухоли при САП) развиваются в нисходящем отделе толстой кишки и сигмовидной кишке. Карциномы при ННРК реже имеют хромосомную нестабильность и ведут себя менее активно, чем спорадический рак кишечника; спорадические опухоли и карциномы при САП часто могут быть анеуплоидными и более энергичными. По этой причине больные наследственным неполипозным раком кишечника (ННРК) имеют лучший прогноз (с учетом стадии и возраста), чем больные с САП или колоректальными опухолями с хромосомной нестабильностью. Помимо колоректального рака, при наследственном неполипозном раке кишечника (ННРК) возможны и другие опухоли, включая рак желудка, тонкого кишечника, поджелудочной железы, почек, эндометрия и яичников; опухоли легкого и молочной железы с наследственным неполипозным раком кишечника (ННРК) не связаны. Пациенты с наследственным неполипозным раком кишечника (ННРК) и известной унаследованной мутацией в течение жизни имеют более 90% риска развития колоректального рака или одной из таких опухолей. Особенности фенотипических проявлений наследственного неполипозного рака кишечника: • Возраст начала: средний • Колоректальный рак • Многочисленные первичные опухоли
Особенности и опасность неполипозного рака толстой кишки
НРТК является наследственным заболеванием. Недуг может возникнуть по причине семейного рака (синдром Линча), или наследованием аденоматозных полипов.
В исследовании болезни очень важно иметь информацию о предшественниках раковых клеток, которые передались больному. Но, бывает так, что пациент не знает своих родственников, а тем более болезней, которым они подвергались. По этой причине – достоверно определить степень опасности и риск данной онкологии не представляется возможным.
Причины заболевания и кто в группе риска?
Основной причиной возникновения ННРТК является мутация гена, отвечающего за процессы в молекулах ДНК. Микросателлитная неустойчивость, которая происходит в молекулах, быстро накапливается в геноме клетки. Ученые называют это явление «генетическим мусором» или «раковым геном». Скорость его накопления у больного достаточно высока, по сравнению со здоровым пациентом. Рак может сформироваться в разных отделах кишечника, в зависимости от вида мутации.
Риск развития заболевания у пациентов с наследственной предрасположенностью составляет 50%. Также, у таких людей, зачастую отсутствуют полипы в кишечнике, поэтому онкология развивается очень быстро. Существуют семьи, которые подвергаются опасности с поколения в поколение.
В большинстве случаев, ННРТК поражает людей с доминантным геном в возрасте до 60 лет. Для женщин риск составляет 91%, а для мужчин – 69%. Для синдрома Линча или ННРТК характерны следующие признаки:
Проявление заболевания у родственников в возрасте до 60 лет, в 2 – 3 поколениях.
Незрелый возраст проявления болезни у обоих родственников, в 2 поколениях.
Два случая любого вида онкологии у двух родственников в 2 – 3 поколениях. При этом, хоть один случай должен быть раком яичников, почечной лоханки, желудка, уретры или кишечника. В этом случае учитывается рак в возрасте только до 50 лет.
Случаи недуга у самых близких (отца и матери) в возрасте до 50 лет.
Диагностирование опухолей в 2 поколениях (до 50 лет).
Хотя-бы один родственник первой степени родства с диагнозом данной болезни.
При наличии генной мутации одного пациента, рекомендуется пройти обследование всем его родственникам. Таким образом, можно обнаружить опухоли на ранней стадии, что значительно увеличит шансы для лечения и полного выздоровления.
В самом начале своего развития, злокачественное образование в кишечнике растет практически без выраженных признаков. Только по мере его прогресса начинают проявляться такие симптомы:
Боли в животе. В зависимости от локализации опухоли, боль может быть разной: ноющей, давящей или в виде легких схваток.
Стабильный дискомфорт в желудке и кишечнике, а именно: чувство вздутия, частое газообразование и урчание.
Нерегулярный стул. Запоры и поносы могут чередоваться.
Возникновение рвотного рефлекса без причин, частые отрыжки и тошнота.
Чувство тяжести и переполнения желудка.
Помимо основных симптомов, ярким показателем образования являются кровяные сгустки в каловых массах. На цвет они бордово-коричневые, по причине сворачиваемости. Такой признак характерный для опухоли, расположенной в самом начале толстого кишечника. При обнаружении крови – следует незамедлительно обратиться к врачу!
Зрелая стадия ННРТК имеет разную симптоматику, в зависимости от места локализации образования. Клиническая картина условно разделяется на две стороны кишечника: правую и левую.
Опухоль в правой части сопровождается такими симптомами:
болевые ощущения, преимущественно, в правой стороне живота;
потеря сил, слабость всего организма;
наличие прощупывания образования.
Когда злокачественное образование развивается в правой стороне толстой кишки, у некоторых пациентов может повышаться температура. По статистике это 2 из 10 больных. Незначительная лихорадка может беспокоить человека долгое время, и многие считают это явление простудным синдромом. Однако, в такой ситуации, рекомендуется срочное обследование желудочно-кишечного тракта, так как повышение температуры – первый показатель правосторонней опухоли.
Симптоматика левостороннего ННРТК значительно отличается от недуга справа. Для рака такой локализации характерно возникновение нескольких мелких образований. Они являются препятствиями для равномерного распределения кала в кишечнике.
У пациентов данной категории наблюдаются продолжительные запоры. Задержка испражнения может длиться до 20 дней, так как плохо поддается медикаментозному лечению. Больной таким видом недуга может ощущать боли в животе, тяжесть и вздутие, что характерно для правостороннего рака. Однако, причиной этих симптомов является не опухоль, а
Необходимые анализы и обследования
Диагностика наследственной онкологии кишечника – довольно сложная задача. Для обследования необходимо детальное исследование семейного анамнеза и генетическое тестирование. На практике такой процесс является дорогостоящим и занимает много времени. По этой причине, обследовать все население невозможно и нецелесообразно.
При выявлении наследственности заболевания, врачи используют стандартные методы обследований, как для классического рака кишечника:
Врач прощупывает нижнюю область живота пациента. Методом пальпации специалист может определить наличие, размер образования.
Пациент должен сдать общий анализ крови на выявление анемии, анализ мочи, а также анализ кала на скрытую кровь и гельминтозы.
С помощью современных аппаратов специалист имеет возможность осмотреть сигмовидную и прямую кишки. Основные исследования – это томография, ректороманоскопия и колоноскопия (осмотр с помощью эндоскопа).
Для оценки состояния других органов, а также для диагностики возможных метастазов, проводиться рентгенография и УЗИ. А в последние годы самые точные показатели получают с помощью МРТ (магнитно – резонансной томографии).
Лечение наследственного неполипозного рака кишечника .
Диагноз наследственного неполипозного рака кишечника (ННРК) устанавливают на основе семейного анамнеза; пациенты не имеют различий в симптоматике. Минимальные критерии, позволяющие предположить наследственный неполипозный рак кишечника (ННРК) как причину случая колоректального рака или другой опухоли, — наличие наследственного неполипозного рака кишечника (ННРК) у трех членов семьи, по крайней мере, два из которых — первой степени родства, не менее чем в двух поколениях, причем развитие колоректальной опухоли, по крайней мере, у одного из больных должно произойти до 50 лет. У пациентов без семейного анамнеза, но с рано появившимся колорек-тальным раком показан ДНК-анализ клеток опухоли, позволяющий обнаружить микросателлитную нестабильность. Для диагностики применяют также иммуно-гистохимическое выявление белков MLH1 и MSH2. Раннее распознавание наследственного неполипозного рака кишечника (ННРК) необходимо для эффективного вмешательства; колоноскопический контроль проксимальных отделов толстой кишки, начатый в возрасте 25 лет, увеличивает ожидаемый срок жизни на 13,5 года, а профилактическое хирургическое удаление кишечника в возрасте 25 лет увеличивает ожидаемый срок жизни на 15,6 года. Биопсия эндометрия и абдоминальное УЗИ у женщин группы риска не показали эффективности в предупреждении рака матки, встречающегося при этом заболевании. В семьях с известными унаследованными мутациями идентификация мутаций в генах репарации ДНК помогает сфокусировать внимание на конкретных членах семьи, но если мутация неизвестна, это не отрицает потребности в частых осмотрах.
Риски наследования наследственного неполипозного рака кишечника.
Эмпирический общепопуляционный риск развития колоректального рака — 5-6%. Этот риск заметно изменяется в зависимости от семейного анамнеза. Относительный риск для пациентов, имеющих родственников первой степени с колоректальным раком, выше популя-ционного в 1,7 раза; он возрастает в 2,75 раза, если коло-ректальный рак наблюдали у двух и более родственников первой степени родства. Если опухоль у такого родственника развилась до 44 лет, относительный риск возрастает более чем в 5 раз. Обратите внимание, что пациент с унаследованной мутацией генов репарации неспаренных оснований ДНК имеет 50% риск родить ребенка, несущего ту же мутацию. Все дети, получившие такую мутацию, имеют приблизительно 90% риск развития опухолей в течение жизни, принимая пенетрантность наследственного неполипозного рака кишечника (ННРК) за 80%, плюс фоновый общепопуляционный риск опухолей кишечника и других опухолей, связанных с наследственным неполипозным раком кишечника (ННРК) (желудка, тонкой кишки, поджелудочной железы, почек, эндометрия, яичников). Пренатальная диагностика очень спорная и не входит в стандартные рекомендации, но теоретически возможна, если известна наследуемая мутация у родителя. Из-за неполной пенетрантности и варьирующей экспрессивности тяжесть и возраст появления рака кишечника и других опухолей предсказать невозможно.
Пример наследственного неполипозного рака кишечника.
40-летняя женщина, бухгалтер, мать троих детей, направлена в клинику онкогенетики лечащим врачом для консультации относительно ее семейного анамнеза опухолей. У ее отца, брата, племянника, племянницы, дяди по отцу и бабушки по отцу развился колоректальный рак. В анамнезе у пациентки не было терапевтических или хирургических проблем. Данные медицинского осмотра оказались нормальными. Генетик объяснил женщине, что ее семейный анамнез напоминает наследственный неполипозный рак кишечника, и наиболее эффективный способ определить генетическую причину рака в ее семье — молекулярный анализ живого больного члена семьи. После обсуждения с племянницей, единственной выжившей из больных членов семьи, женщина и племянница вернулись в клинику для обследования. Анализ архивного образца ткани опухоли, удаленной из кишечника, выявил микросателлитную нестабильность; последующее секвенирование ДНК из образца крови, полученного от племянницы, обнаружило наследуемую мутацию в гене MLH1. Сама пациентка не имела данной мутации; в связи с этим генетик заключил, что риск для нее самой и ее детей по развитию рака кишечника равен общепопуляционному. Однако оказалось, что у ее здорового брата мутация есть, и ему рекомендован постоянный ежегодный колоноскопический контроль.
Для своевременного обнаружения заболевания, а также для предотвращения неполипозного рака толстой кишки, необходимо следить за состоянием своего организма, а именно:
Периодически проходить осмотр у врача.
Незамедлительно лечить любые заболевания ЖКТ.
Соблюдать уровень витаминов А и С в организме.
Максимально правильно питаться.
Вести здоровый образ жизни и поддерживать физическое здоровье.
Наследственный неполипозный рак кишечника встречается с частотой 2-5 на 1000, что составляет приблизительно 3-8% колоректального рака. НРТК является наследственным заболеванием. Недуг может возникнуть по причине семейного рака (синдром Линча), или наследованием аденоматозных полипов. Основной причиной возникновения ННРТК является мутация гена, отвечающего за процессы в молекулах ДНК. Диагностика наследственной онкологии кишечника – довольно сложная задача. Для обследования необходимо детальное исследование семейного анамнеза и генетическое тестирование. На практике такой процесс является дорогостоящим и занимает много времени. По этой причине, обследовать все население невозможно и нецелесообразно. Раннее распознавание наследственного неполипозного рака кишечника (ННРК) необходимо для эффективного вмешательства
Список используемой литературы
1.Медицинская генетика /Роберт Л. Ньюссбаум ,Родерик Р. Мак-Инне,Хантингтон Ф . Виллард «ГЭОТАР-Медиа» 2010
2. Российский журнал Гастроэнтерологии ,Гепатологии ,Колопроктологии,2014
Рак толстой кишки: причины и следствия
Существует множество гипотез о причинах возникновения рака прямой кишки. Учеными установлено, что в любой живой клетке содержится протоонкоген, который при определенных условиях преобразуется в онкогеном. Стимулом для мутации может быть как генетическая предрасположенность, так и внешние факторы. Если первые видоизменения произошли в соматической клетке – карцинома ненаследственная, в герминальной (половой) – наследственная.
Неполипозный колоректальный рак: наследственность
 Синдром Линча
Синдром Линча
Генетическую патологию, поражающую толстый кишечник, называют синдромом Линча. Это аутосомно-доминантное заболевание, при котором образуются, злокачественные неоплазии. Развитие наследственной карциномы толстой кишки часто обусловлено герминативной мутацией одного из генов восстановления ДНК. Особенности данного вида колоректального рака: ранее начало (до 50 лет) и высокая частота первично-множественных опухолей. Современные методы диагностики могут выявить синдром Линча в 89% случаев. Люди с таким диагнозом имеют 70-80% риска развития новообразований на протяжении всей жизни.
Как диагностировать наследственный неполипозный колоректальный рак? Гены системы репарации ДНК (MLH1, MLH3, MSH2, MSH3, MSH6, PMS1 и PMS2) необходимо проверить на наличие мутаций.
Крупные международные исследования выявили, что синдром Линча составляет 3% от всех случаев рака толстой кишки в мире. Более 75% пациентов с данным заболеванием – носители мутированных генов MLH1, MSH2, MSH6. Еще одной распространенной наследственной причиной, провоцирующей опухоли толстой кишки, является диффузный полипоз (семейный аденоматоз). Его проявление – это разрастание железистого эпителия над слизистой оболочкой. Чем больше размер полипа, тем выше вероятность его перехода в злокачественное образование. Вызывает данный колоректальный рак мутация в гене APС (супрессоре), который отвечает за профилактику опухолевого видоизменения клетки. В нормальном состоянии его продукт – антионкобелок, выстуает в роли ингибитора. Трансформации супрессора приводят к полной утрате функций подавления и задерживания физико-химических процессов.
О чем говорит ген MUTYH

В 2002 году были обнаружены мутации в гене MUTYH, влияние которого на формирование предрасположенности к онкозаболеваниям имеет несколько особенностей:
- рецессивность характера наследования;
- большое количество вариаций MUTYH-патологий. Распространенным последствием видоизменения данного гена считают образование незначительного количества аттенуированных полипов;
- опухоли содержат множественные трансверзии.
До 1% из всех случаев заболевания раком толстой кишки в мире вызвано мутациями в гене MUTYH. Пациентам с данным диагнозом регулярно назначаются скрининг кишечника, начиная с 20 лет.
В постановке диагноза «неполипозный колоректальный рак» генетика является важным фактором, на который обращают внимание в первую очередь. Если наследственность исключена, значит, заболевание вызвано внешними факторами, такими как:
- неправильное питание. Фактические данные ВОЗ говорят о прямой связи переизбытка красного мяса и нехватки клетчатки в рационе пациентов, у которых выявили колоректальный рак;
- хронические заболевания толстой кишки (язвы, колит);
- сахарный диабет;
- вредные привычки (алкоголь, курение);
- высокий индекс массы тела;
- отсутствие физической активности.
Неполипозный колоректальный рак: диагностика
Для постановки диагноза врач должен проанализировать историю болезни, провести физикальный осмотр пациента и ознакомиться с результатами всех обследований и анализов. Наследственный синдром Линча можно определить при помощи генетического тестирования. Но из-за отсутствия типичной клинической картины, выявить пациента, которому необходим данный анализ, сложно.

В 1991 году группа международных исследователей согласовала список клинических признаков наследственного неполипозного рака толстой кишки, он состоит из таких пунктов:
- ранний срок возникновения новообразований (до 50 лет);
- наличие минимум 3-х родствеников с морфологически диагностированным раком толстой кишки;
- отсутствие семейного аденоматозного полипоза;
- наличие родственников с колоректальным раком как минимум в 2-х поколениях.
Наследственый неполипозный колоректальный рак у женщины является серьезным поводом для обследования ее репродуктивной системы на наличие злокачественных образований. Около 50% пациентов с раком эндометрия имеют герминогенные мутации, с раком яичников – 10-15%. В рамках планового наблюдения женщинам с наследственным неполипозным колоректальным раком назначают трансвагинальное ультразвуковое исследование малого таза и анализ на онкомаркеры CA-125.
Полипозный колоректальный рак: диагностика

Для выявления злокачественных новообразований в первую очередь собирают семейный анамнез пациента (определяют есть ли генетические предрасположенности). Далее проводится колоноскопия – эндоскопический (внутрипросветный) метод исследования слизистой оболочки толстой кишки, который выявляет патологически измененные ткани и полипы. В ходе процедуры они удаляются полностью или берется их часть для гистологии. В случаях, когда образования имеют широкое основание и не могут быть безопасно удалены при колоноскопии, рассматривается хирургическое вмешательство.
У 75% людей с колоректальным раком выявляют повышенный уровень раково-эмбрионального антигена и онкомаркеры СА19.9. Последующий контроль данных показателей, помогает диагностировать рецидивы на ранних стадиях.
Колоноскопия является наиболее высокоинформативным способом диагностики, который позволяет правильно и точно определить состояние толстой кишки. При наличии полипов или других патологий в кишечнике необходимо регулярно проходить скрининговое исследование, частоту проведения которого определяет врач.
Метастатический КРР

Симптомы и интенсивность их проявлений зависят от стадии заболевания. На ранних этапах рак может иметь слабовыраженную симптоматику или вообще протекать без нее. Основные признаки наличия злокачественных образований:
- боль и дискомфорт в животе;
- диареи, вздутия, запоры;
- кровь в кале;
- анемия;
- резкая потеря веса и недомогание.
Из-за отсутствия симптомов или их сходства с проявлениями распространенных заболеваний злокачественные новообразования в толстой кишке часто диагностируется на поздних стадиях. Клиническая картина говорит, что 50% пациентов с колоректальным раком имеют метастазы в печени, 10%– в брюшине. Распространяются раковые клетки из первичного очага через кровь. Вторичные опухоли могут быть единичными или множественными. По расположению метастазы делятся на региональные и периферические.
Колоректальный рак: сколько живут с таким диагнозом
В Украине, как и во всем мире, существует тенденция роста заболевания карциномой толстой кишки. При этом 70% диагнозов устанавливаются на поздних стадиях развития. По данным ВОЗ каждый год в мире выявляют 600 тысяч новых случаев образования злокачественных опухолей в толстой кишке. Если рак диагностирован на ранней стадии, прогнозы очень позитивные – более 80% пациентов живут дольше 5 лет. Если же диагностирован метастатический колоректальный рак – продолжительность жизни у 40% пациентов составляет менее года. Без специфического лечения около 2% проживают пятилетний срок.
В очередной раз обращаем внимание на необходимость внимательно следить за своим здоровьем – соблюдать принципы ЗОЖ, периодически проходить профилактические осмотры. Любое заболевание, в том числе онкологическое, выявленное на ранней стадии с высокой долей вероятности может быть побеждено.

 Синдром Линча
Синдром Линча
