Аутологичная трансплантация гемопоэтических стволовых клеток при рассеянном склерозе
Одним из новых подходов для лечения рассеянного склероза является трансплантация стволовых клеток. Различают ауто- и аллогенную трансплантацию. В первом случае стволовые клетки забирают у пациента перед началом лечения и вводят обратно в организм после проведения курса радио-химиотерапии. Во втором, источником стволовых клеток служит костный мозг донора. Аллогенная трансплантация более рациональна при лечении аутоиммунных заболеваний, в отличие от аутотрансплантации, т.к. достаточно высок риск повторной аутоиммунизации организма, но с другой стороны более высокая смертность при аллотрансплантации (15-35%), чем при ауто (3-10%) [Tyndall A, Gratwohl A,1997, Bone Marrow Transpl.] делают аутотрансплантацию более привлекательной.
Теоретической основой для разработки обсуждаемого метода лечения стали эксперименты, продемонстрировавшие, что при рассеянном склерозе стволовая полипотентная клетка генетически стабильна, а аутореактивный клон Т-лимфоцитов образуется на более низком уровне клеточной дифференцировки [1,2]. Поэтому, путем использования иммуноаблативной терапии с последующей трансплантацией костного мозга или периферических стволовых кроветворных клеток, можно радикально очистить от патологического клона Т-лимфоцитов лимфатическую систему, а затем восстановить нормальную иммунную систему [3,4,5,].
Первая согласительная конференция Европейской группы трансплантации костного мозга (EBMT) состоялась в феврале 1998 года в Милане. Участие в конференции приняли представители шестнадцати европейских стран, США и государств Южной Америки. Глвными вопросами форума были: основные критерии отбора пациентов, разработка оптимальных схем лечения, стандартизация оценки результатов терапии, создание международной рабочей группы для оценки безопасности и результативности данного метода лечения больных рассеянным склерозом (Blood and Marrow Transplantation and the MS Study Group, 2000).
Показаниями к назначению трансплантации костного мозга являются: ремиттирующее течение рассеянного склероза с тремя и более обострениями в год, отсутствием результата от проводимой терапии (в т.ч. с применением интерферонов), нарастающее ухудшение состояния с изменениями двигательных функций. Противопоказания: тяжелые заболевания, значительные изменения функций почек и печени, инфекции. Перед операцией пациенту в доступной форме должны объяснить ее цель, схему проведения, длительность, вероятные осложнения и побочные эффекты, получить согласие пациента на планируемый метод терапии.
Методика и принципы трансплантации стволовых кроветворных клеток: Известно, что рассеянный склероз – аутоиммунное демиелинизирующее заболевание нервной системы, при котором собственные иммунокомпетентные клетки ( Т- и В-лимфоциты, макрофаги, моноциты) разрушают миелин центральной нервной системы с последующим формированием бляшки. Идея применения трансплантации стволовых кроветворных клеток основана на том что изменения, приводящие к формированию клона аутоагрессивных Т- и В-клеток, происходят не на уровне стволовых клеток, а гораздо позже при их дифференцировки. Таким образом, если ликвидировать клон патологических клеток, то можно затем вырастить здоровые Т- и В-лимфоциты. На практике с этой задачей справляются при помощи высоких доз имммуносупрессоров, либо облучением лимфоидной системы организма. Затем, здоровые стволовые клетки крови вносят в «зачищенную» строму костного мозга. В дальнейшем из них формируется клон ауторезистентных клеток.
Технология проведения трансплантации гемопоэтических стволовых клеток включает следующие этапы:
- Сбор периферических стволовых клеток крови. Для мобилизации используют колоний-стимулирующий фактор (нейпоген в дозе 10мг/кг в течение 3-4 дней). Затем проводят концентрирование и сбор стволовых клеток методом лейкофореза с использованием специальных фильтров. В полученный пул стволовых клеток добавляют криопротектор и хранят в жидком азоте до трансплантации.
- Этап кондиционирования. Супрессивная терапия по методике BEAM (Кармустин 300 мг/м2 в первый день, Цитозинарабинозин 200 мг/м2 и Этопозид 200 мг/м2 в 3,4,5 дни, Мелхалан 140 мг/м2 впоследний день).
- Реинфузия стволовых клеток.
Между первым и вторым этапом существует промежуток, как правило, от 2 до 3 недель для нормализации показателей периферической крови [13].
Результаты первых трансплантаций при рассеянном склерозе выделенных из периферической крови аутологичных гемопоэтических стволовых клеток впервые были опубликованы в 1997 году греческой группой Fassas A [14]. Во многих центрах США и Европы уже произведено более 200 трансплантаций.
Некоторые результаты I/II фазы клинических испытаний метода аутотрансплантации стволовых клеток переферической крови больным рассеянным склерозом
| Рабочая группа | Число пациентов | Смерти после трансплантации | Смерти от других причин | Основной результат, примечания |
|---|---|---|---|---|
| Fassas et al. [1,2,9] | 35 | 1 | 1 (2 года, гемофилия) | 81% без прогрессирования в течении 5 лет ВП, редукция активности по данным МРТ |
| Kozak et al. [7,8] | 15 | 1 (осложнения прогресса РС) | 11 из 15 пациентов – стабилизация или улучшение; МРТ – отсутвие новых очагов повреждения, но 1 – прогресс | |
| EBMT [10] | 85 | 5 | 2 (осложнения прогресса РС) | 78% без прогрессирования в течении 3 лет ВП, редукция активности по данным МРТ |
| Italian coop. [11,12] | 16 | МРТ: уменьшение повреждений, но атрофия прогрессировала | ||
| Carreras et al. [13,14] | 15 | 12 из 15 пациентов – стабилизация или улучшение; МРТ: уменьшение повреждений, но атрофия прогрессировала | ||
| Burt et al. [5,6] | 27 | 2 (осложнения прогресса РС) | Прогресс заболевания чётко зависил от степени начального дисфункционального статуса; МРТ: уменьшение повреждений, но атрофия прогрессировала | |
| Openshaw et al. [4] | 5 | 1 | 1 (инфекция, через 9 мес.) | Стабилизация процесса у 4 пациентов из 5; МРТ: исчезновение некоторых повреждений |
| Nash et al. [15] | 25 | 1 | 1 (осложнения прогресса РС) | Прогресс в 27% в течение 3 лет; МРТ: уменьшение повреждений, но у 4 – появление новых, атрофия минимальна |
ВП – вторичный прогресс; МРТ – магнитно-резонансная томография
После анализа клинических результатов были сделаны следующие выводы:
- Терапия аутологичными гемопоэтическими стволовыми клетками безопасна и не вызывает системной токсичности.
- При терапии гемопоэтическими стволовыми клетками возможно проведение высокодозной иммуносупрессии, способствующей более выраженному результату.
- Аутологичная трансплантация гемопоэтическими стволовыми клетками подавляет системную воспалительную реакцию, ассоциированную с прогрессом заболевания.
- Индикатор обязательного строгого отбора больных – летальность 1-1,5%, связанная с операцией.
- Пациенты молодого возраста с небольшой выраженностью изменения функций, но с быстро прогрессирующим из-за иммунных нарушений и системных воспалительных реакций в отсутствие нейродегенерации заболеванием, имеют весьма высокий шанс на положительный эффект от этого метода лечения.
- Неясным еще является действие трансплантированных клеток. Сначала основной являлась теория о том, что после взятия клеток и высокодозной химиоабляции оставшегося происходит полное замещение клеток иммунной системы реципиента. Но сейчас ученые склоняются к иному, более мягкому определению клеточной иммунорегуляции после трансплантации – “функциональная переустановка иммунной системы” на регуляторном уровне. Скорее спекулятивными кажутся предположения о возможной миграции с последующей нейродифференцировкой и тканевой заменой гемопоэтических стволовых клеток в ЦНС.
Первая операция по пересадке при рассеянном склерозе стволовых кроветворных клеток периферической крови в России по протоколу Европейской группы трансплантации костного мозга (EBMT) была проведена в Военно-Медицинской Академии совместно кафедрами гематологии и клинической иммунологии и нервных болезней в 1999 году [3,4,5]. В настоящее время в России действует несколько крупных медицинских исследовательских центров, занимающихся трансплантацией стволовых клеток крови при РС. Среди них: ГВКГ им. Бурденко, Москва; ВМА, Санкт-Петербург; ГМУ им. акад. И.П.Павлова, Санкт-Петербург; Калининский региональный центр, Самара; Институт клинической иммунологии, Новосибирск; Свердловский областной гематологический центр, Екатеринбург.
К сожалению, трансплантация стволовых кроветворных клеток не дает возможности компенсации тех морфофизиологических изменений, которые уже имеют место в организме, однако, позволяет остановить процесс аутоиммунизации, т.е., избежать дальнейшего разрушения миелиновых оболочек и развития комплекса патологических симптомов.
После окончания завершающей фазы широких рандомизированных клинических исследований можно будет окончательно судить о целесообразности применения метода трансплантации стволовых кроветворных клеток для лечения рассеянного склероза.
ЛИТЕРАТУРА
1. Burt RK, Traynor AE, Cohen B et al. T cell-depleted autologous hematopoietic stem cell transplantation for multiple sclerosis: report on the first three pacients. Bone Marrow Transplant 1998; 21(6): 537-41
2.Karussis D, Vourka-Karussis U, Mizrachi-Koll R, Abramsky O. Acut/relapsing experimental autoimmune encephalomyelitis: induction of long lasting, antigen-specific tolerance by syngenetic bone marrow transplantation. Mult Scler 1999; 5(1): 17-21
3.Трансплантация костного мозга в клинике внутренних болезней. / Клиническая медицина и патофизиология, СПБ № 2, 1997 г. 120/6 / А.А. Новик, А.Н. Богданов
4.Трансплантация периферических стволовых кроветворных клеток у больных с рассеянным склерозом. / V-Всероссийская научно-практическая конференция ”Актуальные вопросы диагностики и лечения в многопрофильном лечебном учреждении” СПБ 26-27.04.2001 (105) / Новик А.А., Одинак М.М., Бисага Г.Н., Новицкий А.В.
5.Опыт первых трансплантаций стволовых кроветворных клеток при рассеянном склерозе. / Клиническая онкология и гематология N4 2001 (Журнал Новосибирского общества клинических онкологов и онкогематологов) 10-17/36 / А.А. Новик, А.Н. Богданов, М.М. Одинак, С.В. Волошин, Г.Н. Биссага
6. Lovell-Badge R. // Nature. 2001. V. 414. P. 88-91.
7. Корочкин Л.И. // Онтогенез. 2003. Т.34, N 3. С. 164-166.
8. Корочкин Л.И. // Онтогенез. 2000. Т. 31, N 2. С. 94-113.
9. Корочкин Л.И. Биология индивидуального развития. М. Наука. 2002. 263 с.
10. Корочкин Л.И. // Изв. АН. Сер. Биол. 2001. N 6. С. 666-671.
11. Корочкин Л.И. // Генетика. 2000. Т. 36. N 11. С. 1438-1442.
12. Сухих Г.Т., Малайцев В.В. // Бюлл. Эксп. Биол. и Мед. 2001. Т.131, N 2. С. 244-255
13. G. Comi, L. Kappos, M. Clanet, A. Tyndall, M. Filippi et al. Guidelines for autologous blood and marrow stem cell transplantation in multiple sclerosis. J. Neurol (2000) 247: 376-382
14. Fassas A, et al. Peripheral blood stem cell transplantation in the treatment of progressive multiple sclerosis: first results of a pilot study. Bone Marrow Transplant 1997; 20: 631–638.
15. Fassas A, Kazis A. High-dose immunosuppression and autologous hematopoietic stem cell rescue for severe multiple sclerosis. J Hematother Stem Cell Res 2003; 12:701–711
16. Muraro PA, et al. Hematopoietic stem cell transplantation for multiple sclerosis: current status and future challenges. Curr Opin Neurol 2003; 16; 3: 299-305
17. Saiz A, Graus F. Transplantation of haematopoietic stem cells in multiple sclerosis. Rev Neurol 2002; 35; 12: 1136-1141
18. Fassas A, et al. Autologous stem cell transplantation in progressive multiple sclerosis – an interim analysis of efficacy. J Clin Immunol 2000; 20: 24–30.
19. Comi G, et al. Guidelines for autologous blood and marrow stem cell transplantation in multiple sclerosis: a consensus report written on behalf of the European Group for Blood and Marrow Transplantation and the European Charcot Foundation. J Neurol 2000; 247: 376–382.
20. Openshaw H, et al. Peripheral blood stem cell transplantation in multiple sclerosis with busulfan and cyclophosphamide conditioning: report of toxicity and immunological monitoring. Biol Blood Marrow Transplant 2000; 6: 563–575.
21. Burt RK, et al. Treatment of autoimmune disease by intense immunosuppressive conditioning and autologous hematopoietic stem cell transplantation. Blood 1998; 92: 3505–3514.
22. Burt RK, et al. Hematopoietic stem cell transplantation for progressive multiple sclerosis: failure of intense immune suppression to prevent disease progression in patients with high disability scores. Blood 2003; 102: 2373–2378. E-pub July 3, 2003.
23. Kozak T, et al. High-dose immunosuppressive therapy with PBPC support in the treatment of poor risk multiple sclerosis. Bone Marrow Transplant 2000; 5: 525–531.
24. Kozak T, et al. Immunoablative therapy with PBPC support with in vitro or in vivo T-cell depletion in patients with poor risk multiple sclerosis. Bone Marrow Transplant 2002; 29 (Suppl.2): S15.
25. Kimiskidis VK, et al. Autologous stem cell transplantation in multiple sclerosis: the MRI study. J Neurol 2002; 249(Suppl.1): I/61.
26. Fassas A, et al. Hematopoietic stem cell transplantation for multiple sclerosis: a retrospective multicenter study. J Neurol 2002; 249: 1088–1097.
27. Mancardi GL, et al. Autologous hematopoietic stem cell transplantation suppresses Gd-enhanced MRI activity in MS. Neurology 2001; 57: 62–68.
28. Saccardi R, et al. Autologous hematopoietic stem cell transplantation in secondary progressive MS: clinical, instrumental findings and impact on quality of life. Blood 2002; 100 (Suppl.): 865a
29. Carreras E, et al. CD34+ selected autologous peripheral blood stem cell transplantation for multiple sclerosis: report of the toxicity and treatment results at one year of follow-up in 15 patients. Haematologica 2003; 88: 306–314.
30. Saiz A, et al. MRI and CSF oligoclonal bands after autologous hematopoietic stem cell transplantation in MS. Neurology 2001; 56: 1084–1089.
31. Nash RA, et al. High-dose immunosuppressive therapy and autologous peripheral blood stem cell transplantation for severe multiple sclerosis. Blood 2003; 102: 2364–2372. E-pub May 22, 2003.
Эффективность стволовых клеток при рассеянном склерозе
Рассеянным склерозом именуется особая патология нервной системы — когда-то ее считали неизлечимой, сегодня же специалисты способны справиться с этим недугом при условии своевременно начатого лечения. Полноценный шанс на выздоровление предоставляет операция по пересадке стволовых клеток — такая методика считается инновационной, однако до сих пор признана не во всех странах.
Как показывает практика, пересадка стволовых клеток успела зарекомендовать себя с лучших сторон. После подобного вмешательства качество жизни пациентов существенно повышается.
Откуда берётся рассеянный склероз
Для того чтобы понять, какая схема терапии будет оптимальной для лечения рассеянного склероза, необходимо выяснить первопричину данного заболевания в каждом конкретном случае. По сей день специалисты не могут достоверно сказать, почему болезнь проявляется у того или иного человека. В числе провоцирующих факторов перечисляются:
- генетическая предрасположенность — у ребенка вполне возможно проявится такое заболевание, если ранее у его родственников наблюдались признаки рассеянного склероза;
- излишние интеллектуальные нагрузки, которые провоцируют психологическую нестабильность и стресс, что тоже может привести к заболеванию;
- ослабление иммунной системы, сопровождающееся частыми инфекциями и поражением структур головного мозга;
- аутоиммунные заболевания – они также могут выступать в качестве провоцирующих факторов, когда организм перестает воспринимать свои же ткани, считая их чужеродными и создавая защитные клетки, что вызывает хроническое течение воспаления и подрыв деятельности нервной системы;
- вредные привычки увеличивают риск возникновения рассеянного склероза, если человек злоупотребляет алкоголем и табаком несколько десятков лет, то шансы на то, что он столкнется с данным заболеванием, резко увеличиваются.
Как определить наличие рассеянного склероза
Лечение болезни невозможно без определения её проявлений. Последние напрямую связаны с поражением нервных волокон, а потому клиническая картина полностью зависит от той части тела, в которой сформирован очаг заболевания. К числу основных проявлений рассеянного склероза можно отнести:
- тремор конечностей;
- нарушение восприятия тела в пространстве;
- нарушение координации движений;
- отсутствие контроля над мышцами лица;
- покалывание кожных покровов;
- нетипичные проявления мышечного тонуса;
- сбои в мочеиспускании в сторону недержания.
Неврологически перечисленные симптомы проявляются, как смена настроения пациента, которое может варьироваться от плаксивости и депрессии до эйфории. Перед тем, как определить, действительно ли конкретному больному поможет пересадка стволовых клеток, специалист должен провести неврологический осмотр и исследовать нервную систему инструментально.
Что представляет собой методика пересадки стволовых клеток
Данный процесс основан на способности стволовых клеток дифференцироваться в конкретные зоны человеческого организма. В нашей стране трансплантация их при рассеянном склерозе допустима на законодательном уровне. Доказано, что подобная терапия приводит к полному восстановлению миелиновой оболочки волокон нервов мозга, положительно отражается она и на состоянии иммунной системы.
Важно! Использование стволовых клеток для лечения рассеянного склероза допустимо в случае, когда ранее уже применялись другие терапевтические мероприятия и значимого результата они не принесли. В обязательном порядке биоматериал необходимо забирать непосредственно от пациента, что позволяет снизить вероятность занесения инфекции, иммунологических несовпадений и возможных мутаций клеток.
Как проводится трансплантация
Данный процесс делится на три этапа, предварительно специалисты всегда оценивают исходное состояние здоровья человека, а также определяют ту стадию, в которой находится заболевание на конкретный момент времени.
Первым этапом является забор стволовых клеток. Учитывая, что дифференцировать нужные клетки в должном объеме сразу не представляется возможным, процедуру забора крови порой приходится проводить 3-4 раза. После этого полученные клетки замораживаются до пересадки.
Второй этап подразумевает уничтожение тех иммунных клеток, которые ранее были поражены патологическими процессами. Для этой цели применяют противовоспалительные и иммуносупрессивные препараты. Именно такое комплексное воздействие подготавливает организм к трансплантации.
Завершающим этапом является подача внутривенно в кровяное русло стволовых клеток.
От чего зависит результат лечения
Для того чтобы получить должный эффект и значительно повысить качество жизни пациента, необходимо соблюсти целый перечень условий. Повышенная эффективность процедур достигается, если воздействовать на заболевание в определённой стадии, контролируя его прогрессирование. Многое зависит от возраста больного и восприимчивости его тканей к такой терапии. Сопутствующие тяжёлые заболевания тоже имеют значение.
Больше всего шансов на выздоровление имеют пациенты на начальной стадии рассеянного склероза, так как в этом случае миелиновая оболочка регенерируется гораздо быстрее. Превосходный результат на практике демонстрировали и те люди, у которых рассеянный склероз наблюдался на протяжении 7-8 лет. После проведения нескольких процедур восстанавливалось большинство клеток, включая те, что были поражены на 80%.
Вероятные риски
Когда в организм пациента вводятся его собственные стволовые клетки, риск отторжения сводится к минимуму. В качестве исключения можно привести пример тех пациентов, которые изначально имели аутоиммунные патологии. В подобных ситуациях должный эффект можно получить посредством дополнительного приема медикаментов иммуносупрессивного типа.
К числу осложнений после пересадки относятся редкие случаи:
- неправильно подобранного объёма материала;
- несоблюдения стерильности;
- недостаточной подготовленности организма;
- невыдержанного интервала между этапами введения стволовых клеток.
Важно! Крайне нежелательно вводить пациенту стволовые клетки другого человека — такое рискованное мероприятие может привести к летальному исходу.
Только ранняя диагностика заболевания и своевременное введение стволовых клеток с использованием специализированного оборудования и привлечением врачей высокой квалификации позволяет обеспечить полное выздоровление.
Трансплантация кроветворных стволовых клеток при рассеянном склерозе
Рассеянный склероз (РС) – хроническое прогрессирующее заболевание центральной нервной системы, которое клинически проявляется мультисистемной неврологической симптоматикой, а патоморфологически характеризуется образованием множественных очагов демиелинизации в белом веществе головного и спинного мозга. Основным механизмом, приводящим к повреждению миелина, является опосредованная Т-лимфоцитами реакция гиперчувствительности замедленного типа, а непосредственными клетками-эффекторами иммунопатологического процесса – макрофаги.
Существующие методы лечения не позволяют достичь устойчивого терапевтического эффекта при рассеянном склерозе. Выдвигалась гипотеза, основанная на доклинических данных, о высокой эффективности аллогенной транплантации стволовых кроветворных клеток (ТСКК). Однако высокая посттрансплантационная летальность не позволила приступить к клиническим исследованиям данного вида терапии РС. По мнению большинства экспертов одним из наиболее перспективных методов лечения РС на сегодняшний день является высокодозная химиотерапия (ВДТ) с аутологичной трансплантацией стволовых кроветворных клеток (АуТСКК). Начиная с 1995 года, безопасность ВДТ+AyТКСК при РС была изучена в ряде клинических исследований. Тем не менее, объем информации о клинической эффективности данного метода и, особенно, о его влиянии на качество жизни больных РС, остается недостаточным. Кроме того, большинство пациентов, включенных в вышеупомянутые исследования, имели вторично-прогрессирующую форму РС и значительную степень инвалидизации со значением шкалы EDSS 4.5-8.5 баллов. К сожалению, даже полное прекращение активности иммунопатологического процесса у таких больных не может привести к значительному улучшению качества жизни. Поэтому вопрос об оптимальных сроках проведения трансплантации по-прежнему остается открытым.
В статье приведены результаты проспективного многоцентрового исследования безопасности и эффективности ВДТ+АуТКСК при РС, которое было начато в 1999 году и в настоящее время объединяет 5 крупных российских медицинских центров. Изучали влияние ВДТ+АуТКСК на клиническое течение и показатели качества жизни больных с разными формами и стадиями РС.
Ключевые слова
трансплантация стволовых кроветворных клеток, рассеянный склероз, качество жизни, ранняя трансплантация, этапная трансплантация, трансплантация спасения
Материалы и методы
В исследование было включено 109 больных РС (49 мужчин, 60 женщин; средний возраст – 33 года; диапазон – 17-54): 51 с вторично-прогрессирующим течением, 19 с первично-прогрессирующим, 8 с прогрессирующе-рецидивирующим и 31 с рецидивирующе-ремиттирующим течением. Значение индекса EDSS до трансплантации колебалось от 1.5 до 8.0 баллов (в среднем было равно 5.0 баллам). Длительность наблюдения составила в среднем 19 месяцев (от 6 до 108 месяцев). Активность заболевания определяли с помощью неврологического осмотра и данных магнитно-резонансной томографии.
Больным были выполнены следующие виды ВДТ+АуТКСК:
– Ранняя трансплантация проводилась в дебюте заболевания при наличии неблагоприятных прогностических факторов в отношении химиорезистентности или возможности тяжелой инвалидизации больного.
– Этапная трансплантация проводилась при выходе заболевания из-под контроля традиционных методов лечения и формировании вторичной химиорезистентности.
– Трансплантация спасения проводилась в далеко зашедшей стадии заболевания при высокой активности иммунопатологического процесса и быстром прогрессировании инвалидизации больного.
Тридцати двум больным была выполнена ранняя трансплантация (EDSS 1.5-3.0); 70 больным – этапная трансплантация (EDSS 3.5-6.5) и 7 больным – трансплантация спасения (EDSS 7.0-8.0).
Оценку клинического ответа и ответа, связанного с качеством жизни, проводили до трансплантации, при выписке из стационара, через 3, 6, 9 и 12 месяцев после трансплантации, затем – каждые 6 месяцев в течение первых 4 лет и ежегодно впоследствии. Изучение неврологического статуса включало определение выраженности неврологического дефицита по шкале EDSS и магнитно-резонансную томографию. Качество жизни больных 16 www.ctt-journal.com 2008;1(2) оценивали с использованием опросников FACT-BMT (функциональная оценка состояния больных после трансплантации костного мозга) и FAMS (функциональная оценка больных с рассеянным склерозом). Клиническим улучшением считали уменьшение выраженности неврологической симптоматики, по меньшей мере, на 0.5 балла по шкале EDSS по сравнению с исходным уровнем, при условии, что это улучшение было подтверждено через 6 месяцев на следующем визите. Любое увеличение выраженности неврологической симптоматики по шкале EDSS считали прогрессированием заболевания. Рецидив констатировали при появлении новых симптомов или нарастании выраженности прежних симптомов, по меньшей мере, в течение 24 часов в отсутствие лихорадки у пациента, который был стабилен в течение 4 предшествующих недель. Ответ, связанный с качеством жизни, характеризовался как минимальный, умеренный, хороший или максимальный. Для определения ответа, связанного с качеством жизни, рассчитывали различия в значении интегрального показателя качества жизни до проведения трансплантации и в различные периоды времени после нее.
Результаты
У всех 79 больных со сроком наблюдения ≥9 месяцев отмечено клиническое улучшение или стабилизация в течении заболевания. Во время проведения трансплантации не было зарегистрировано ни одного смертельного исхода и тяжелых неконтролируемых побочных эффектов. Через 6 месяцев после трансплантации распределение пациентов согласно клиническому ответу было следующим: улучшение – 42 (53%) больных, стабилизация – 37 (47%) больных. Среди больных с улучшением у 20 было вторично-прогрессирующее течение, у 7 – первично-прогрессирующее, у 4 – прогрессирующе-рецидивирующее и у 11 – рецидивирующе-ремиттирующее течение. В этой группе 25 больных проведена этапная трансплантация, 15 – ранняя и 2 – трансплантация спасения. Из 37 больных, у которых зарегистрирована стабилизация заболевания, у 19 было вторично-прогрессирующее течение, у 8 – первично-прогрессирующее, у 2 – прогрессирующе-рецидивирующее и у 8 – рецидивирующе-ремиттирующее течение. В этой группе 23 больным проведена этапная трансплантация, 9 – ранняя и 5 – трансплантация спасения.
В более длительные сроки наблюдения у 40 больных (50.6%) сохранялось улучшение, у 34 (43.1%) – стабилизация. У одного больного после 6 месяцев и двух больных после 18 месяцев стабилизации произошло повышение индекса инвалидизации. У двух пациентов прогрессирование заболевания наступило после 12 и 30 месяцев клинического улучшения. По данным МРТ у всех больных без прогрессирования заболевания после трансплантации отсутствовали активные или новые очаги поражения. В целом, 6-летняя выживаемость без прогрессии после ВДТ+АуТКСК составила 72%. Больные, у которых не было зарегистрировано признаков прогрессирования заболевания, не получали иммуномодулирующую или иммуносупрессивную терапию после трансплантации. Мониторинг качества жизни проводился у 44 пациентов, включенных в исследование. У 40 из них наблюдали улучшение показателей качества жизни через 6 месяцев после трансплантации. Улучшение параметров качества жизни установлено с помощью опросников – FACT-BMT и FAMS. Через 1 год после ВДТ+АуТКСК зарегистрировано следующее распределение пациентов в соответствии со степенью ответа, связанного с качеством жизни: у 3 больных наблюдали максимальный ответ (более чем 75% улучшение интегрального показателя качества жизни в сравнении с исходным уровнем); у 12 больных – хороший ответ (улучшение на 50-75%); у 11 больных – умеренный ответ (на 25-50%); у 13 – минимальный ответ (улучшение менее чем на 25%) и у 5 больных ответ, связанный с качеством жизни, отсутствовал. Следует отметить, что у пациентов с более длительным сроком наблюдения было отмечено дальнейшее улучшение показателей качества жизни. В статье представлена классификация типов трансплантации при рассеянном склерозе, основанная на концепции ВДТ+ТКСК при аутоиммунных заболеваниях.
Заключение
Высокодозная иммуносупрессивная терапия с аутологичной трансплантацией кроветворных стволовых клеток является эффективным методом лечения больных рассеянным склерозом: у большинства больных после ВДТ+АуТКСК зарегистрировано клиническое улучшение или стабилизация заболевания; ВДТ+АуТКСК сопровождается существенным улучшением качества жизни больных. Результаты свидетельствуют о целесообразности изучения результатов ранней трансплантации, этапной трансплантации и трансплантации спасения. Необходимы дальнейшие исследования для определения оптимальных сроков проведения трансплан-тации и уточнения режимов кондиционирования.
Эффективность пересадки стволовых клеток при рассеянном склерозе. Лечение рассеянного склероза стволовыми клетками

УЧРЕЖДЕНИЯ-РАЗРАБОТЧИКИ: ГУО «Белорусская медицинская академия
последипломного образования», УО «Белорусский государственный медицинский
университет», г. Минск.
МЕТОД КЛЕТОЧНОЙ ТЕРАПИИ РАССЕЯННОГО СКЛЕРОЗА
У пациентов развивается рассеянный склероз, когда ауто-антитела нацелены на собственные миелиновые антигены, вызывая демиелинизацию.
Клинические исследования показали, терапия методом трансплантации мезенхимальных стволовых клеток (МСК) эффективна при лечении повреждения нервов у пациентов с рассеянным склерозом (РС).

Расширенная диагностика перед трансплантацией клеток.
В программу лечения включена одна из самых современных и эффективных методик для диагностики, определения характеристики и анализа стадии заболевания.
Неврологический осмотр
Специальных тестов на РС нет. Вместо этого диагноз рассеянного склероза часто основан на исключении других состояний, которые могут вызывать аналогичные признаки и симптомы, что называется дифференциальным диагнозом.
Магнитно-резонансная томография (МРТ) – это тест выбора для диагностики рассеянного склероза в сочетании с первоначальными анализами крови. МРТ использует радиоволны и магнитные поля для оценки относительного содержания воды в тканях тела. Они могут обнаружить нормальные и аномальные ткани и выявить неровности.

ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
1. Рассеянный склероз (РС) (рецидивно-ремиттирующий и прогредиентнорецидивирующий типы течения при количестве баллов по расширенной шкале
инвалидизации Куртцке (EDSS) от 1 до 6,5), верифицированный на основании
клинико-диагностических критериев протоколов терапии рассеянного склероза,
утвержденных Министерством здравоохранения Республики Беларусь.
2. Прогрессирование заболевания (ухудшение неврологического статуса за
последний год >1 балла по шкале EDSS (если исходный уровень EDSS составлял
5,5 баллов.
3. Отсутствие эффекта от терапии, модифицирующей клиническое течение
заболевания и отсутствие эффекта/ухудшение патоморфологических показателей по
данным нейровизуализации в течение 6 месяцев до забора биологического
материала.
Мы готовы помочь. Отправьте нам запрос сегодня.
Как проводится трансплантация мезенхимальных стволовых клеток?
СХЕМА ЛЕЧЕНИЯ
Для разработки тактики лечения и определения схемы трансплантации стволовых клеток проводится консультация специалиста-невролога отделения регенеративной медицины и клеточной терапии. Также необходимо обязательное медицинское обследование.
1 этап. Костномозговая пункция.
Пациентам с РС, имеющим показания к проведению трансплантации МСК,
для получения взвеси клеток выполняют общепринятым методом
костномозговую пункцию.
Эксфузию костного мозга с целью получения МСК выполняют под местной
анестезией. Костный мозг аспирируют иглой Кассирского из области грудины
или иглами большого диаметра путем пункций гребня крыла подвздошной кости
с обеих сторон в шприцы, содержащие антикоагулянт (гепарин). Объем
забираемой костномозговой взвеси — от 30 до 100 мл.
2 этап. Выделение МСК костного мозга.
1. Мононуклеары из пунктата костного мозга выделяют по стандартной
методике сепарации на градиенте фиколл-верографин (р = 1,077).
2. Полученную суспензию клеток отмывают центрифугированием в течение
10 мин/400G в фосфатном буферном растворе и высевают во флаконы
культуральные пластиковые стерильные газопроницаемыми крышками в
специализированной среде для культивирования МСКв плотности 5×106
/см2
поверхности дна флакона.
3. Через 24 ч инкубации в СО2-инкубаторе среду с неадгезировавшимися
клетками собирают, флакон культуральный троекратно активно промывают
стерильным фосфатным буферным раствором и заливают специализированной
средой для культивирования МСК
3 этап. Трансплантация Клеточного продукта
Трансфузию МСК проводят в день 0.
Премедикацию, состоящую из внутривенного введения 60 мг преднизолона и
4 мл ондансетрона, выполняют за 15–30 мин до начала трансфузии МСК.
Трансфузию взвеси мезенхимальных клеток начинают сразу же после их доставки в
отделение. Введение выполняют в течение 20–30 мин внутривенно в дозе не менее
1 млн клеток на кг веса пациента.
Клеточная терапия рассеянного склероза
В Петербурге пациентов с рассеянным склерозом лечат с помощью стволовых клеток и химиотерапии
В Первом меде возрождают метод лечения тяжелых аутоиммунных заболеваний с помощью трансплантации собственных стволовых клеток. Пока он используется для пациентов с рассеянным склерозом в рамках клинической апробации. Хотя у метода уже есть собственная история.
Рассеянный склероз (РС) – аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга, что приводит к тяжелым двигательным и другим нарушением вплоть до глубокой инвалидизации.
О том, как в России и за рубежом сегодня лечат аутоиммунные заболевания с помощью высокодозной иммуносупрессивной терапии и аутологичной трансплантации гемопоэтических стволовых клеток, «Доктору Питеру» рассказал Алексей Полушин, к.м.н., невролог НИИ детской онкологии, гематологии и трансплантологии им. Горбачёвой, ассистент кафедры неврологии ПСПбГМУ им. Павлова.
– Алексей Юрьевич, трансплантацией стволовых клеток пациентам с таким аутоиммунным заболеванием, как рассеянный склероз, в мире начали заниматься еще в самом начале этого века. И очень быстро от нее отказались. Почему вы вернулись к этому методу?
– В сложные 1990-е и «творческие» (в медицинском плане) 2000-е годы у наших врачей выработалась негативная реакция к понятиям «стволовые клетки» и «трансплантация». Но только не у тех, кто с ними реально работает, спасая жизни, в том числе детские. Я говорю о гематологах и онкологах. И и сейчас мы говорим о технологиях, созданных ими, а не о тиражируемом сегодня понятии «лечение стволовыми клетками», под которым неизвестно что подразумевается.
Изначально именно они этот метод продвигали и продолжают его применять, используя принцип лечения гематологических онкологических заболеваний: с помощью высокодозной иммуносупрессивной терапии «обнулялся» костный мозг, а затем переливался донорский трансплантат. Тогда стало понятно, что метод аллогенной (донорской) трансплантации гемопоэтических стволовых клеток (ТГСК) сопровождается высокой частотой осложнений и смертности.
То есть, в начале века, проблемы оставались, да и сегодня мало что поменялось. Поскольку трансплантацию воспринимали, как терапию отчаяния, ее назначали тем, кому не помогала лекарственная терапия. А это годы. В итоге эффективность трансплантации выглядела, мягко говоря, невысокой, в особенности с учетом ожиданий пациентов, которые думали, что после нее они начнут бегать.
Опыт последних 20 лет использования ТГСК для лечения аутоиммунных заболеваний показал, что «обнулять» костный мозг, с использованием «жестких» режимов иммуносупрессивной терапии (химиотерапии, или как говорят врачи, кондиционирования), как при онкогематологических заболеваниях, не обязательно. И когда начали использовать аутотрансплантацию — пересадку собственных стволовых клеток пациента после «мягких» режимов химиотерапии, все встало на свои места. Сегодня гематологи, специализирующиеся на лечении аутоиммунных заболеваний, говорят, что самая эффективная терапия – та, что проведена в дебюте заболевания, потому что соответствует неврологическому принципу – «время – мозг».
– Что вы знаете о судьбах тех пациентов, которые прошли тогда через трансплантацию?
– Опыт применения трансплантации гемопоэтических стволовых клеток для пациентов с рассеянным склерозом имеет примерно такую же историю, как и ПИТРС (препаратов, изменяющих течение рассеянного склероза). Лечение с ее применением в нашем университете получили в общей сложности 45 человек. Я общаюсь и встречаюсь с людьми, которым сделали трансплантацию более 15 лет назад. Среди тех, кто прошел лечение в 2000-х, есть несколько человек, кому применили метод вовремя. Весной ко мне приходила женщина, которой в 37 лет сделали ТГСК. Сейчас ей 51 год — прибежала на каблуках, у нее сейчас нет никакого ограничения функций, лишь минимальная симптоматика, выявляемая при неврологическом осмотре, что соответствует 1 баллу по шкале EDSS (эта шкала используется для оценки степени инвалидности пациента, в которой до 4,5 баллов — полностью сохраненная подвижность, выше 7 — глубокая инвалидизация — Прим. ред.). То есть, всё, в том числе ТГСК, надо делать вовремя и по показаниям, и тогда успех будет, ведь при рассеянном склерозе действует простая формула – чем меньше очагов в мозге, то есть чем меньше степень инвалидизации, тем эффективнее лечение, если оно назначено своевременно и целенаправленно.
У тех пациентов, которые трансплантировались в НИИ им. Горбачевой с 6-7 баллами по шкале EDSS, за этот длительный срок неврологический статус увеличился от 0 до 1,5 баллов. Это говорит о том, что противовоспалительная терапия все равно сыграла свою роль, и прогрессия заболевания у большинства из них как минимум затормозилась. Поэтому, помимо гематологической службы, огромного уважения требует и решительность неврологов, которые участвовали в судьбе пациентов, рекомендовали им этот метод лечения.
– Если прежде пациентов с рассеянным склерозом направляли на ТГСК когда лекарственная терапия была уже неэффективна, то как это происходит сейчас?
– Большинство пациентов находят нас сами. Однако без помощи классической неврологии принимать решение о применении ТГСК неправильно. Часто к нам обращаются пациенты, которым только вчера поставили диагноз «рассеянный склероз», кому не подходят ПИТРС из-за нежелательных проявлений или те, кто годами не может получить в своем регионе лекарства. Два года назад к нам обратился пациент из Архангельской области, который стоял 4 года в очереди на получение банального интерферона (1-я линия терапии ПИТРС). Тут метод ТГСК не был методом выбора, по его мнению, он стал единственным выходом из сложившейся ситуации.
Безусловно, общаясь с пациентом, сначала мы пытаемся разъяснить, что существующие в нашей стране принципы помощи пациентам с рассеянным склерозом вполне оправданы, и подчас пациенты длительно находятся на приеме ПИТРС без рецидивов заболевания. Если пациент настаивает, необходима дополнительная диагностика и скрупулезная работа специалистов для определения показаний к использованию метода и исключения других заболеваний, схожих с рассеянным склерозом.
– Вы подчеркиваете, что прежде ТГСК проводилась на «жесткой» химиотерапии. Как ее проводят сегодня?
– Не проводится супервысокодозная химиотерапия, эффект при аутоиммунных болезнях достигается более низкими дозами. То есть, все равно с помощью химиопрепаратов мы «убиваем» аутоиммунные лимфоциты, подавляем причину развития заболевания – патологическую активность иммунитета, поддерживающую воспалительный процесс в мозге, из-за которого поражается миелин – защитная оболочка нейронов. Условно говоря, при ТГСК происходит то же самое, что и при приеме ПИТРС 2-й линии, просто доза лекарства намного выше. Но важно понимать, что зерно рассеянного склероза посеяно не в нервной системе, а по другую сторону гематоэнцефалического барьера, преодолеть который сложно. Но это как раз и дает нам возможность влиять на основную причину, запускающую агрессию по отношению к миелину, – то есть кровь и лимфатическую систему. Другими словами, мы не тушим костер, а перестаем подкладывать в него хворост — сокращаем количество аутоиммунных лимфоцитов и антител в крови.
Поэтому надо понимать, что не трансплантация оказывает основной лечебный эффект, а высокая доза иммуносупрессивного препарата. Поэтому, чтобы не пугать тех, кто застрял в 1990-х, лучше использовать понятие «высокодозная иммуносупрессивная терапия (ВИСТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток – (ВИСТ+АТГСК)». Тем не менее, иммуносупрессия без трансплантации чревата тем, что в определенном проценте случаев костный мозг может не восстановиться, а это высокий риск смертельного исхода: любая иммуносупрессия приводит к тому, что в организме активируются «дремлющие» вирусы. Чтобы этого не произошло, после нее нужна трансплантация стволовых клеток, с помощью которой достигается более быстрое восстановление параметров крови в ответ на подавление иммунитета химиотерапией. Еще одна немаловажная роль непосредственно ТГСК – иммунная реконституция (в простонародье «перезапуск» иммунной системы): мы вводим человеку его собственные гемопоэтические стволовые клетки (CD34+), которые еще не перешли в стадию лимфоцитов.
– А какой смысл при аутоиммунных заболеваниях переливать свои клетки? Организм выработает такие же.
– Мы пока не можем доказать, что рассеянный склероз является генетически обусловленным заболеванием, хотя знаем о потенциальной иммуногенетической предрасположенности к этому заболеванию. Если бы рассматривался вопрос о применении ауто-ТГСК пациенту с «семейной» формой рассеянного склероза, то логики в аутотрансплантации, действительно, было бы меньше. Сейчас мы говорим о важности достижения так называемой иммунной «перезагрузки» с умеренными дозами химиотерапии и с переливанием собственных клеток пациента без серьезных осложнений, например, реакции «трансплантат против хозяина».
– Что должен делать пациент, который хотел бы сделать трансплантацию?
– Все-таки хотелось бы, чтобы мотивация на ее проведение исходила от лечащего врача. Если на всех предыдущих этапах лечения возможности исчерпаны и невролог выносит решение о проведении ТГСК по неврологическим показаниям, то готовность к лечению в гематологическом трансплантационном стационаре (и никак иначе) складывается из отсутствия активной воспалительной и тяжелой сопутствующей патологии.
– Что представляет собой процесс трансплантации? Звучит пугающе.
– После этапа подтверждения диагноза, анализа критериев «за» и «против», подготовки к ТГСК пациент госпитализируется в гематологическое отделение. Там в течение нескольких дней с помощью специальных препаратов стимулируется выход стволовых клеток (CD34+) из костного мозга в периферическую кровь, и они забираются с помощью аппарата для афереза (как при донации крови).
Пока полученные клетки готовятся к трансплантации, у пациента восстанавливается работа костного мозга. На следующем этапе проводится высокодозная иммуносупрессия (введение химиопрепарата), а затем переливание собственных, ранее заготовленных, клеток в вену пациента. Таким образом, это не хирургическая в классическом понимании, а сложная терапевтическая операция. Затем начинается этап восстановления параметров крови, которые изменяются в результате применения химиотерапии. Госпитализация длится в общей сложности не более 30 дней.
– Аутоиммунных заболеваний насчитывается достаточно много, это ведь не только рассеянный склероз, системная красная волчанка, склеродермия, ревматоидный артрит, васкулит, антифосфолипидный синдром и т. д. Предпринимаются ли попытки лечить их таким же способом?
– Действительно, описано уже около 100 аутоиммунных синдромов и болезней. Терапевтические подходы к ним схожи, и в «трансплантационном мире» они активно и эффективно используются. В нашем университете, например, недавно успешно выполнили такое лечение пациенту, страдающему одновременно склеродермией и красной волчанкой. Официально в регистре Европейского сообщества по трансплантации костного мозга (ЕВМТ), куда мы также подаем данные, зарегистрировано более 3000 трансплантаций при аутоиммунных заболеваниях. Более 1300 из них выполнены пациентам с рассеянным склерозом, около 800 – с заболеваниями соединительной ткани, более 220 – при воспалительных заболеваниях кишечника. Установлено, что риск этой процедуры при других тяжелых аутоиммунных заболеваниях выше, поскольку в отличие от рассеянного склероза, при них часто поражаются внутренние органы.
Справка
Первая ТГСК при аутоиммунных заболеваниях в нашей стране была выполнена в НИИ ФКИ в Новосибирске в 1998 году. У истоков ТГСК при рассеянном склерозе также стояли петербургские профессора Андрей Новик и Борис Афанасьев. Первая в России диссертация на эту тему была защищена в 2006 году в ПСПбГМУ им. Павлова. В Петербурге лечение пациентов с рассеянным склерозом изначально проводилось при взаимодействии с неврологами на базе НИИ Детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой, как члена Европейского общества по трансплантации крови и костного мозга (EBMT).
Лечение рассеянного склероза стволовыми клетками
В этом материале пойдет речь о таком широко распространенном заболевании, как рассеянный склероз (РС), а также о том, насколько высокоэффективным может стать лечение рассеянного склероза стволовыми клетками, которое осуществляется в нашем учреждении.
Рассеянный склероз 
Первое описание болезни было составлено неврологом Жаном Мартеном Ширко (Франция) в 1868 году. Рассеянный энцефаломиелит (а именно таково научное название этого недуга) — аутоиммунное прогрессирующее хроническое заболевание нервной системы, протекание которого сопровождается постепенным поражением миелиновой оболочки нервных волокон головного и спинного мозга. Волокна соединяют центры мозга посредством электрических импульсов, ускорение скорости которых и обеспечивает миелин — электролизующее белое вещество липидно-белкового происхождения. Помимо этой функции оболочка выполняет и другую, не менее важную, — миелин изолирует нервные отростки друг от друга.
Причины появления и развития рассеянного склероза
Основным источником развития патологии являются многочисленные вирусы — это краснуха, паротит, герпес, корь, бешенство и ряд других. Проникая в нервные клетки, они живут в них годами, разрушая как сами клетки, так и миелин. Болезнь развивается следующим образом.
- Разрушенные ткани постепенно заменяются прионом — чужеродным белком, играющим роль мощного антигена.
- На его появление и распространение иммунная система человека отвечает мощной аутоиммунной агрессией — происходит выработка антител.
- Последние направляются на уничтожение белого вещества нервных волокон, воспринимая его как чужеродный белок.
В результате иммунная система организма постепенно уничтожает нервную систему. В процессе развития патологии происходит поражение сразу нескольких ее отделов: оболочка постепенно разрушается и в ходе демиелинизации образуются очаги поражения — так называемые бляшки рассеянного склероза. Поскольку очаги поражения имеют рассеянный характер, склероз называется рассеянным. Само слово «склероз» в данном контексте означает «рубец» — это те самые спорадически распространяющиеся рубцы-бляшки (участки соединительной ткани), которые образуются на месте уничтоженных нервных тканей. Размер образований может доходить до нескольких сантиметров и более (если в ходе болезни они сливаются). Активные очаги, находящиеся в стадии образования, называют острыми.
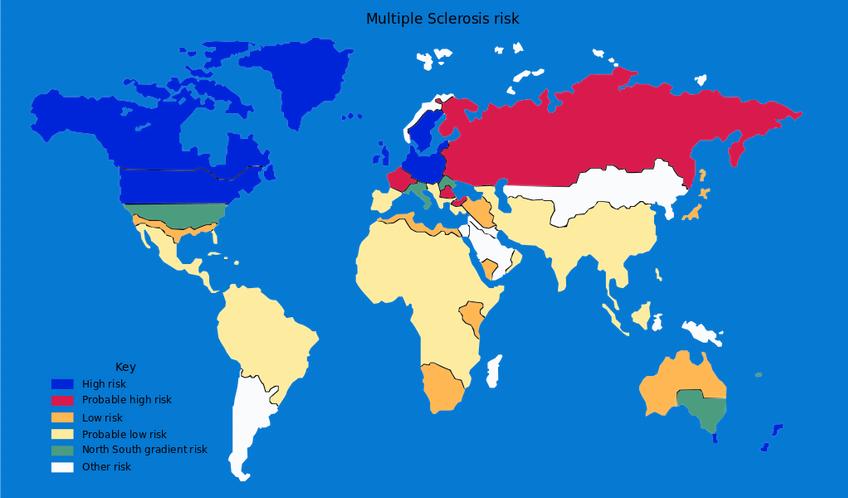
Группы и факторы риска
Темно-синим цветом выделены регионы с высоким риском заболевания РС, красным — с вероятно высоким риском.
Много ранее, задолго до появления технологии лечения рассеянного склероза стволовыми клетками, считалось, что основную группу риска составляют женщины в возрасте от 20 до 40 лет. Современный коллективный портрет больных весьма неоднороден: медики отмечают значительный рост случаев заболевания среди мужчин и женщин старше 40 лет. При этом у мужчин чаще всего протекает неблагоприятная прогрессирующая форма заболевания. Значительно чаще рассеянный склероз встречается сегодня среди европейцев — жителей северных регионов (Скандинавия, Северо-Запад России, Белоруссия). Таким образом, регион проживания сегодня признан одним из факторов риска, обусловливающих возможность появления рассеянного склероза. Помимо этого, в ряду других основных факторов:
- сосудистые заболевания;
- аутоиммунные заболевания;
- нарушенное психоэмоциональное состояние;
- инфекционно-аллергические заболевания;
- генетическая предрасположенность (изменение ферментных показателей, недостаточность Т-супрессоров).
Рассеянный склероз — клинические проявления
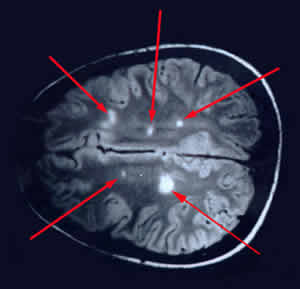
На фото: Бляшки — очаги демиелинизации
Клинические проявления РС — прямое следствие очаговых поражений отделов головного мозга.
Симптоматика рассеянного склероза сложна и разнообразна. В ряду наиболее частых характерных проявлений назовем следующие.
- Нарушения двигательной системы, связанные с поражением мозжечка, — у больного появляются пошатывания при ходьбе, возникает неловкость в движениях, нарушается координация, повышается мышечный тонус в руках. В отдельных случаях возникают парезы, случаются параличи.
- Нарушение зрения — возможно нарушение движения глазного яблока, появление «пелены» перед глазом или черной точки по центру поля зрения, при этом снижение зрения (вплоть до его потери) характерно для одного глаза.
- Нарушение функций тазовых органов — недержание мочи.
- Снижение вкусовой чувствительности.
- Поражение лицевого нерва с ослаблением мышц на одной стороне лица.
- Нарушения психической сферы — неврозоподобные состояния, астенический синдром, депрессия и т.д.
- Быстро наступающая усталость, утомляемость даже после незначительных физических и умственных нагрузок.
Рассеянный склероз — весьма «коварное» заболевание: после появления первых проявлений симптоматика может исчезнуть на довольно длительный срок (даже на 10 — 15 лет), однако впоследствии, при отсутствии лечения болезни, она обязательно даст о себе знать в более тяжелых проявлениях. Кроме того, обострение болезни может быть спровоцировано перегреванием и переохлаждением, ОРВИ и другими заболеваниями, нервно-эмоциональными перегрузками.
Рассеянный склероз по степени тяжести
- Легкий тип: ремитирующее течение РС — обострения редки, периоды ремиссии — длительны.
- Среднее по тяжести течение — ремитирующе-прогрессирующее.
- Тяжелое, прогрессирующее течение (может быть первичным или вторичным).
Рассеянный склероз по форме
Форма рассеянного склероза определяется в зависимости от преобладающих симптомов. Выделяют спинальную, церебральную, глазную, гиперкинетическую, а также атипическую форму РС.
Лечение рассеянного склероза
Этиотропная терапия РС, т.е. лечение, направленное на устранение конкретной причины заболевания, не практикуется в силу невозможности выявить его конкретный возбудитель. Вследствие этого применяется патогенетическая терапия, главными задачами которой являются:
- купирование обострения заболевания с воздействием на очаги аутоиммунного воспаления и одновременной активизацией компенсаторно-приспособительных механизмов;
- предотвращение и уменьшение выраженности обострений;
- симптоматическая терапия по устранению симптомов, негативно сказывающихся на возможности пациента вести привычный образ жизни.
В ходе лечения рассеянного склероза используются плазмаферез, глюкокортикоиды, копаксон, адренокортикотропный гормон, биостимуляторы, витамины группы В и другие препараты.
Лечение РС стволовыми клетками в нашей клинике 
Один из наиболее эффективных методов борьбы с коварным недугом — лечение рассеянного склероза стволовыми клетками. Именно этот прогрессивный и действенный метод заместительной терапии сегодня предлагается в передовых клиниках Санкт-Петербурга. Он обеспечивает:
- восстановление миелина, а вместе с ним — и нормальной скорости передачи нервных импульсов;
- регенерацию клеток головного и спинного мозга на участках нервных тканей, замещенных соединительной рубцовой тканью;
- нормализацию деятельности иммунной системы с прекращением аутоиммунных «атак» с ее стороны на нервную систему организма.
На раннем этапе развития болезни возможно излечение РС благодаря мощному регенеративному потенциалу стволовых клеток. Метод лечения рассеянного склероза стволовыми клетками характеризуется достижением высоких результатов: в каждом из имевших место случаев терапевтического воздействия он обеспечивает стойкую ремиссию. В результате проводимых терапевтических процедур пациенты клиники вновь обретают моторику двигательных функций, возможность полностью обслуживать себя, самостоятельно передвигаться, иными словами — возможность жить полноценной жизнью.
Процедура лечения РС стволовыми клетками
Та или иная методика терапии выбирается в зависимости от формы течения РС и тяжести протекания заболевания. Процедура лечения РС стволовыми клетками осуществляется в несколько этапов.
- На первом выполняются медикаментозные процедуры с использованием уже упомянутых плазмафереза, копаксона и других препаратов — в зависимости от формы рассеянного склероза, специфики протекания заболевания и других факторов. Основная задача на первом этапе процедур — приостановление процесса разрушения миелина и купирование иммуновоспалительного процесса.
- На втором, третьем, а при необходимости и на четвертом этапе лечения рассеянного склероза осуществляется трансплантация стволовых клеток. Это собственные мезенхимальные стволовые клетки, выделенные из биоматериалов пациента — костного мозга и жировой ткани.
Процедуры трансплантации осуществляются с месячным интервалом. Как правило, в ходе одной процедуры в кровь пациента вводятся клетки в количестве из расчета 1 млн на 1 кг тела пациента (например, для пациента с массой тела 70 кг необходимо введение 70 млн клеток). Уже в течение короткого времени организм больного демонстрирует первые признаки улучшения, связанные с нормализацией приема и передачи нервных импульсов и восстановления популяции нейронов.
- Через 1,5-2 месяца улучшается ситуация с удержанием равновесия, происходит восстановление чувствительности, улучшается психологическое состояние.
- В течение 3-4 месяцев нормализуется походка, восстанавливается память, исчезает двоение в глазах.
- В течение года прекращается образование новых зон демиелинизации и появление новых рубцов.
Наступает стойкая ремиссия. Исчезает неврологическое расстройство, восстанавливается память, преодолеваются симптомы хронической усталости. Полностью восстанавливается работа речевого аппарата. Достигнутый терапевтический эффект может длиться годами, в зависимости от образа жизни пациента (отсутствие вредных привычек и т.д.). Человек обретает возможность полноценной жизни в социуме.