Эритропоэз — как происходит образование эритроцитов крови?
Эритропоэз — процесс образования эритроцитов в костном мозге. Первой клеткой эритроидного ряда, образующейся из колониеобразующей клетки эритроцитарной (КОК-Э) — клетки-предшественницы эритроидного ряда, является проэритробласт, из которого в ходе 4—5 последующих удвоений и созревания образуется 16—32 зрелых эритроцита.

Схема процесса: 1 проэритробласт (удвоение) => два базофильных эритробласта I порядка => 4 базофильных эритробласта II порядка => 8 полихроматофильных эритробластов I порядка => 16 полихроматофильных эритробластов II порядка => 32 полихроматофильных нормобласта =>
32 оксифильных нормобласта => денуклеация нормобластов => 32 ретикулоцита => 32 эритроцита.
Эритропоэз до формирования ретикулоцита занимает 5 дней.
Эритропоэз у человека и животных (от проэритробласта до ретикулоцита) протекает в эритробластических островках костного мозга, которых в норме содержится до 137 на 1 мг ткани костного мозга. Макрофаги эритроцитарных островков играют основную роль в физиологии эритроидных клеток, влияя на их пролиферацию и созревание.
Макрофаги фагоцитируют вытолкнутые из нормобластов ядра, обеспечивают эритробласты ферритином и пластическими веществами, секретируют эритропоэтин и гликозаминогликаны, последние повышают концентрацию ростковых факторов в островках. Эти благоприятные условия для развития эрит-робластов макрофаги создают благодаря наличию рецепторов к эритроидным клеткам-предшественницам.
Из костного мозга ретикулоциты выходят в кровь и в течение суток созревают в эритроциты. По количеству ретикулоцитов в крови судят об эритроцитарной продукции костного мозга и интенсивности эритропоэза. У человека их количество составляет 5— 10%о. За сутки в 1 мкл крови поступает 60—80 тыс. эритроцитов.
В 1 мкл крови у мужчин содержится 5,21 (4,52—5,9) млн, а у женщин — 4,6 (4,1—5,1) млн эритроцитов.
Уменьшение количества эритроцитов в единице объема крови называется анемией, увеличение — эритроцитозом.
Последний может носить физиологический, приспособленный для организма человека характер (например, при подъеме человека в горы, на высоту более 3000 м над уровнем моря).
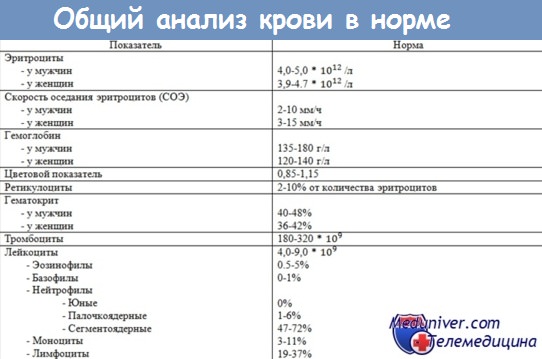 Общий анализ крови в норме
Общий анализ крови в норме
Эритропоэз — как происходит образование эритроцитов крови?
Основной функцией эритроцитов является перенос кислорода из лёгких к тканям тела, и транспорт диоксида углерода (углекислого газа) в обратном направлении.
Однако, кроме участия в процессе дыхания, они выполняют в организме также следующие функции:
- участвуют в регулировке кислотно-щелочного равновесия;
- поддерживают изотонию крови и тканей;
- адсорбируют из плазмы крови аминокислоты, липиды и переносят их к тканям.
Формирование эритроцитов
Формирование эритроцитов (эритропоэз) происходит в костном мозге черепа, ребер и позвоночника, а у детей — еще и в костном мозге в окончаниях длинных костей рук и ног. Продолжительность жизни – 3-4 месяца, разрушение (гемолиз) происходит в печени и селезенке. Прежде чем выйти в кровь, эритроциты последовательно проходят несколько стадий пролиферации и дифференцировки в составе эритрона — красного ростка кроветворения.
а) Из стволовых гемопоэтических клеток сначала появляется большая клетка с ядром, не обладающая характерным красным цветом — мегалобласт
б) Затем она окрашивается в красный цвет — теперь это эритробласт
в) уменьшается в размере в процессе развития — теперь это нормоцит
г) утрачивает ядро — теперь это ретикулоцит. У птиц, пресмыкающихся, земноводных и рыб ядро просто теряет активность, но сохраняет способность реактивации. Одновременно с исчезновением ядра по мере взросления эритроцита из его цитоплазмы исчезают рибосомы и другие компоненты, участвующие в синтезе белка.
Ретикулоциты попадают в кровеносную систему и через несколько часов становятся полноценными эритроцитами.
Структура и состав
Обычно эритроциты имеют форму двояковогнутого диска и содержат в основном дыхательный пигмент гемоглобин. У некоторых животных (например, верблюда, лягушки) эритроциты имеют овальную форму.
Содержимое эритроцита представлено главным образом дыхательным пигментом гемоглобином, обусловливающим красный цвет крови. Однако на ранних стадиях количество гемоглобина в них мало, и на стадии эритробластов цвет клетки синий; позже клетка становится серой и, лишь полностью созрев, приобретает красную окраску.
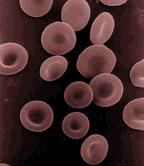
Важную роль в эритроците выполняет клеточная (плазматическая) мембрана, пропускающая газы (кислород, углекислый газ), ионы (Na, K) и воду. Плазмолемму пронизывают трансмембранные белки – гликофорины, которые, благодаря большому количеству остатков сиаловой кислоты, ответственны примерно за 60% отрицательного заряда на поверхности эритроцитов.
На поверхности липопротеидной мембраны находятся специфические антигены гликопротеидной природы — агглютиногены — факторы систем групп крови (на данный момент изучено более 15 систем групп крови: AB0, резус фактор, Даффи, Келл, Кидд), обусловливающие агглютинацию эритроцитов.
Эффективность функционирования гемоглобина зависит от величины поверхности соприкосновения эритроцита со средой. Суммарная поверхность всех эритроцитов крови в организме тем больше, чем меньше их размеры. У низших позвоночных эритроциты крупные (например, у хвостатого земноводного амфиумы — 70 мкм в диаметре), эритроциты высших позвоночных мельче (например, у козы — 4 мкм в диаметре). У человека диаметр эритроцита составляет 7,2—7,5 мкм, толщина — 2 мкм, объём — 88 мкм³.
Переливание крови
При переливании крови от донора к реципиенту возможна агглютинация(склеивание) и гемолиз(разрушение) эритроцитов. Чтобы этого не происходило стоит учитывать группы крови, открытые К. Ландштейнером и Я. Янским в 1900 г. Агглютинацию вызывают белки, находящиеся на поверхности эритроцита, – антигены (агглютиногены) и находящиеся в плазме антитела (агглютинины). Существуют 4 группы крови, для каждой характерны различные антигены и антитела. Переливание возможно лишь между представителями одной группы крови. Но например, I группа крови(0) является универсальным донором, а IV(AB) – универсальным реципиентом.
| I – 0 | II – A | III – B | IV – AB |
|---|---|---|---|
| αβ | β | α | — |
Место в организме
Форма двояковогнутого диска обеспечивает прохождение эритроцитов через узкие просветы капилляров. В капиллярах они движутся со скоростью 2 сантиметра в минуту, что дает им время передать кислород от гемоглобина к миоглобину. Миоглобин действует как посредник, принимая кислород у гемоглобина в крови и передавая его цитохромам в мышечных клетках.
Количество эритроцитов в крови в норме поддерживается на постоянном уровне (у человека в 1 мм³ крови 4,5—5 млн эритроцитов, у некоторых копытных 15,4 млн (лама) и 13 млн (коза) эритроцитов, у пресмыкающихся — от 500 тыс. до 1,65 млн, у хрящевых рыб — 90—130 тыс.) Общее число эритроцитов снижается при анемиях, повышается при полицитемии.
Продолжительность жизни эритроцита человека в среднем 125 суток (ежесекундно образуется около 2,5 млн эритроцитов и такое же их количество разрушается). У собак — 107 дней, у кроликов и кошек — 68.
Патология
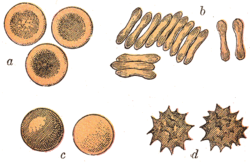
При различных заболеваниях крови возможно изменение цвета эритроцитов, их размеров, количества, а также формы; они могут принимать, например, серповидную, овальную или мишеневидную форму.
При изменении кислотно-щелочного баланса крови в сторону закисления (от 7.43 до 7.33) происходит склеивание эритроцитов в виде монетных столбиков, либо их агрегация.
Среднее содержание гемоглобина для мужчин 13,3—18 г% (или 4,0-5,0*10 12 единиц), для женщин 11,7—15,8г% (или 3,9-4,7*10 12 единиц). Единица измерения уровня гемоглобина, представляет собой процент содержания гемоглобина в 1 грамме эритроцитарной массы.
Образование эритроцитов и регуляция эритропоэза
Локальныерегуляторные механизмы представлены комплексом клеточных, экстрацеллюлярных и гуморальных факторов, расположенных в непосредственной близости к гемопоэтическим элементам и носящих название кроветворного или гемопоэзиндуцирующего микроокружения (ГИМ).
Понятие о гемопоэзе
РЕГУЛЯЦИЯ ЭРИТРОПОЭЗА
Гемопоэз – процесс, заключающийся в серии клеточных дифференцировок, которые приводят к образованию зрелых клеток периферической крови. Основной функциональной чертой гемопоэза является продукция огромного количества клеточных элементов в единицу времени, что объясняется гибелью соответствующего числа клеток крови в процессе жизнедеятельности.
Образование форменных элементов крови (гемоцитопоэз) осуществляется в специализированных гемопоэтических тканях: миелоидной(в эпифизах трубчатых и полости многих губчатых костей) и лимфоидной (тимус, селезенка, лимфатические узлы). В миелоидной ткани образуются эритроциты, гранулоциты, моноциты, тромбоциты, предшественники лимфоцитов. В лимфоидной ткани происходит образование лимфоцитов, плазматических клеток, а также процессы элиминации клеток крови и продуктов их распада.
Различают два периода кроветворения: эмбриональныйи постнатальный. Эмбриональное кроветворение происходит в период внутриутробного развития, постнатальное – после рождения ребенка.
По современным представлениям единой материнской клеткой кроветворения является стволовая клетка, из которой образуются через ряд промежуточных стадий все виды форменных элементов крови, причем эритроциты образуются интраваскулярно (внутри сосуда) в синусах красного костного мозга, а лейкоциты – экстраваскулярно.
Образование форменных элементов крови происходит под влиянием системных и местных (локальных) регуляторных механизмов.
Системныерегуляторные механизмы осуществляются за счет нервной системы (гипоталамическая область головного мозга, вегетативная нервная система – ее симпатический и парасимпатический отделы) и гуморальныхфакторов – экзогенных и эндогенных. К экзогенным факторам относят витамины, микроэлементы, к эндогенным – гормоны, гемопоэтины. Гемопоэтины -образующиеся в организме вещества, стимулирующие гемопоэз.
Согласно современным представлениям в формировании гемопоэзиндуцирующего микроокружения принимают участие различные клеточные элементы и продукты их жизнедеятельности, входящие в состав как стромы, так и паренхимы кроветворных органов. К компонентам ГИМ следует в первую очередь отнести отдельные субпопуляции Т-лимфоцитов и макрофагов, фибробласты с продуцируемыми ими компонентами экстраклеточного матрикса, жировые и эндотелиальные клетки, элементы микроциркуляторного русла.
Компоненты ГИМ осуществляют контроль за процессами кроветворения как через продуцируемые цитокины, так и благодаря непосредственным контактом с гемопоэтическими клетками. Такой контроль может быть как положительным, так и отрицательным (блокирование пролиферации и дифференцировки) в зависимости от субпопуляции клетки ГИМ и их функционального состояния.
По времени действия различают две группы гемопоэтинов.
К раннедействуюшим гемопоэтинам относят интерлейкин-3, вырабатываемый активированными Т-лимфоцитами, интерлейкин-1 и интерлейкнн-6, образуемые макрофагами, стромальными, эндотелиальными и жировыми клетками, а также гранулоцитарно-макрофагальный колониестимулирующий фактор, который образуется практически всеми клеточными элементами гемопоэзиндуцирующего микроокружения.
К поздно действующим гемопоэтинам относятся гранулоцитарный и макрофагальный колониестимулирующий факторы, участвующие в регуляции соответственно грануло- и моноцитопоэза. Они образуются макрофагами, фибробластами и эндотелиальными клетками. Кроме того, клетки стромы и макрофаги вырабатывают коллаген 1, II и IV типов, ретикулярные волокна, фибронектин и другие белковые компоненты внеклеточного матрикса, который обеспечивает концентрацию гемопоэтических ростовых факторов и модуляцию их функций. Следовательно, основное вещество соединительной ткани костного мозга является физиологически активной средой, что дает основание рассматривать ее в качестве важнейшего регулятора кроветворения.
Эритроциты образуются в кроветворных тканях – желточном мешке у эмбриона, печени и селезенке у плода и красном костном мозге плоских костей у взрослого человека. Во всех этих органах содержатся так называемые плюрипотентные стволовые клетки — общие предшественники всех клеток крови.
Этапы созревания эритроцитов: стволовая клетка → базофильный проэритробласт → эритробласт (макробласт) → нормобласт → ретикулоцит → ретикулоцит ІІІ → ретикулоцит IV → эритроцит.
Эритропоэз – это процесс образования эритроцитов в организме, который связан с понятием эритрон. Эритрон – система красной крови, включающая периферическую кровь, органы эритропоэза и эритроциторазрушения. Эритрон включает в себя 4 категории клеток:
1)ядросодержащие эритроидные клетки костного мозга – эритрокариоциты;
2)ретикулоциты костного мозга;
3)ретикулоциты крови;
4)зрелые эритроциты периферической крови.
В костном мозге находится лишь 6% клеток эритрона, в циркулирующей крови – 94 %. Поддержание постоянного количества эритроцитов периферической крови, имеющих продолжительность жизни около 120 дней, возможно лишь при достаточно высокой скорости эритропоэза. Популяция циркулирующих эритроцитов в норме составляет 25×10 12 и содержит около 750 г гемоглобина.
Для поддержания постоянства содержания эритроцитов в периферической крови в костном мозге здорового человека массой 70 кг ежесуточно образуется примерно 20-25×10 эритроцитов, а из костного мозга в кровь освобождается в 1мин примерно 1,8х10 9 молодых эритроцитов (ретикулоцитов). В условиях патологии, при чрезвычайной стимуляции гемопоэза (гипоксия, гемолиз эритроцитов, кровопотеря), интенсивность эритропоэза может возрастать в 6-8 раз.
Важнейшим регулятором эритропоэза является эритропоэтин. По физико-химическим свойствам эритропоэтин относится к группе кислых гликопротеинов. Биологическая активность эритропоэтина в значительной мере обусловлена наличием в молекуле остатков тирозина, триптофана, а также сиаловой кислоты.
Человеческий эритропоэтин представляет собой димер с молекулярной массой от 46 000 до 50 000-60 000 Д.
Установлен химический состав высокоочишенных препаратов почечного эритропоэтина: содержание белка в нем составляет около 65,5%, углеводов – около 30%.
Считают, что основным местом синтеза эритропоэтина являются почки. Местом образования почечного эритропоэтина является юкстагломерулярный аппарат (ЮГА) почек. Есть работы, доказывающие канальцевое происхождение эритропоэтина. Почечный эритропоэтин называют иногда эритрогенином. В небольших концентрациях он вырабатывается печенью и слюнными железами. Эритропоэтин обнаруживается в плазме крови здоровых людей. Выделяется эритропоэтин с мочой, а также в составе слюны и желудочного сока.
В процессе взаимодействия почечного эритрогенина со специализированными белками плазмы крови α-глобулинами, вырабатываемыми в печени, образуется активная форма эритропоэтина.
Останавливаясь на молекулярных механизмах действия эритропоэтина, необходимо отметить, что для него характерен мембранный тип рецепции эритропоэтинчувствительными клетками. Вторичным сигналом, который возникает при взаимодействии эритропоэтина с рецепторами клеточной мембраны и действует на ядро, является изменение внутриклеточных концентраций циклических нуклеотидов, ионов калия и кальция.
Основным стимулятором образования эритропоэтина является гипоксия различного происхождения (при сердечной, легочной недостаточности, кровопотере, гемолизе эритроцитов, снижении барометрического давления). Можно выделить несколько механизмов стимуляции продукции эритропоэтина в условиях гипоксии (рис. ):
1. Прямое воздействие крови с пониженным парциальным напряжением О2 на клетки ЮГА и канальцевый аппарат, продуцирующие эритропоэтин.
2. Опосредованный эффект через активацию гипоталамо-гипофизарно-надпочечниковой системы в условиях гипоксии, усиление выброса гормонов адаптации – глюкокортикоидов, катехоламинов, стимулирующих гуморальным путем образование эритропоэтина в почках и усиление процессов эри-тропоэза в костном мозге.

Рис. 3. Схема влияния гипоксии на образование эритропоэтина
Изменение снабжения организма кислородом в ту или иную сторону от нормального параметра включает гуморальные механизмы регуляции эритропоэза, направленные на восстановление этого параметра. При недостатке кислорода вырабатывается эритропоэтин, стимулирующий эритропоэз, а при избытке – ингибитор эритропоэза, снижающий уровень последнего. У взрослого человека в более широком диапазоне проявляются эритропоэзстимулирующие реакции, в раннем возрасте — эритропоэзтормозящие.
Синтез эритропоэтина контролируется рефлекторным механизмом: хеморецепторы каротидного синуса → гипоталамус → спинной мозг → симпатические нервы почек. У животных с выключением любого отдела рефлекторной дуги стимуляция эритропоэза при гипоксии сохраняется, но запаздывает в развитии. Таким образом, эта стимуляция имеет сложный нервно-гуморальный механизм, где центральное место занимает эритропоэтин, скорость включения которого обеспечивает нервная система.
Важнейшими модуляторами эритропоэза являются гормоны. Тропные гормоны аденогипофиза (АКТГ, ТТГ, ГТГ) оказывают стимулирующее воздействие на эритропоэз за счет усиления продукции соответствующих гормонов периферическими эндокринными железами: глюкокортикоидов, тироксина, трийодтиронина, андрогенов. Стимулирующим воздействием на эритропоэз обладает и соматотропин. Очевидно, что главным механизмом действия гипофизарных гормонов на эритропоэз является модуляция продукции и секреции эритропоэтина в почках. Стимуляция эритропоэза после введения гипофизарных гормонов и гормонов периферических желез может быть связана с повышением утилизации О2 в тканях и возникновением его дефицита в почках.
Стимулирующимвоздействием на эритропоэз обладает гипофизарный и плацентарный пролактин, обеспечивая стимуляцию эритропоэза во время беременности.
Тиреоидные гормоны оказывают стимулирующее воздействие на эритропоэз не только путем повышения почечной продукции эритропоэтина, но и путем прямого действия на эритропоэтинчувствительные клетки, реализуемым через b2-адренорецепторы.
В отличие от андрогенов эстрогены оказывают тормозящее влияние на эритропоэз.
В последние годы появились работы, свидетельствующие о возможном участии гормонов поджелудочной железы в регуляции эритропоэза. Установлено, что инсулин в больших фармакологических концентрациях стимулирует образование эритропоэтина. В противоположность действию инсулина глюкагоноказывает ингибирующее влияние на эритропоэз.
Регуляторами эритропоэза, наряду с гормонами, являются витамины и микроэлементы. Микроэлементы железа, меди, марганца и цинка необходимы для: а) созревания эритробластов, дифференцировки их в нормоциты; б) для синтеза гема и глобина (железо, кобальт, медь); в) стимуляции образования эритропоэтинов (кобальт); г) повышения обмена веществ в кроветворных органах, усиления насыщения эритроцитов гемоглобином (марганец). Однако чрезмерные концентрации марганца в организме затрудняют всасывание железа, приводят к развитию анемии. Недостаток содержания меди в организме вызывает развитие микроцитарной нормохромной анемии. Цинк, как известно, входит в состав различных гормонов (инсулина, половых гормонов, гормонов гипофиза), витаминов и в соответствии с этим также является одним из важнейших регуляторов эритропоэза.
| | | следующая лекция ==> | |
| Поступление железа в организм и синтез гемоглобина | | | Вычисление объема тела по площадям параллельных сечений |
Дата добавления: 2014-01-20 ; Просмотров: 2112 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Эритропоэз
Образование эритроцитов, или эритропоэз, происходит в красном костном мозге. Эритроциты вместе с кроветворной тканью носят название «красного ростка крови», или эритрона.
Для образования эритроцитов требуются железо и ряд витаминов.
Железо организм получает из гемоглобина разрушающихся эритроцитов и с пищей. Трехвалентное железо пищи с помощью вещества, находящегося в слизистой кишечника, превращается в двухвалентное железо. С помощью белка трансферрина железо всосавшись, транспортируется плазмой в костный мозг, где оно включается в молекулу гемоглобина. Избыток железа депонируется в печени в виде соединения с белком — ферритина или с белком и липоидом — гемосидерина. При недостатке железа развивается железодефицитная анемия.
Для образования эритроцитов требуются витамин В12(циано-кобаламин) и фолиевая кислота. Витамин В12 поступает в организм с пищей и называется внешним фактором кроветворения. Для его всасывания необходимо вещество (гастромукопротеид), которое вырабатывается железами слизистой оболочки пилорического отдела желудка и носит название внутреннего фактора кроветворения Касла. При недостатке витамина В12 развивается В12-дефицитная анемия. Это может быть или при недостаточном его поступлении с пищей (печень, мясо, яйца, дрожжи, отруби), или при отсутствии внутреннего фактора (резекция нижней трети желудка). Считается, что витамин В12 способствует синтезу глобина. Витамин В12 и фолиевая кислота участвуют в синтезе ДНК в ядерных формах эритроцитов. Витамин В12 (рибофлавин) необходим для образования липидной стромы эритроцитов. Витамин В2 (пиридоксин) участвует в образовании гема. Витамин С стимулирует всасывание железа из кишечника, усиливает действие фолиевой кислоты. Витамин Е (а-токоферол) и витамин РР (пантотеновая кислота) укрепляют липидную оболочку эритроцитов, защищая их от гемолиза.
Для нормального эритропоэза необходимы микроэлементы. Медь помогает всасыванию железа в кишечнике и способствует включению железа в структуру гема. Никель и кобальт участвуют в синтезе гемоглобина и гемсодержащих молекул, утилизирующих железо. В организме 75% цинка находится в эритроцитах в составе фермента карбоангидразы. Недостаток цинка вызывает лейкопению. Селен, взаимодействуя с витамином Е, защищает мембрану эритроцита от повреждения свободными радикалами.
Физиологическими регуляторами эритропоэза являются эри-тропоэтины, образующиеся главным образом в почках, а также в печени, селезенке и в небольших количествах постоянно присутствующие в плазме крови здоровых людей. Эритропоэтины усиливают пролиферацию клеток-предшественников эритроидного ряда — КОЕ-Э (колониеобразующая единица эритроцитар-ная) и ускоряют синтез гемоглобина. Они стимулируют синтез информационной РНК, необходимой для образования энзимов,
пторые участвуют в формировании гема и глобина. Эритропоэтины увеличивают также кровоток в сосудах кроветворной ткани
увеличивают выход в кровь ретикулоцитов. Продукция эритро-поэтинов стимулируется при гипоксии различного происхождения: пребывание человека в горах, кровопотеря, анемия, заболевания сердца и легких. Эритропоэз активируется мужскими половыми гормонами, что обусловливает большее содержание эритроцитов в крови у мужчин, чем у женщин. Стимуляторами эритропоэза являются соматотропный гормон, тироксин, катехоламины, интерлейкины. Торможение эритропоэза вызывают особые вещества — ингибиторы эритропоэза, образующиеся при увеличении массы циркулирующих эритроцитов, например у спустившихся с гор людей. Тормозят эритропоэз женские половые гормоны (эстрогены), кейлоны. Симпатическая нервная система активирует эритропоэз, парасимпатическая — тормозит. Нервные и эндокринные влияния на эритропоэз осуществляются, по-видимому, через эритропоэтины.
Об интенсивности эритропоэза судят по числу ретикулоцитов — предшественников эритроцитов. В норме их количество составляет 1 — 2%. Созревшие эритроциты циркулируют в крови в течение 100—120 дней.
Разрушение эритроцитов происходит в печени, селезенке, в костном мозге посредством клеток мононуклеарной фагоцитарной системы. Продукты распада эритроцитов также являются стимуляторами кроветворения.
Эритроциты – их образование, строение и функции
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Кровь – это жидкая соединительная ткань, которая наполняет всю сердечно-сосудистую систему человека. Ее количество в организме взрослого человека достигает 5 литров. Она состоит из жидкой части под названием плазма и таких форменных элементов как лейкоциты, тромбоциты и эритроциты. В данной статье мы поговорим именно об эритроцитах, их строении, функциях, способе образования и т.д.
Что представляют собой эритроциты?
Данный термин произошел от 2-ух слов «erythos» и «kytos», что в переводе с греческого языка означает «красный» и «вместилище, клетка». Эритроциты представляют собой красные кровяные тельца крови человека, позвоночных, а также некоторых беспозвоночных животных, на которые возложены весьма разнообразные очень важные функции.
Образование красных клеток
Образование данных клеток осуществляется в красном костном мозге. Первоначально происходит процесс пролиферации (разрастания ткани путем размножения клетки). Затем из стволовых гемопоэтических клеток (клеток – родоначальниц кроветворения) формируется мегалобласт (крупное красное тельце, содержащее ядро и большое количество гемоглобина), из которого в свою очередь образуется эритробласт (ядросодержащая клетка), а потом и нормоцит (тельце, наделенное нормальными размерами). Как только нормоцит утрачивает свое ядро, он тут же превращается в ретикулоцит – непосредственного предшественника красных кровяных клеток. Ретикулоцит попадает в кровеносное русло и трансформируется в эритроцит. На его трансформацию уходит около 2 – 3 часов.
Строение
Данным кровяным тельцам присуща двояковогнутая форма и красный окрас, обусловленный наличием в клетке большого количества гемоглобина. Именно гемоглобин составляет основную часть данных клеток. Их диаметр варьирует в пределах от 7 до 8 мкм, а вот толщина достигает 2 – 2,5 мкм. Ядро в созревших клетках отсутствует, что значительно увеличивает их поверхность. Помимо этого отсутствие ядра обеспечивает быстрое и равномерное проникновение внутрь тельца кислорода. Продолжительность жизни данных клеток составляет около 120 дней. Общая поверхность красных кровяных клеток человека превышает 3000 квадратных метров. Данная поверхность в 1500 раз больше поверхности всего человеческого тела. Если разместить все красные клетки человека в один ряд, то Вы сможете получить цепочку, длина которой будет составлять около 150000 км. Разрушение данных телец происходит преимущественно в селезенке и частично в печени.
Функции
2. Ферментативная: являются носителями различных ферментов (специфических белковых катализаторов);
3. Дыхательная: данная функция осуществляется гемоглобином, который способен присоединять к себе и отдавать как кислород, так и углекислый газ;
4. Защитная: связывают токсины за счет присутствия на их поверхности специальных веществ белкового происхождения.
Термины, применяемые для описания данных клеток
- Микроцитоз – средний размер красных кровяных клеток меньше нормального;
- Макроцитоз – средний размер красных кровяных клеток больше нормального;
- Нормоцитоз – средний размер красных кровяных клеток нормальный;
- Анизоцитоз – размеры красных кровяных клеток значительно отличаются, одни чересчур маленькие, другие очень большие;
- Пойкилоцитоз – форма клеток варьирует от правильной до овальной, серповидной;
- Нормохромия – красные кровяные тельца окрашены нормально, что является признаком нормального уровня в них гемоглобина;
- Гипохромия – красные кровяные клетки окрашены слабо, что указывает на то, что гемоглобина в них меньше нормы.
Скорость оседания (СОЭ)
Скорость оседания эритроцитов или СОЭ – это достаточно известный показатель лабораторной диагностики, под которым подразумевается скорость разделения несвернувшейся крови, которую помещают в специальный капилляр. Кровь разделяется на 2 слоя – нижний и верхний. Нижний слой состоит из осевших красных кровяных телец, а вот верхний слой представлен плазмой. Данный показатель принято измерять в миллиметрах в час. Величина СОЭ напрямую зависит от пола пациента. В нормальном состоянии у мужчин данный показатель составляет от 1 до 10 мм/час, а вот у женщин – от 2 до 15 мм/час.
При повышении показателей речь идет о нарушениях работы организма. Существует мнение, что в большинстве случаев СОЭ повышается на фоне увеличения соотношения в плазме крови белковых частиц крупных и мелких размеров. Как только в организм попадают грибки, вирусы либо бактерии, уровень защитных антител тут же возрастает, что и приводит к изменениям соотношения белков крови. Из этого следует, что особенно часто СОЭ увеличивается на фоне воспалительных процессов таких как воспаление суставов, ангина, воспаление легких и т.д. Чем выше данный показатель, тем ярче выражен воспалительный процесс. При легком течении воспаления показатель возрастает до 15 – 20 мм/час. Если же воспалительный процесс является тяжелым, тогда он подскакивает до 60 – 80 мм/час. Если во время курса терапии показатель начинает снижаться, значит, лечение было подобрано правильно.
Помимо воспалительных заболеваний увеличение показателя СОЭ возможно и при некоторых недугах невоспалительного характера, а именно:
- Злокачественные образования;
- Инсульт либо инфаркт миокарда;
- Тяжелые недуги печени и почек;
- Тяжелые патологии крови;
- Частые переливания крови;
- Вакцинотерапия.
Нередко показатель повышается и во время менструаций, а также в период беременности. Использование некоторых медикаментов также может спровоцировать увеличение СОЭ.
Гемолиз – что это такое?
Гемолиз представляет собой процесс разрушения мембраны красных кровяных клеток, вследствие чего гемоглобин выходит в плазму и кровь становится прозрачной.
Современные специалисты выделяют следующие виды гемолиза:
1. По характеру течения:
- Физиологический: происходит разрушение старых и патологических форм красных клеток. Процесс их разрушения отмечается в мелких сосудах, макрофагах (клетках мезенхимного происхождения) костного мозга и селезенки, а также в клетках печени;
- Патологический: на фоне патологического состояния разрушению подвергаются здоровые молодые клетки.
2. По месту возникновения:
- Эндогенный: гемолиз происходит внутри организма человека;
- Экзогенный: гемолиз осуществляется вне организма (к примеру, во флаконе с кровью).
3. По механизму возникновения:
- Механический: отмечается при механических разрывах мембраны (к примеру, флакон с кровью пришлось встряхнуть);
- Химический: отмечается при воздействии на эритроциты веществ, которым свойственно растворять липиды (жироподобные вещества) мембраны. К числу таких веществ можно отнести эфир, щелочи, кислоты, спирты и хлороформ;
- Биологический: отмечается при воздействии биологических факторов (ядов насекомых, змей, бактерий) либо при переливании несовместимой крови;
- Температурный: при низких температурах в красных кровяных тельцах формируются кристаллики льда, которым свойственно разрывать оболочку клеток;
- Осмотический: происходит тогда, когда красные кровяные тельца попадают в среду с более низким чем у крови осмотическим (термодинамическим) давлением. При таком давлении клетки набухают и лопаются.
Эритроциты в крови
Норма содержания красных кровяных телец
Определить уровень данных клеток помогает клинический (общий) анализ крови.
- У женщин – от 3.7 до 4.7 триллионов в 1 л;
- У мужчин – от 4 до 5.1 триллионов в 1 л;
- У детей старше 13 лет – от 3.6 до 5.1 триллионов в 1 л;
- У детей в возрасте от 1 года до 12 лет – от 3.5 до 4.7 триллионов в 1 л;
- У детей в 1 год – от 3.6 до 4.9 триллионов в 1 л;
- У детей в полгода – от 3.5 до 4.8 триллионов в 1 л;
- У детей в 1 месяц – от 3.8 до 5.6 триллионов в 1 л;
- У детей в первый день их жизни – от 4.3 до 7.6 триллионов в 1 л.
Высокий уровень клеток в крови новорожденных обусловлен тем, что во время внутриутробного развития их организм нуждается в большем количестве красных кровяных телец. Только так плод может получать необходимое ему количество кислорода в условиях относительно низкой его концентрации в крови матери.
Уровень эритроцитов в крови беременных
Чаще всего количество данных телец во время беременности слегка понижается, что является совершенно нормальным явлением. Во-первых, во время вынашивания плода в организме женщины задерживается большое количество воды, которая попадает в кровь и разбавляет ее. Кроме этого организмы практически всех будущих мамочек не получают достаточное количество железа, вследствие чего формирование данных клеток опять таки уменьшается.
Повышение уровня эритроцитов в крови
Состояние, характеризующееся повышением уровня красных кровяных клеток в крови, именуют эритремией, эритроцитозом или полицитемией.
Самыми частыми причинами развития данного состояния являются:
- Поликистоз почек (заболевание, при котором в обеих почках появляются и постепенно увеличиваются кисты);
- ХОБЛ (хронические обструктивные болезни легких – бронхиальная астма, эмфизема легких, хронические бронхиты);
- Синдром Пиквика (ожирение, сопровождающееся легочной недостаточностью и артериальной гипертензией, т.е. стойким повышением артериального давления);
- Гидронефроз (стойкое прогрессирующее расширение почечной лоханки и чашечек на фоне нарушения оттока мочи);
- Курс терапии стероидами;
- Врожденные либо приобретенные пороки сердца;
- Пребывание в высокогорных районах;
- Стеноз (сужение) почечных артерий;
- Злокачественные новообразования;
- Синдром Кушинга (совокупность симптомов, которые возникают при чрезмерном увеличении количества стероидных гормонов надпочечников, в частности кортизола);
- Длительное голодание;
- Чрезмерные физические нагрузки.
Понижение уровня эритроцитов в крови
 Состояние, при котором уровень красных кровяных клеток в крови понижается, получило название эритроцитопения. В данном случае речь идет о развитии анемии различной этиологии. Малокровие может развиться вследствие нехватки как белка, так и витаминов, а также железа. Оно же может быть следствием злокачественных новообразований либо миеломы (опухоли из элементов костного мозга). Физиологическое понижение уровня данных клеток возможно в периоды между 17.00 и 7.00, после приема пищи и при взятии крови в положении лежа. О других причинах понижения уровня данных клеток Вы сможете узнать, получив консультацию специалиста.
Состояние, при котором уровень красных кровяных клеток в крови понижается, получило название эритроцитопения. В данном случае речь идет о развитии анемии различной этиологии. Малокровие может развиться вследствие нехватки как белка, так и витаминов, а также железа. Оно же может быть следствием злокачественных новообразований либо миеломы (опухоли из элементов костного мозга). Физиологическое понижение уровня данных клеток возможно в периоды между 17.00 и 7.00, после приема пищи и при взятии крови в положении лежа. О других причинах понижения уровня данных клеток Вы сможете узнать, получив консультацию специалиста.
Эритроциты в моче
В норме красных кровяных телец в моче быть не должно. Допускается их присутствие в виде единичных клеток в поле зрения микроскопа. Находясь в осадке мочи в очень маленьких количествах, они могут указывать на то, что человек занимался спортом либо выполнял тяжелую физическую работу. У женщин их незначительное количество может наблюдаться при гинекологических недугах, а также во время менструации.
Значительное повышение их уровня в моче можно заметить сразу же, так как моча в таких случаях приобретает бурый либо красный оттенок. Самой распространенной причиной появления данных клеток в моче принято считать заболевания почек и мочевыводящих путей. К их числу можно причислить различные инфекции, пиелонефрит (воспаление ткани почек), гломерулонефрит (заболевание почек, характеризующееся воспалением гломерулы, т.е. обонятельного клубочка), почечнокаменную болезнь, а также аденому (доброкачественную опухоль) предстательной железы. Выявить данные клетки в моче удается и при опухолях кишечника, различных нарушениях свертываемости крови, сердечной недостаточности, оспе (заразной вирусной патологии), малярии (остром инфекционном заболевании) и т.д.
Нередко красные кровяные клетки появляются в моче и на фоне терапии некоторыми медикаментами типа уротропина. Факт наличия эритроцитов в моче должен насторожить как самого больного, так и его лечащего врача. Такие пациенты нуждаются в проведении повторного анализа мочи и полном обследовании. Повторный анализ мочи должен браться с использованием катетера. В случае если повторный анализ еще раз установит факт наличия в моче многочисленных красных клеток, тогда обследованию подвергают уже мочевыводящую систему.
Автор: Пашков М.К. Координатор проекта по контенту.
Физиология эритропоэза, синтез гемоглобина, как происходит образование эритроцитов?

Синтез эритроцитов представляет собой один из самых важнейших и сложных процессов формирования клеток в организме. В норме каждую секунду создается два-три миллиона кровяных телец. Сам процесс образования эритроцитов называется эритропоэзом. Как же он происходит? Как выполняется нервная и гуморальная регуляция этого процесса?
Кроветворение
Можно выделить единую схему образования всех компонентов крови, в том числе и эритроцитов. На ней кратко и отчетливо видны стадии развития конкретной клетки. С помощью данной схемы можно отследить, на каком этапе произошла ошибка, и образование эритроцита прекратилось.
Специалист может активизировать созревание телец на этой стадии. Пользуясь схемой можно понять физиологию процесса кроветворения, верно поставить диагноз и вовремя предпринять меры по устранению патологии.
 Схема образования клеток крови
Схема образования клеток крови
Физиология формирования клеток
Какова же физиология образования кровяных клеток? Эритропоэзом называют процесс, в ходе которого формируются и созревают кровяные тельца – эритроциты. Это происходит в костном мозге человека. Первый элемент, от которого начинается происхождение эритроцитов, – полипотентная стволовая клетка.
Она способна дифференцироваться во все клетки без исключения и подвергается нескольким этапам деления, в результате чего появляются клетки-предшественники, от которых потом начинают развиваться эритроциты, лейкоциты, лимфоциты.
Все предшественники эритроцитов в костном мозге и зрелые клетки в кровотоке образуют замкнутую систему, которая называется эритроном. Клетки созревают под регуляцией гормона эритропоэтина и других необходимых компонентов. По времени этот процесс протекает не более двух недель.
Со стадии проэритробласта начинает вырабатываться гемоглобин. Ядро по мере развития эритроцита уменьшается, а потом исчезает вовсе. Уже на стадии ретикулоцита кровяные тельца выходят в кровь. В ней они за нескольких часов дозревают до полноценных эритроцитов.
Когда у человека происходят какие-либо патологические нарушения, которые сопровождаются анемией: острые кровопотери, отравления, инфекционные болезни, в крови могут образовываться недозрелые тельца, называемые нормобластами. Это говорит о том, что эритропоэз происходит в усиленном режиме. Для проверки физиологии этого нарушения проводятся лабораторные исследования.
Важно! Стоит отметить, что при образовании предшественников эритроцитов происходит разрушение части клеток еще в костном мозге. Этот процесс называют неэффективным эритропоэзом. Он заключается в разрушении и гибели кровяных телец, которые не обладают функциональной полноценностью. Роль неэффективного типа эритропоэза состоит в регуляции эритрона.
Компоненты, необходимые для эритропоэза
Чтобы все этапы эритропоэза проходили нормально, требуются микроэлементы, гормоны, витамины и прочие важные для этого процесса веществ. К ним относят:
- Железо. Для образования эритроцитов организму требуется до 25 мг железа в сутки. Этот элемент поступает в костный мозг, когда происходит разрушение кровяных телец. Накапливается железо в печени и селезенке, немного в других органах. При дефиците данного компонента образуется железодефицитная анемия.
- Медь. Ее роль тоже очень важна для формирования эритроцитов. Она усваивается непосредственно в костном мозге, участвует в выработке гемоглобина. Без меди эритроциты не могут развиваться полностью, они доходят только до стадии ретикулоцита. Если уровень меди снижен, то синтез крови в костном мозге останавливается, что вызывает анемию.
- Витамин B12 и фолиевая кислота. Данные компоненты взаимодополняют друг друга, положительно влияя на эритропоэз.
- Витамин В6 нужен, чтобы в гемоглобине сформировалось железо.
- Витамин В2 Требуется для нормализации окислительных и восстановительных процессов в организме.
- Гормоны, отвечающие за обмен белков и кальция и принимающие участие в созревании клеток.
- Половые гормоны мужчин. Они немного активизируют процесс эритропоэза. А вот женские эстрогены, наоборот, тормозят его. Этим и объясняется тот факт, что количество эритроцитов у женщин меньше, чем у мужчин.
Важно! Главным элемент эритропоэза – гормон эритропоэтин, гуморальный регулятор созревания кровяных телец. Секреция и синтез данного компонента происходит в перитубулярных клетках почек. Некоторая часть эритропоэтинов формируется в печени, селезенке и костном мозге.
Как меняются клетки?
Проходя через все стадии эритропоэза, клетки подвергаются изменения морфологических характеристик. Происходит следующее:
- Меняются параметры клеток в сторону уменьшения.
- Увеличивается число цитоплазматического матрикса.
- Изменяется оттенок телец от голубого до красного. Это происходит потому, что снижается концентрация РНК и ДНК, а уровень гемоглобина, наоборот, повышается.
- Становятся меньше параметры ядра, в конечном итоге оно вообще исчезает.
- Содержащий в эритроцитах хроматин приобретает большую плотность.
 Стадии созревания клеток
Стадии созревания клеток
Гуморальная регуляция
Регуляция образования крови еще не полностью исследована на данный момент. Чтобы эритропоэз протекал непрерывно, все потребности различных клеток удовлетворялись в полной мере, обеспечивалось постоянство и баланс гомеостаза, требуется работа сложного регуляторного механизма.
Главный гуморальный регулятор, как уже говорилось, – гормон эритропоэтин. Он образуется в различных внутренних органах человека, но больше всего в почках, сосудах и печени. Концентрация этого компонента всегда одинаковая. Но возникают ситуации, когда уровень гормона нарушается. Это происходит при обильном кровотечении, подъеме в горы, ишемической болезни почек.
Вместе с гуморальным регулятором эритропоэтином в синтезе эритроцитов принимают участие ингибиторы. Они представляют собой разнообразные вещества, некоторые из которых относятся к токсинам, выделяющимся при патологических нарушениях.
На первых стадиях дифференцировки регуляция происходит благодаря факторам микроокружения клеток. Затем только в игру вступают эритропоэтин и ингибиторы.
Когда организму требуется в краткий срок сформировать множество новых кровяных телец, начинает действовать стрессовый механизм. Это значит, что эритропоэтин становится намного активнее ингибиторов эритропоэза, в результате чего нарушается регуляция эритропоэза. Возможен и обратный эффект, когда ингибиторы сильнее воздействуют на созревание клеток, приводя к торможению этого процесса.
Нервная регуляция
Конечно же, воздействие гуморальных факторов на эритропоэз намного сильнее и значимее, чем влияние нервной системы, но все же и последнее имеется. Когда возбуждается симпатический отдел вегетативной нервной системы, повышается количество эритроцитов в крови. Такое нарушение имеет перераспределительный характер и во многом зависит от опорожнения селезенки, в которой скапливаются кровяные тельца.
В это же время адреналин и норадреналин способствует стимуляции аденилатциклазной системы. В итоге усиленно выделяется эритропоэтин. В гипоталамусе человека присутствуют особые центры, благодаря которым происходит нервная регуляция эритропоэза. Если на него воздействует какой-то раздражитель, то он начинает провоцировать образование клеток, что приводит к повышению уровня эритроцитов в крови.
Выработка гемоглобина
Гемоглобин содержит в себе железо, дефицит которого может вызвать развитие анемии. Выработка этого вещества и эритропоэз связаны друг с другом. Когда уровень гемоглобина достигает определенного порога, образование эритроцитов останавливается.
Синтез гемоглобина начинается в клетках-предшественниках кровяных телец. Это происходит еще при внутриутробном развитии плода. После появления ребенка на свет у него появляется гемоглобин F, а потом гемоглобин А. У взрослых может отмечаться возникновение гемоглобина F, например, при кровопотере.
В составе гемоглобина содержатся два типа цепей глобина. Они располагаются вокруг гема, который содержит в себе железо. Исходя из того, как изменяются последовательности остатков аминокислот в цепях, модифицируются и свойства гемоглобина. К примеру, он может под воздействием некоторых условий преобразовываться в кристаллы и терять способность к растворению.
Образование эритроцитов и прочих компонентов крови – это довольно сложный и важный процесс, который проходит в несколько этапов. Любое нарушение в созревании клеток может привести к отклонениям в работе организма, поэтому необходимо своевременно выявлять факторы, способные вызвать его.
Эритропоэз. Роль железа, витаминов и микроэлементов в кроветворении
Эритропоэз
Под эритропоэзом понимают процесс образования эритроцитов в костном мозге.
Первой морфологически распознаваемой клеткой эритроидного ряда, образующейся из колониеобразующей единицы эритроцитарной (КОЕ-Э) — клетки-предшественницы эритроидного ряда, является проэритробласт, из которого в ходе 4-5 последующих удвоений и созревания образуется 16-32 зрелых эритроидных клеток.
(Например, 1 проэритробласт → 2 базофильных эритробласта I порядка — (удвоение) → 4 базофильных эритробласта II поряда → 8 полихроматофильных эритробластов I порядка → 16 полихроматофильных эритробластов II порядка → 32 полихроматофильных нормобласта → 32 оксифильных нормобласта → денуклеация нормобластов → 32 ретикулоцита → 32 эритроцита).
Эритропоэз в костном мозге (до формирования ретикулоцита) занимает 5 дней.
В костном мозге человека и животных эритропоэз (от проэритробласта до ретикулоцита) протекает при взаимодействии эритроидных клеток с макрофагами костного мозга. Эти клеточные ассоциации получили название эритробластических островков (ЭО) (рис.6.2.).
 рис.6.2.
рис.6.2.
рис.6.2.Эритробластический островок костного мозга человека.
1-эритробласт
2-цитоплазма макрофага.
У здоровых людей в костном мозге содержится до 137 ЭО на мкг ткани, при угнетении же эритропоэза их количество может уменьшаться в несколько раз, а при стимуляции —увеличиваться.
Макрофаги ЭО играют важную роль в физиологии эритроидных клеток, влияя на их размножение (пролиферацию) и созревание за счет:
- Фагоцитоза вытолкнутых из нормобластов ядер;
- Поступления из макрофага в эритробласты с помощью пиноцитоза ферритина, других пластических веществ, необходимых для развития эритроидных клеток;
- Секреции эритропоэтинактивных веществ;
- Высокого сродства к эритроидным клеткам-предшественницам, позволяющим макрофагам создавать благоприятные условиях для развития эритробластов.
Из костного мозга в кровь поступают ретикулоциты, в течение суток созревающие в эритроциты. Поэтому количество ретикулоцитов в крови отражает эритроцитарную продукцию костным мозгом, и по их количеству в крови судят об интенсивности эритропоэза. У человека их количество составляет 5- 10 %. За сутки в 1 мкл крови поступает 60-80 тыс. эритроцитов.
В 1 мкл крови у мужчин содержится 5+0,5 млн, а у женщин — 4,5±0,5 млн эритроцитов.
Регуляция эритропоэза
Гуморальным регулятором эритропоэза является гормон эритропоэтин. Основным источником его у человека являются почки, их перитубулярные клетки — в них образуется до 85-90 % гормона, остальное количество вырабатывается в макрофагах (купферовские клетки и др.).
Синтез и секреция эритропоэтина
Синтез и секреция эритропоэтина определяется уровнем оксигенации почек. Структурой почек, чувствительной к гипокисии, является гемсодержащий белок перитубулярных клеток, связывающий молекулу кислорода. При достаточной оксигенации почек оксиформа гемопротеина блокирует ген, регулирующий синтез эритропоэтина. В отсутствии кислорода деоксиформа гемопротеина прекращает тормозить синтез эритропоэтина. При дефиците кислорода в почечных структурах активируются чувствительные к гипоксии ферменты. Например, фосфолипаза А2 ответственная за синтез простагландинов, в т.ч. Е1 и Е2-, активирующих аденилатциклазу и вызывающих рост концентрации цАМФ в перитубулярных клетках почек, синтезирующих эритропоэтин. Лактан, адреналин, норадреналин, взаимодействующие с В2-адренорецепторами почек, также активируют аденилатциклазную систему, при этом нарастает концентрация цАМФ и цГМФ, вызывающих усиление синтеза и секрецию эритропоэтина в кровь. Так, продукцию эритропоэтина стимулирует пребывание человека в горах, где рО2 в атмосферном воздухе снижено; кровопотеря, уменьшающая кислородную емкость крови и т.д. У человека количество эритропоэтина составляет 0,01-0,08 МЕ/мл плазмы, но при гипоксии оно может возрастать в 1000 и более раз. Существует взаимосвязь между величиной гематокрита и уровнем эритропоэтина в плазме. При гематокрите, равном 40-45, количество эритропоэтина составляет 5-80 милиЕД/мл, а при гематокрите равном 10-20 — 1-8 ЕД/мл плазмы. Эритропоэтин усиливает пролиферацию клеток-предшественниц эритроидного ряда — КОЕ-Э, а также всех способных к делению эритробластов и ускоряет синтез гемоглобина во всех эритроидных клетках, включая ретикулоциты. Эритропоэтин «запускает» в чувствительных к нему клетках синтез иРНК, необходимых для образования энзимов, участвующих в формировании гема и глобина. Гормон увеличивает также кровоток в сосудах, окружающих эритропоэтическую ткань в костном мозге, и увеличивает выход в кровь ретикулоцитов из его синусоидов.
Торможение эритропоэза
Торможение эритропоэза вызывают особые вещества — ингибиторы эритропоэза, образующиеся при увеличении массы циркулирующих эритроцитов, несоответствующей потребностям тканей в кислороде. Они обнаруживаются, например, в крови у спустившихся с гор людей. Ингибиторы эритропоэза удлиняют цикл деления эритроидных клеток, тормозят в них синтез гемоглобина.
Эритропоэз активируют увеличивающие чувствительность ткани костного мозга к эритропоэтину мужские половые гормоны — андрогены. Стимулирующее влияние оказывают не сами андрогены, а продукты их 5-В- редуктазного превращения — 5-В- Н- метаболиты.
Женские половые гормоны — эстрогены обладают противоположным действием на эритропоэз. После полового созревания устанавливающиеся различия в содержании эритроцитов и гемоглобина с более высокими их значениями у мужчин, чем у женщин, связаны с указанным эффектом половых гормонов.
Катехоламины, взаимодействуя с В-адренорецепторами КОЕ-Э, усиливают пролиферацию этих эритроидных клеток- предшественниц.
Роль железа в кроветворении
Из 4 — 5 г железа, содержащегося в организме, 1/4 составляет резервное железо, а остальное — функционально активно. Из этого количества в состав гемоглобина эритроцитов входит 62-70%, 5-10% содержится в миоглобине, остальное — в тканях, где оно участвует во многих метаболических процессах: в составе металлосодержаших энзимов обеспечивает митохондриальный транспорт электронов, синтез ДНК и деление клеток, метаболизм катехоламинов (гормонов мозгового вещества надпочечников), детоксикационные механизмы, т.е. снижающие активность токсических веществ, поддерживая, в частности, концентрацию цитохрома Р450. Поэтому дефицит железа в организме человека понижает его физическую активность и работоспособность.
В организме человека происходит интенсивный обмен железа, оно постоянно перемещается из мест его накопления к местам использования и обратно. Так, эритропоэз ежесуточно требует от 20 до 25 мг железа. Почти все это количество железа костный мозг получает за счет его повторного использования. Только около 1 мкг железа вновь ежедневно всасывается в кишечнике, пополняя потери с калом, мочой, потом и слущиванием кожи. У молодых женщин потери железа больше (менструация, беременность). Fe ++ поступает в эритробласты с белком плазмы — трансферрином, гликопротеином (MB 76000), мигрирующим при электрофорезе белков плазмы вместе с В1— глобулинами. Плазма содержит от 1,8 до 2,6 мг/л трансферрина. Поскольку 1 мг белка связывает 1,25 мкг Fe ++ , то в общем объеме плазмы содержится около 3 мг железа. В норме лишь 1/3 трансферрина плазмы насыщена железом. Дополнительное количество железа, которое может связываться с ненасыщенным железом трансферрином плазмы, определяет ненасыщенную железосвязывающую способность крови. Общее количество железа, которое может быть связано трансферрином, называется общей железосвязывающей способностью крови (ОЖСК). Концентрация железа в плазме достигает у мужчин 120 мг%, у женщин — 80 мг%. ОЖСК нормальной сыворотки крови составляет 290-380 мг%, с мочой выводится за сутки 60-100 мкг железа.
Комплекс трансферрин-железо фиксируется на рецепторах мембраны эритробласта, количество рецепторов уменьшается в ходе созревания эритроидных клеток, исчезая после созревания ретикулоцитов. Поэтому зрелый эритроцит не включает железо. Освобождение железа из комплекса трансферрин-железо обеспечивается энергией АТФ. Молекула трансферрина, отдавшая железо, смещается с мембранного участка молекулами трансферрина, связанными с железом, поскольку их сродство к рецепторам более сильное. Железо, поступившее в эритробласт, используется в митохондриях для синтеза гема и депонируется в эритробласте в виде резерва. В макрофагах печени, костного мозга резервное железо депонируется в молекуле ферритина, состоящей из 24 единиц белка апоферритина, образующих подобие скорлупы, в центре которой аккумулируется железо. Молекулы ферритина, в свою очередь, образуют внутри лизосом большие аморфные нерастворимые агрегаты — гемосидерин. Таким образом, ферритин и гемосидерин — это формы резервного железа в клетках. При освобождении железа из клеточного резерва оно переводится в двухвалентное состояние (благодаря энзиму ксантиноксидазе, аскорбиновой кислоте и др.), соединяется с трансферрином и транспортируется к эритробластам.
Абсорбция железа эпителиальными клетками желудочно-кишечного тракта усиливается при увеличении концентрации трансферрина в слизистой кишечника, эритропоэтической активности костного мозга и снижается при увеличении концентрации железа в клетках слизистой оболочки кишечника. Абсорбция Fe ++ в кишечнике более эффективна, чем Fe +++ и вещества, поддерживающие двухвалентную форму железа, его растворимость — аскорбиновая кислота, фруктоза, аминокислоты (цистеин, метионин), ускоряют абсорбцию железа. Важным условием абсорбции железа в кишечнике является его биодоступность. Например, железо, входящее в состав гема (мясные продукты, кровяная колбаса) лучше всасывается вкишечнике, чем железо из пищи растительного происхождения.
Роль витаминов в кроветворении
Для нормального метаболизма кроветворная ткань нуждается в поступлении в костный мозг ряда вешеств.
Витамин В12 и фолиевая кислота необходимы для синтеза нуклеопротеинов, созревания и деления ядер клеток. При их дефиците в наиболее интенсивно делящейся ткани организма — эритроидной, раньше, чем в других, возникают нарушения, выражающиеся в развитии анемии. Она связана с формированием в костном мозге огромных ядросодержаших эритроидных клеток — мегалобластов с замедленной скоростью созревания. Образующиеся из них большие эритроциты — мегалоциты обладают резко укороченным периодом жизни. Вследствие указанных нарушений — замедленного поступления эритроцитов в кровь и быстрого их разрушения в ней, возникает анемия. Это заболевание эффективно излечивается введением витамина В12.
Причина дефицита В12 в организме связана с утратой способности париетальных клеток желудка продуцировать «внутренний фактор» — гликопротеин (MB 60000), который, связывая витамин В12 , поступающий с пищей, предохраняет его от расщепления пищеварительными ферментами. Эти нарушения возникают при атрофии слизистой желудка, часто наблюдающейся, например, у стариков (глава 20). И хотя запаса витамина В12 в печени хватает взрослому человеку на 1-5 лет, постепенное его истощение приводит к заболеванию.
Витамин В12 содержится в больших количествах в таких продуктах питания, как печень, почки, яйца. Ежесуточная потребность организма в витамине В12 достигает 5 микрограмм, содержание в плазме крови — 150-450 микрограмм/л. Поступив в кишечник, комплекс гликопротеин- В12 фиксируется специальными рецепторами слизистой тонкого кишечника и витамин поступает в интестинальные клетки, и далее — в кровь, в которой с помощью особых транспортирующих молекул — транскобаламинов (I, II и III типов) переносятся к печени и костному мозгу. Транскобаламины I и III типа продуцируются лейкоцитами, II — макрофагами. Поэтому при гиперлейкоцитозе отмечается гипервитаминоз В12.
Фолиевая кислота (витамин В9) поддерживает синтез ДНК в клетках костного мозга благодаря обеспечению этого процесса одним из нуклеотидов — диокситимидилатом, образующимся в результате митилирования диоксиуридиловой кислоты в присутствии тетрагидрофолата (одной из редуцированных форм фолиевой кислоты). Ежедневная нормальная потребность организма человека в фолиевой кислоте составляет 500-700 мгр. Ее резерв в организме равен 5- 10 мг, причем треть его находится в печени. Недостаточное поступление фолиевой кислоты с пищей уже через несколько месяцев вызывает анемию, связанную с ускоренным разрушением эритроцитов. Фолиевой кислотой богаты овощи (шпинат), дрожжи, молоко.
Витамин В6 (пиридоксин) является кофактором (т.е. дополнительным фактором активности) АЛК-синтетазы (рис.6.1.), участвующей в образовании гема в эритробластах, и его дефицит вызывает анемию вследствие нарушенного гемоглобинопоэза.
 рис.6.1. Схема синтеза гемоглобина у человека.
рис.6.1. Схема синтеза гемоглобина у человека.
Витамин С поддерживает основные этапы эритропоэза, способствуя метаболизму фолиевой кислоты в эритробластах. Он участвует в метаболизме железа как на уровне его абсорбции в желудочно-кишечном тракте, так и мобилизациии депонированного в клетках железа.
Витамин Е (а-токоферол) осуществляет защиту фосфатидилэтаноламина мембран эритроцитов от перекисного окисления, усиливающего гемолиз эритроцитов.
Витамин РР. Защиту гемоглобина и мембраны эритроцитов от окисления осуществляет и витамин РР, являющийся одним из составляющих пиридиннуклеотидов НАД и НАДФ.
Витамин В2 участвует в окислительно-восстановительных реакциях и его дефицит вызывает у человека анемию гипорегенеративного типа.
Роль микроэлементов в кроветворении
В метаболизме гемопоэтической ткани участвуют микроэлементы:
Медь, обеспечивающая лучшее всасывание железа в кишечнике и мобилизацию его резерва из печени и ретикулярных клеток;
Никель и Кобальт, имеющие отношение к синтезу гемоглобина и гемсодержаших молекул, способствующих утилизации железа. Их недостаток вызывает анемию (например, в районах, где почвы бедны этими микроэлементами).
Селен, тесно воздействуя с витамином Е, защищает мембрану эритроцита от повреждения свободными радикалами.
Цинк— Почти 75% всего цинка в организме человека находится в эритроцитах, в составе фермента карбоангидразы. Недостаток цинка вызывает лейкопению.
Иисус Христос объявил: Я есмь Путь, и Истина, и Жизнь. Кто же Он на самом деле ?
Жив ли Христос? Воскрес ли Христос из мертвых? Исследователи изучают факты


