Токсоплазмоз
Токсоплазмоз – заболевание, которое в терминах паразитологии относится к группе протозойных паразитозов. Эта группа болезней характеризуется рядом специфических особенностей, поскольку весьма своеобразны их возбудители, составляющие подцарство простейших (protozoa). Более подробные сведения об этой группе патогенов представлены в статьях «Болезни, вызываемые простейшими» и «Простейшие. Амебиаз».
Возбудитель
Заболевание токсоплазмоз вызывается единственным (насколько сегодня известно) представителем рода токсоплазмы – простейшим Toxoplasma Gondii. Назван этот микроорганизм именем североафриканского горного грызуна гонди (другой вариант названия – гунди), у которого он был впервые обнаружен в 1908 году. Морфологически токсоплазма представляет собой округлую или, чаще, продолговатую клетку, формой напоминающую банан либо дольку апельсина. Это один из самых мелких представителей протозойного подцарства: длина составляет 8-10 мкм, поперечный габарит 2-4 мкм. Тем не менее, по всем признакам (см.выше) это именно простейшее, а не бактерия. Наряду с двумястами плазмодиями, из которых как минимум пять вызывают малярию, токсоплазма входит в класс споровиков (Sporozoa).
Токсоплазма является внутриклеточным паразитом и в качестве промежуточного хозяина может колонизировать около 300 видов теплокровных животных, включая человека, и не менее 60 видов птиц. Однако окончательным хозяином является семейство кошачьих, в том числе обычная домашняя кошка. Не будь этой особенности, – и едва ли стоило бы размещать данную статью на сайте Лахта Клиники. Дело в том, что организм «промежуточного хозяина» используется возбудителем для паразитирования в тканевых формах и размножения простым бесполым делением, тогда как «окончательный хозяин» означает организм, в котором токсоплазма размножается половым путем и образует т.н. ооцисты (яйцецисты) – ту самую форму, которая устойчива как ко внешним, так и к внутренним средам, и может годами пребывать в зрелом жизнестойком состоянии, чтобы однажды активизироваться в организме нового или «хронического» хозяина. В том числе и человека.
На сегодняшний день общая распространенность носительства токсоплазмы в мире оценивается в пределах 40-70%; иногда приводятся и более высокие проценты. Однако статистика обнаруживает выраженную региональную зависимость, что отчасти обусловлено неравномерностью распределения самой токсоплазмы в земной экосистеме (в Южной Корее, например, ее почти совсем нет, а в Южной Америке очень много – в некоторых областях заражено до 90% населения). Частота встречаемости в России оценивается на уровне 20%, то есть каждый пятый из нас является, как минимум, носителем.
В течение активного, острого периода течения токсоплазмоза (2-3 недели) больная кошка с фекалиями выделяет порядка двух миллиардов цист.
Жизнеспособность их сохраняется, в зависимости от условий, до двух и более лет.
Заражение
Присутствие токсоплазмы в организме домашней кошки можно считать доказанным, если в ее рационе хотя бы эпизодически случается сырое мясо, если она имеет возможность охотиться на мышей и если бывает на улице. Любая песочница, к которой имеют доступ коты, – инфицирована. Человек заражается через мясо, недостаточно обработанное термически; в некоторых странах (например, во Франции), где в блюдах национальной кухни присутствует «мясо с кровью», частота выявляемости антител к токсоплазме значительно выше. Возможно заражение через немытые овощи и фрукты, грязные руки, а также, в единичных случаях, через поврежденную кожу (раньше это представлялось сомнительным, в настоящее время сомнений не вызывает).
Кроме того, возможно внутриутробное трансплацентарное заражение от первично инфицированной матери. Обратим на это особое внимание.
Патогенез
Проникнув в кишечник промежуточного хозяина, – например, человека, – циста благодаря пищеварительным ферментам избавляется от защитной оболочки и высвобождает активную форму токсоплазмы, т.н. спорозоиты. В свою очередь, спорозоиты представлены двумя разными типами – тахизоитами и брадизоитами (напомним, «тахи-» и «бради-» переводится как «быстро» и «медленно», соотв.), которые гематогенным путем разносятся в различные участки организма, где стремятся внедриться в клетки хозяина. Во внутриклеточном пространстве брадизоиты, которые с трудом или вообще не идентифицируются иммунной системой, медленно размножаются, воспроизводя активные формы. Тахизоиты делятся гораздо быстрее (напомним, обе формы в промежуточном хозяине размножаются «бактериальным» агамогенезом и увеличивают свою популяцию стремительно – по тому же экспоненциальному закону, что и бактерии). Когда растущая плотная колония тахизоитов (псевдоциста) внутри клетки достигает критического объема, клетка погибает, тахизоиты оказываются в межклеточном пространстве (здесь их могут обнаружить и уничтожить иммунные факторы), и те из них, кто успел внедриться в следующую клетку, начинают цикл заново. Таким образом, в процессе постоянного самовоспроизведения внутриклеточно-паразитарные формы токсоплазмы, во-первых, быстро увеличивают свою численность, во-вторых, последовательно убивают колонизированные ими ткани. Кроме того, в организме могут оставаться целостные цисты, по какой-либо причине не активизировавшиеся в кишечнике, а также образовываться новые, – если паразитоз из-за слабости иммунной системы, неспособной к полной эрадикации, приобрел хронический характер и вошел в «бесконечный цикл» рецидивов и ремиссий.
Опасность для человека, симптоматика
Крайне важно отметить: доля инфицированных токсоплазмой людей, у которых развивается клинически значимый токсоплазмоз, очень мала – по разным оценкам, она варьирует от долей процента до нескольких процентов. Животные и птицы болеют токсоплазмозом гораздо чаще (см. ниже). Человек же практически всегда переносит токсоплазменную инвазию бессимптомно, поскольку иммунная система мгновенно распознает этот микроорганизм как враждебный – и реагирует настолько мощно, что инфицированный обычно даже не узнаёт о том, что был чем-то заражен. Кроме того, исключена опасность заразиться от инфицированного, даже если он переживает острый период токсоплазмоза (как правило, не подозревая об этом).
Таким образом, нет никаких оснований создавать лепрозории для носителей, повсеместно истреблять диких кошек и избавляться от кошек домашних, а ребенка выпускать на улицу лишь в скафандре высшей эпидемиологической защиты. Можно сказать, что мы, взрослые люди, если и были когда-то инфицированы, то эта проблема давным-давно решена, причем раз и навсегда: к токсоплазме вырабатывается устойчивый пожизненный иммунитет, и даже если человек попадает в незначительный процент переболевших в клинически значимой степени (лихорадка, легкое общее недомогание, мышечные боли, лимфаденопатия, спленогепатомегалия), то это уже не повторяется ни при каких обстоятельствах.
Иными словами, токсоплазма распространена широко, однако токсоплазмозом как болезнью почти никто из людей не болеет. И на этом, опять же, можно было бы поставить точку, если бы не слово «почти» и связанные с ним три «но».
Почти никто – это ведь не значит «абсолютно никто», особенно в пересчете на статистические масштабы. В какой-то, пусть даже малой, доле случаев острый период токсоплазмоза протекает отнюдь не бессимптомно и не в легкой гриппоподобной форме, а с весьма тяжелыми воспалительными осложнениями, такими как хориоретинит (поражаются сетчатка и сосуды глаз), пневмония (воспаление легких), энцефалит (воспаление головного мозга), эндокардит (воспаление внутрисердечной оболочки). Шансы вытянуть несчастливый билет в этой лотерее, повторим, статистически очень малы, но они не равны нулю, и в этом заключается первое «но».
Второе «но» состоит в том, что токсоплазма очень опасна для людей с выраженным иммунодефицитом. Ослабление иммунитета в силу «обычных» причин (переохлаждение, переутомление, стрессы, гиповитаминоз, перенесенная операция и мн.др.) является прямым фактором риска развития ОРВИ и многих других инфекций, но к токсоплазмозу это отношения не имеет. Речь идет именно о глубоком, выраженном иммунодефиците. В первую очередь это, конечно, ВИЧ/СПИД, но не только. Есть определенный процент лиц, вынужденных принимать онкологическую химиотерапию или иммуносупрессоры (напр., при аутоиммунных заболеваниях, после трансплантации органов и т.д.). Для всех этих категорий людей «почуявшая слабину» токсоплазма смертельно опасна: если при здоровом или даже ослабленном иммунитете ее быстро и безжалостно уничтожает наша природная защита, то в отсутствие или при глубокой недостаточности такой защиты токсоплазма столь же быстро и безжалостно пожирает мозговые, легочные, сердечные ткани, приводя к их массовому некрозу и, в итоге, к летальному исходу.
Наконец, третье «но», – главный мотив публикации данного материала: токсоплазмоз и беременность. Вопросы на эту тему сегодня звучат постоянно, и некоторым женщинам в период гестации действительно приходится сталкиваться с проблемой, которая, наверное, правильного решения не имеет вообще – ни рационального, ни эмоционального, ни интуитивного. Поэтому всё, что здесь можно сделать – это еще на этапе планирования беременности как можно лучше изучить вопрос и по возможности отчетливо представлять себе, в каком случае токсоплазма опасна, и насколько она опасна, и чем именно, и какие существуют способы предотвратить беду.
Как показано выше, токсоплазма способна проникать через плаценту в организм плода. Единственный вариант и единственное стечение обстоятельств, при которых это представляет реальную угрозу, – первичное инфицирование токсоплазмой в период беременности, т.е. первое в жизни заражение женщины, у которой ранее не было иммунитета к возбудителю. В этом случае действуют следующие статистические риски и клинические закономерности.
Чем больше срок беременности, тем выше проницаемость плаценты и вероятность инфицирования плода: в зависимости от триместра, этот риск оценивается как 15%, 25% и 70%.
Если внутриутробное заражение все же произошло, то тяжесть последствий для плода тем больше, чем меньше срок беременности. Вероятности того, что внутриутробный токсоплазмоз в дальнейшем ничем себя не проявит, – не существует. Надеяться на то, что произойдет уникальное чудо и последствий удастся избежать, к несчастью, не приходится даже в том случае, когда инвазия сразу же диагностирована и подвергнута интенсивному квалифицированному лечению. На практике внутриутробный токсоплазмоз означает смерть плода со спонтанным абортом, рождение с гидро- либо микроцефалией, или же развитие, в дальнейшем, тяжелейших поражений центральной нервной, зрительной и других систем организма. Интеллектуальная недостаточность характеризуется глубокой степенью выраженности.
В подобной ситуации, – когда происходит первичное заражение беременной женщины, – приходится ставить вопрос об искусственном прерывании беременности.
На последующие беременности вышеописанные риски не распространяется: речь, повторим, идет лишь о ситуациях, когда первичная инвазия токсоплазмы приходится на гестационный период.
Частота врожденного токсоплазмоза на сегодняшний день варьирует в пределах от 1:1000 до 1:10000 новорожденных.
Диагностика
Стандартом диагностики токсоплазмоза, в том числе на этапе внутриутробного развития, является серологическое исследование: реакция непрямой флюоресценции или ИФА (иммуноферментный анализ). Дополнительно назначают УЗИ и другие исследования по показаниям.
Лечение
Не лишне повторить снова и снова: абсолютное большинство случаев приобретенного (не внутриутробного) токсоплазмоза лечения не требует, поскольку иммунная система справляется с вторжением паразита и на будущее вырабатывает антитела к нему. Однако и на случай осложненного течения в арсенале современной паразитологии есть медикаментозные средства, эффективные в отношении токсоплазмы, напр., пириметамин, сульфадиазин, клиндамицин и т.д. При поражении сетчатки глаза и центральной нервной системы может быть целесообразным назначение глюкокортикоидных гормонов. Пациенты, инфицированные вирусом иммунодефицита, противорецидивную терапию получают пожизненно.
При врожденной инфекции, даже если в перинатальном периоде она протекает бессимптомно (что является, увы, лишь вопросом времени), назначают продолжительную терапию указанными выше средствами с добавлением фолиевой кислоты. Пытаются справиться и с внутриутробным заражением (например, применяют природный антибиотик спирамицин).
Разумеется, любое лечение токсоплазмоза должно назначаться исключительно врачом и осуществляться под его постоянным наблюдением и лабораторным контролем.
Терапия врожденного и хронического токсоплазмоза малоэффективна или не эффективна вообще.
Профилактика
Учитывая вышесказанное, женщине при планировании или наступлении беременности чрезвычайно важно пройти все назначенные обследования, ни в коем случае не игнорируя какие бы то ни было анализы и процедуры. Если обнаружено отсутствие иммунитета к токсоплазме, или же имеет место выраженный иммунодефицит, необходимо принимать все меры предосторожности, особенно при наличии в доме кошки: животное не должно гулять на улице и питаться сырым мясом. Санитарную обработку туалетного лотка следует производить регулярно, и лучше бы к нему не прикасаться человеку, для которого токсоплазма представляет опасность. Кошку желательно обследовать в ветеринарной клинике и, если выявлен паразитоз, качественно пролечить. Возможно, наилучшим решением является, – как бы тяжело это ни было для большинства семей, – расстаться с домашним питомцем, по крайней мере временно, на период вынашивания беременности.
Овощи и фрукты необходимо тщательно отмывать; любые мясные продукты должны проходить достаточную термическую обработку, а столы и доски, на которых разделывается мясо, – очищаться с применением моющих средств. Все гигиенические процедуры, особенно после любого контакта с землей, овощами, фруктами, ягодами и т.д., лица из группы риска должны выполнять сразу же, с мылом, самым тщательным образом.
В заключение отметим, что мир простейших микроорганизмов по-прежнему находится в фокусе напряженного внимания исследователей, – в том числе фармакологов, – однако многие вопросы остаются неясными. Это касается и токсоплазмы, которое свое название получила отнюдь не случайно: вырабатываемый ею токсин необычен и может оказаться гораздо опасней, чем принято считать в настоящее время. Известно и доказано, в частности, что это вещество каким-то образом искажает баланс нейромедиаторов и, если концентрация его в организме высока, влияет на поведение носителя (например, определенные виды птиц именно по этой причине, а не из-за токсоплазмоза как такового, поставлены под угрозу вымирания). Кроме того, изучается серьезно обоснованная гипотеза о том, что токсоплазма играет патогенетическую роль в возникновении и развитии душевных болезней человека, – прежде всего, исследуется возможная связь между токсоплазмой и шизофренией. Для психиатрии такие исследования чрезвычайно важны, поскольку шизофрения, – эта «жестокая королева» психических заболеваний, – как тяжелый хронический эндогенный процесс за последние сто лет досконально изучена в клинических проявлениях, однако до сих пор совершенно непонятна в триггерных и патогенетических механизмах, и ежегодно наносит колоссальный социальный, психологический и экономический ущерб в масштабах всей цивилизации.
Токсоплазмоз головного мозга: симптомы, методы лечения и профилактики
1. Течение токсоплазмоза нервной системы. Toxoplasma gondii — это внутриклеточный паразит, поступающий в организм алиментарным путем. Заболевание развивается только при иммунодефицитных состояниях. Токсоплазмоз ЦНС обусловлен либо реактивацией местной инфекции вследствие иммунодефицита, либо гематогенным заносом инфекции из других органов также при реактивации. Токсоплазмоз ЦНС — наиболее частая оппортунистическая инфекция, вызывающая энцефалит у ВИЧ-инфицированных.
2. Клиническая картина токсоплазмоза нервной системы. Заболевание обычно начинается подостро и первыми признаками являются головные боли и лихорадка. Позже (от нескольких дней до 1-2 недель) развивается очаговый неврологический дефицит или признаки диффузного поражения мозга. У некоторых пациентов заболевание начинается остро, с припадков.
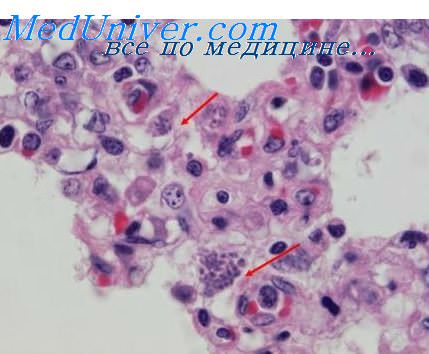
3. Диагностика токсоплазмоза нервной системы. Методы нейровизуализации позволяют выявить очаговые поражения у 80-85% больных токсоплазмозом ЦНС. МРТ — более чувствительный метод, чем КТ. Большинство очагов по виду напоминают опухоли, но в некоторых случаях их можно принять за инфаркт. Примерно у 15-20% больных выявляются единичные очаги неспецифичного вида. Результаты серологического исследования на IgG антитела к Toxoplasma gondii оказываются позитивными в 85% случаев. Антитела IgM не выявляются. В диагностике помогает проведение полимеразной цепной реакции (ПЦР), которая позволяет обнаружить ДНК токсоплазмы в ЦСЖ. Для подтверждения диагноза необходимо выявление самого возбудителя.
4. Лечение токсоплазмоза нервной системы
– Эффект лечения токсоплазмоза обычно наступает быстро. Поэтому прежде, чем принять решение о необходимости биопсии мозга у больных с множественными очагами и положительными результатами серологических проб на токсоплазму, проводится пробная терапия в течение 2 недель. Биопсия обязательна всем пациентам с одним очагом при негативных данных серологических исследований на токсоплазмоз. Обычно рекомендуется начать лечение с сульфадиазина в дозе 1,5 г внутрь каждые 6 ч в комбинации с пириметамином внутрь в начальной дозе 100 мг, с последующим снижением до 75 мг/сут. Для предотвращения миелосупрессии, которая нередко является осложнением лечения пириметамином, назначается фолиевая кислота в дозе 10 мг/сут. внутрь. Больным, которые не переносят сульфаниламиды, назначают клиндамицин в дозе 600—900 мг 4 раза в сутки, который не менее эффективен для подавления острой инфекции. Кортикостероиды обычно не назначаются при эмпирическом лечении, чтобы не помешать правильной диагностике. При развитии судорожных припадков показаны антиконвульсанты.
– При хороших результатах вышеописанной начальной терапии через 6 недель показан переход на пожизненное поддерживающее лечение сульфадиазином в дозе 300 мг 4 раза в сутки и пириметамином в дозе 50 мг/сут. в сочетании с фолиевой кислотой. Те больные, которые не переносят сульфаниламиды или клиндамицин, должны получать лечение атоваквоном* в дозе 750 мг внутрь 4 раза в сутки. Недостатком препарата является меньшая эффективность.
– К побочным эффектам и осложнениям лечения сульфаниламидами относятся аллергические реакции, токсическое поражение почек, поджелудочной железы и печени, нарушение функции желудочно-кишечного тракта и реже — гемолитическая анемия вследствие дефицита Г6ФД (глюкозо-6-фосфат-дегидрогеназы), а также токсическая энцефалопатия, невриты и головокружение. Среди побочных эффектов клиндамицина можно назвать нарушение функции желудочно-кишечного тракта в виде диареи, болей в животе, тошноты и рвоты. Возможно токсическое поражение печени, полиартрит и аллергические реакции. При быстром внутривенном введении препарата может наблюдаться артериальная гипотензия. Побочными эффектами пириметамина являются тромбоцитопения, анемия и лейкопения вследствие недостаточности фолиевой кислоты. Также изредка отмечается токсическое воздействие препарата на ЦНС в виде головной боли, спутанности сознания, припадков, тремора, атаксии, депрессии и бессонницы. Прием атоваквона может привести к нарушениям пищеварения, лихорадке, бессоннице, головным болям, головокружению и аллергическим реакциям. В редких случаях отмечаются признаки токсического поражения ЦНС, почек и подавление костномозгового кроветворения при использовании хинонов.
5. Ожидаемый результат лечения токсоплазмоза нервной системы. Крайне важно систематическое наблюдение за больным, получающим эмпирическое лечение токсоплазмоза. Нейровизуализационное обследование необходимо повторить через 2 недели после начала антибиотикотерапии. Если картина остается прежней, то требуется биопсия очагов. Если, несмотря на поддерживающую терапию, очаги увеличиваются в размере, также показана биопсия для исключения иной природы поражения. Большинство больных токсоплазмозом хорошо реагируют на антибиотикотерапию. Примерно у 10% пациентов развиваются рецидивы после прекращения поддерживающего лечения. Если, несмотря на поддерживающую терапию, отмечается рецидив, то показана биопсия для исключения альтернативного процесса. 6. Профилактика. Обследования больных СПИДом, принимающих сульфаниламиды с целью профилактики пневмоцистной пневмонии, показали, что такое превентивное лечение служит профилактикой и для токсоплазмоза ЦНС. Рекомендован ежедневный прием триметоприма-сульфаметоксазола DS или дапсона в дозе 50 мг/сут. и пириметамина в дозе 50 мг в неделю.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Токсоплазмоз
Токсоплазмоз – зоонозная протозойная инфекция, имеющая длительное течение и приводящая к поражению нервной, лимфатической, зрительной, мышечной систем, миокарда, печени, селезенки. Острый токсоплазмоз протекает с лихорадочно-интоксикационным синдромом, лимфаденопатией, гепатоспленомегалией, кожными высыпаниями; в тяжелых случаях – с развитием миокардита, энцефалита, энцефаломиелита. Диагноз токсоплазмоза устанавливается с помощью бактериологического посева, ПЦР, ИФА. Лечение токсоплазмоза включает прием этиотропных антипаразитарных препаратов, десенсибилизирующих, общеукрепляющих средств, иммунотерапию токсоплазмином.
МКБ-10
Общие сведения
Токсоплазмоз – хроническая паразитарная инвазия, вызываемая внутриклеточными простейшими (токсоплазмами) и сопровождающаяся развитием лимфаденита, гепатита, менингоэнцефалита, пневмонии, миокардита, миозита и др. Показатель инфицированности населения токсоплазмозом чрезвычайно высок: в Европе и Северной Америке он составляет 25-50%; в странах Африки, Южной и Латинской Америки – до 90%.
Огромную опасность токсоплазмоз представляет для беременных женщин и лиц со сниженным иммунитетом. В первом случае может происходить внутриутробное инфицирование плода с самопроизвольным прерыванием беременности, мертворождением или формированием эмбрио- и фетопатий; во втором – токсоплазмоз приобретает тяжелое манифестное течение. Учитывая множественные и разнообразные клинические проявления, токсоплазмоз актуален не только для инфекционных болезней, но также для неврологии, офтальмологии, пульмонологии, кардиологии.

Причины токсоплазмоза
Инфекционным агентом, приводящим к заболеванию, выступает Toxoplasma gondii (токосплазма), принадлежащая к роду облигатных внутриклеточных микроорганизмов, отряду кокцидий, классу споровиков. Токсоплазма имеет изогнутую форму полумесяца, один конец которого заострен, а другой более закруглен, длину 4-7мкм и ширину 2-5 мкм. В своем развитии возбудитель токсоплазмоза проходит фазы полового и бесполого размножения и стадии трофозоитов, цист и ооцист.
Половой цикл протекает в эпителиальных клетках кишечника представителей семейства кошачьих (домашних кошек, рыси, ягуара, пумы и др.), которые выступают окончательными хозяевами токсоплазм. Здесь образуются гаметоциты, которые затем дифференцируются в мужские и женские гаметы; при их слиянии формируется зигота, а затем ооциста. С испражнениями кошек ооцисты выделяются во внешнюю среду, где превращаются в инвазивные формы – спорозоиты.
Бесполый цикл размножения токсоплазм происходит в клетках различных тканей (ЦНС, печени, миокарда, плаценты и др.) человека и теплокровных животных. В организме паразит существует в форме трофозоитов, размножающихся путем продольного деления. При хроническом течении токсоплазмоза возбудители принимают форму тканевых цист, которые десятки лет могут пребывать в «спящем» состоянии и реактивироваться при понижении иммунитета, вызывая рецидив токсоплазмоза. Цисты и ооцисты токсоплазм высокоустойчивы во внешней среде (в почве сохраняются более 1 года) и резистентны к воздействию химиопрепаратов.
Инфицирование токсоплазмозом чаще всего происходит алиментарным путем при употреблении в пищу продуктов, обсемененных ооцистами, а также сырого мяса инфицированных животных; реже – контактным путем через поврежденную кожу. При беременности возможна вертикальная передача инфекции плоду через плаценту. Реже заражение токсоплазмозом происходит парентеральным путем (при переливании крови или трансплантации органов).
Патогенез
Попав в организм человека через ЖКТ, ооцисты внедряются в энтероциты нижних отделов тонкой кишки, откуда проникают в мезентериальные лимфоузлы, вызывая их воспаление (мезаденит), некроз, кальцификацию и образование специфических гранулем. Из первичного лимфатического очага токсоплазмы попадают в кровь и гематогенным путем разносятся по организму, где фиксируются в органах-мишенях: печени, селезенке, миокарде, ЦНС, оболочках глаз, скелетной мускулатуре, вызывая формирование некрозов, гранулем, нарушение функции пораженных органов.
Жизнедеятельность токсоплазм сопровождается выделением аллергенов и токсинов, что находит выражение в развитии общеинфекционного и аллергического синдромов. По мере выработки специфических антител вегетативные формы токсоплазм инцистируются, что знаменуется переходом токсоплазмоза в хроническую форму. При снижении активности иммунной системы (у больных СПИДом, гематологических и онкологических больных) возможна реактивация инфекции с генерализованным течением.
Симптомы приобретенного токсоплазмоза
С учетом характера инфицирования различают врожденный и приобретенный токсоплазмоз. Приобретенная инфекция может протекать в острой, хронической и латентной форме; при этом латентная форма подразделяется на первичную и вторичную, развивающуюся после острого или рецидива хронического токсоплазмоза.
Латентная форма
Примерно у 95-99% людей токсоплазмоз протекает в виде латентной инфекции. При острой манифестной форме токсоплазмоза инкубационный период составляет 2-3 недели. Легкое и субклиническое течение токсоплазмоза обычно диагностируется ретроспективно по положительным результатам кожных проб с токсоплазмином, серологическим реакциям, кальцифицированным лимфоузлам и другим признакам.
Генерализованная форма
Клинические проявления тяжелого генерализованного токсоплазмоза развиваются остро с внезапной лихорадки (t – до 38-39 °С) и явлений общей интоксикации (познабливания, снижения аппетита, миалгии, артралгии). Характерно увеличение печени и селезенки (гепатоспленомегалия), развитие лимфаденопатии, появление макулопапулезных высыпаний на коже. Чаще всего реакция выражена со стороны шейных, подмышечных, паховых, мезентериальных лимфоузлов, а также лимфатических узлов средостения. Кожные высыпания при токсоплазмозе располагаются по всему телу (кроме волосистой части головы, ладоней и подошв), могут сливаться в пятна с неровными волнистыми краями. На высоте остроты процесса может развиваться острый миокардит, энцефалит, менингоэнцефалит, энцефаломиелит. Тяжелые формы острого токсоплазмоза могут иметь летальный исход.
Хроническая форма
Хронический токсоплазмоз характеризуется длительным торпидным течением. Общие симптомы включают субфебрилитет, недомогание, похудание, генерализованные артралгии, лимфаденопатию. Проявлениями мезаденита служат диспепсические расстройства: тошнота, метеоризм, боли в животе, запор. Специфическими признаками хронического токсоплазмоза выступает поражение мышечной ткани, проявляющееся миозитом. Поражение сердца вызывает развитие очаговых или диффузных изменений миокарда или перикардита, проявляющихся утомляемостью, сердцебиением, одышкой, кардиалгиями.
Со стороны нервной системы отмечаются явления астении и вегето-сосудистой дистонии, неврастенические реакции и фобии. Многолетнее хроническое течение токсоплазмоза приводит к развитию эпилепсии, психических расстройств, снижению интеллекта. Эндокринные расстройства могут включать импотенцию, нарушение менструального цикла, вторичную надпочечниковую недостаточность. Поражение глаз при токсоплазмозе протекает в форме прогрессирующей близорукости, увеита, ретинита и хориоретинита с атрофией зрительного нерва.
Симптомы врожденного токсоплазмоза
Течение и исходы врожденного токсоплазмоза зависят от гестационного возраста плода. Инфицирование в I и II триместре приводит к внутриутробной гибели плода или формированию внутриутробных пороков – бластопатий, эмбрио- и фетопатий. В случае более позднего внутриутробного заражения (в III триместре) ребенок рождается с хронической, подострой или острой формой токсоплазмоза; при этом, чем позднее происходит инфицирование, тем тяжелее выражены симптомы на момент рождения.
Состояние новорожденных с острой формой токсоплазмоза тяжелое с первых дней. Отмечается фебрильная температура тела, выраженная интоксикация, обильные полиморфные высыпания на коже, генерализованная лимфоаденопатия, кровоизлияния в слизистые оболочки и склеры. Печень и селезенка обычно увеличены, часто развивается желтуха, диспепсические расстройства. Острый токсоплазмоз у новорожденных может приводить к развитию пневмонии, миокардита, энцефалита, менингоэнцефалита и летальному исходу. Подострое и хроническое течение токсоплазмоза характеризуется гидроцефалией, судорожным синдромом, длительной желтухой, субфебрилитетом, хориоретинитом.
В отдаленном периоде выявляются стойкие необратимые изменения, обусловленные внутриутробным инфицированием. Такими последствиями могут служить отставание в физическом развитии, задержка психического и речевого развития (ЗПР и ЗРР), микроцефалия, олигофрения, эпилепсия, микрофтальмия, слепота, тугоухость, глухота. Эти и другие нарушения расцениваются как резидуальный токсоплазмоз. Врожденный токсоплазмоз может иметь длительное латентное течение с клинической манифестацией на 2-7 году жизни ребенка.
Диагностика токсоплазмоза
В диагностике внутриутробного инфицирования большая роль отводится акушерскому анамнезу, результатам анализа на TORCH-инфекции у матери и серологических реакций у новорожденного, исследованию околоплодных вод и плаценты методом ПЦР. Дети нуждаются в наблюдении педиатра, детского офтальмолога, отоларинголога, невролога; проведении люмбальной пункции, КТ головного мозга, нейросонографии. Врожденный токсоплазмоз нужно дифференцировать с врожденной краснухой, герпесом, листериозом, цитомегалией, хламидийной инфекцией, внутричерепной родовой травмой.
Среди клинических проявлений наибольшее диагностическое значение при приобретенном токсоплазмозе имеет сочетание лимфаденопатии, гепатоспленомегалии, поражения глаз и ЦНС. Обязательно консультирование больного неврологом, офтальмологом, терапевтом или кардиологом. Основной перечень инструментальных исследований включает ЭЭГ, Эхо-ЭГ, рентгенографию или КТ черепа, офтальмоскопию, ЭКГ.
Для лабораторного подтверждения токсоплазмоза используются паразитологические и иммунологически методы. Первые предполагают микроскопическое выявление возбудителя в мазках-отпечатках пораженных органов, биоптате лимфоузлов, крови или спинномозговой жидкости. Возможно проведение биологической пробы с заражением лабораторных грызунов. Иммунологическая диагностика токсоплазмоза включает серологические методы (РСК, РНИФ, ИФА, РНГА), а также внутрикожную аллергическую пробу с токсоплазмином. В случае приобретенной инфекции в первую очередь исключается туберкулез, лимфогранулематоз, ревматизм, болезнь кошачьих царапин, инфекционный мононуклеоз, герпесвирусная инфекция.
Лечение токсоплазмоза
В зависимости от преимущественных органных поражений, лечение больных токсоплазмозом осуществляется в профильных отделениях: неврологических, терапевтических, кардиологических, офтальмологических и т. д. Этиотропная терапия при манифестном токсоплазмозе проводится препаратами противопаразитарного действия: чаще хлоридином в комбинации с сульфаниламидными препаратами или антибиотиками тетрациклинового ряда; при противопоказаниях – метронидазолом, хлорохином, аминохинолом. Обычно курс лечения токсоплазмоза состоит из 3-х 5-10-дневных циклов, повторяемых с интервалами 7-10 дней. Дополнительно назначаются антигистаминные и общеукрепляющие средства, поливитамины. При хроническом токсоплазмозе медикаментозный курс лечения дополняется иммунотерапией – внутрикожным введением токсоплазмина. Тактика ведения беременных с первично-хроническим или первично-латентным токсоплазмозом предполагает проведение химиопрофилактики спирамицином. При острой форме токсоплазмоза у беременной рекомендуется медицинский аборт.
Профилактика
Профилактика заражения человека токсоплазмозом включает комплекс ветеринарных (обследование и лечение домашних животных) и санитарно-гигиенических мероприятий. Последние предполагают избегание тесного контакта с кошками, тщательную термическую обработку мяса, защиту детских песочниц от испражнений безнадзорных животных, соблюдение мер личной гигиены. Обследование беременных на токсоплазмоз проводится трижды, в каждом триместре.
Токсоплазмозный энцефалит
Что провоцирует / Причины Токсоплазмозного энцефалита:
Возбудитель – Toxoplasma gondii относится к простейшим. Тип Protozoa. Подтип Sporozoa (обычно образуют споры; реснички, жгутики или псевдоподии отсутствуют). Класс Telosporea (имеется фаза полового размножения). Подкласс Coccidea (трофозоиты располагаются внутриклеточно, имеют “верхушечный комплекс”). Отряд Eucoccideia (жизненный цикл включает чередование бесполого – шизогония и полового размножения – спорогония). Подотряд Eimeriina (половая стадия в эпителии кишки у позвоночных животных; один хозяин или чередование двух хозяев; спорозоиты находятся в “споре”). Вид Toxoplasma gondii. Существует в трех основных формах: трофозоиты (эндозоиты), цисты и ооцисты. Трофозоиты имеют размеры 4-7 мкм в длину и 2-4 мкм в ширину, по форме напоминают полумесяц, хорошо окрашиваются по Романовскому. Они размножаются внутриклеточно во всех клетках млекопитающих за исключением безъядерных (эритроциты) и обнаруживаются в тканях в острой стадии инфекции. Скопление трофозоитов внутри одной клетки называют псевдоцистой. На трофозоиты активно воздействуют различные химиопрепараты (хлоридин, сульфаниламиды, макролиды и др.), они нестойки вне клетки и во внешней среде, быстро погибают при высушивании, прогревании, под влиянием дезинфицирующих средств.
Цисты формируются в организме хозяина, имеют собственную плотную оболочку. Размеры их до 100 мкм, внутри содержится 3000-5000 паразитов и более. Через плотную оболочку цист не проникают ни антитела, ни лекарственные препараты. Они очень устойчивы к различным воздействиям и в организме хозяина сохраняются десятки лет. Большая часть их локализуется в скелетных мышцах, миокарде, центральной нервной системе.
Ооцисты представляют собой образования овальной формы диаметром 10-12 мкм. Они формируются в слизистой оболочке тонкой кишки некоторых представителей семейства кошачьих и выделяются с испражнениями. Сроки появления ооцист в испражнениях кошки зависят от характера инфицирования и составляют от 3 до 24 дней. Экскреции продолжаются от 7 до 20 дней, за сутки с испражнениями может выделяться до 10 млн ооцист. Споруляция в выделенных фекалиях происходит через 2-3 дня (при температуре 24°С); она не реализуется при температуре ниже 4°С и выше 37°С. Ооцисты при благоприятных условиях сохраняются во внешней среде до 1 года и более. Именно они играют основную роль в передаче инфекции.
Культивируются токсоплазмы путем заражения лабораторных животных (белые мыши, морские свинки, кролики, хомяки), в развивающихся куриных эмбрионах, а также в культуре тканей. Имеются различные штаммы токсоплазм, некоторые из них отличаются высокой вирулентностью (штамм RH) и быстро приводят к гибели лабораторных животных, другие – маловирулентные (авирулентные) обычно не вызывают заметных клинических проявлений болезни.
Патогенез (что происходит?) во время Токсоплазмозного энцефалита:
Воротами инфекции чаще служат органы пищеварения, хотя известны случаи внутрилабораторных заражений высоковирулентными штаммами токсоплазм при повреждении кожи (пипеткой или шприцем с культурой токсоплазм). Внедрение возбудителя происходит в нижних отделах тонкой кишки, затем с током лимфы токсоплазмы достигают регионарных (мезентериальных) лимфатических узлов. Здесь развиваются воспалительные изменения с формированием инфекционных гранулем, напоминающих по клеточному составу туберкулезные или бруцеллезные гранулемы. Мезентериальные лимфатические узлы значительно увеличиваются. Затем токсоплазмы попадают в кровь, разносятся по всему организму и фиксируются в различных органах и тканях (печень, селезенка, лимфатические узлы, нервная система, глаза, миокард, скелетные мышцы). В этих органах образуются скопления паразитов в виде цист, которые могут сохраняться в организме десятки лет и даже пожизненно. В местах фиксации возникают воспалительные очаги, а в некоторых органах (нервная система, скелетные мышцы) – очажки некроза, в которых затем откладываются соли кальция и образуются кальцинаты.
В результате жизнедеятельности паразита и выделения антигенов и аллергенов наступает аллергическая перестройка организма (по типу реакций гиперчувствительности замедленного типа) и вырабатываются антитела, которые выявляются в различных иммунных реакциях (РСК, реакция с красителем Сэбина-Фельдмана, РПГА, ИФА и др.). В развитии иммунитета большое значение имеют как клеточные, так и гуморальные факторы. Наличие антител предохраняет от нового заражения даже высоковирулентными штаммами токсоплазм и обусловливает бессимптомное (латентное) течение токсоплазмоза у большинства инфицированных лиц. При ослаблении защитных сил организма и снижении напряженности иммунитета может наступить обострение заболевания (переход латентной формы в манифестную).
Обострение хронического токсоплазмоза, как правило, провоцируется интеркуррентными заболеваниями (грипп, ОРЗ, пневмонии и др.) и может наблюдаться иногда спустя длительное время (до 10-20 лет) после инфицирования. Описаны обострения с развитием тяжелого токсоплазмозного энцефалита после лечения лиц с латентным токсоплазмозом цитостатиками и иммунодепрессантами. В последние годы важное значение приобрела проблема генерализации латентного токсоплазмоза у ВИЧ-инфицированных. В этих случаях токсоплазмоз приобретает острое злокачественное течение с развитием некротического локализованного или диффузного менингоэнцефалита, в процесс вовлекаются глаза и многие органы (сердце, печень, легкие). На фоне развернутой картины СПИДа наслоившееся обострение (генерализация токсоплазмоза) может приводить к гибели больных.
Основная роль в развитии токсоплазмоза у лиц с иммуносупрессией отводится нарушениям продукции цитокинов. Показано, что при развитии токсоплазмоза на фоне ВИЧ-инфекции резко снижается как концентрация сывороточного гамма-интерферона, так и его способность активировать макрофаги. К факторам защиты относят интерлейкин-12, ФНО-, CD-8+, к факторам, способствующим генерализации заболевания – интрелейкины-4, -6, -10.
В патогенезе манифестных форм хронического токсоплазмоза основную роль играет развитие реакций гиперчувствительности замедленного типа к антигенам токсоплазм и продуктам их жизнедеятельности.
Симптомы Токсоплазмозного энцефалита:
Токсоплазмозный энцефалит служит основной причиной заболеваемости и смертности у больных со СПИДом. Заболеваемость токсоплазмозным энцефалитом среди больных этой категории, имеющих антитела к токсоплазмам, колебалась от 6 до 12%. На основании этого полагают, что имелось приблизительно 170 случаев токсоплазмозного энцефалита среди 7000 больных СПИДом, о которых сообщалось в 1984 г., а развитие еще 150 случаев ожидается среди 7000 больных, которые должны заболеть СПИДом по прогнозу на 1985 г.
Частота случаев токсоплазмозного энцефалита у больных со СПИДом и энцефалитом, как сообщалось, колебалась от 25 до 80%. Диагноз токсоплазменного энцефалита следует иметь в виду у лиц с заболеванием центральной нервной системы, не относящихся к группе риска по СПИДу, так как гетеросексуальная передача вируса лейкоза Т-клеток человека (HTLV III) приводит к развитию СПИДа у лиц, не относящихся к типичным группам повышенного риска.
К внешним признакам и симптомам токсоплазменного энцефалита у больных со СПИДом относят озноб, лихорадку, головную боль, припадки, депрессию и неврологические нарушения; эти проявления могут возникать в сочетании с хориоретинитом. У большинства больных со СПИДом и токсоплазмозным энцефалитом в сыворотке отсутствуют специфические антитела, указывающие на наличие острого токсоплазмоза. Демонстрация повышения титра антител к токсоплазмам в спинномозговой жидкости, но не в сыворотке свидетельствует о токсоплазмозном энцефалите у больных со СПИДом.
Диагностика Токсоплазмозного энцефалита:
В спинномозговой жидкости выявляют плеоцитоз, повышение содержания белка и гипогликорахию; в препаратах из центрифугата спинномозговой жидкости могут быть обнаружены тахизоиты. При исследовании спинномозговой жидкости (или тканей мозга) на наличие вирусов методами культивирования необходимо тщательно контролировать клеточные культуры с целью обнаружения токсоплазм, также способных вызывать формирование бляшек или обширные цитопатические эффекты. Клеточные культуры могут быть окрашены красителем Гимзы.
При компьютерной томографии головного мозга наблюдаются признаки диффузного энцефалита и/или одного или нескольких очагов объемного поражения. Внутривенное введение контрастного вещества может выявить кольцевидные, узелковые, мишеневидные поражения в коре или белом веществе, при этом отмечается тенденция к локализации этих поражений глубоко в пределах базальных ганглиев. В начальной фазе инфекционного процесса отклонения от нормы на сканограммах головного мозга выявляются не всегда; иногда первые признаки нарушений впервые могут появиться спустя несколько недель после заражения.
Исследования с задержкой в 1 ч с двойной дозой контрастного вещества помогают выявить поражения, неразличимые на простых сканограммах. При возможности следует произвести биопсию пораженных участков головного мозга, обнаруженных на сканограммах, так как дифференциальная диагностика этих поражений включает энцефалиты, вызываемые грибками родов Candida и Aspergillus, микобактериями и Cryptococcus neoformans, равно как и многоочаговую лейкоэнцефалопатию и лимфому.
При стандартных методах окраски токсоплазмы обнаруживаются только в 50% биоптатов головного мозга от больных с токсоплазмозным энцефалитом. Однако при использовании специфических иммуногистологических методов окрашивания тахизоиты, цисты и/или антигены токсоплазм обнаруживают в биоптатах, полученных от большинства зараженных больных.
Если у больных СПИДом появляются неврологические признаки или симптомы, а на сканограмме головного мозга очаговых изменений не выявляется, однако отмечается положительный тест Сейбина-Фельдмана или высокий уровень IgG в реакции непрямой флюоресценции антител (НФА), целесообразно проведение пробного лечения токсоплазмозного энцефалита. Если при компьютерной томографии на сканограммах выявляются очаговые нарушения, антитела к токсоплазмам, а проведение биопсии затруднено локализацией очагов поражения или клиническим состоянием больного, следует начать предварительное лечение токсоплазмоза.
В подобных случаях положительный эффект от проводимого лечения, наблюдающийся в течение первых 7- 10 дней, подтверждает диагноз токсоплазмозного энцефалита. Если лечение осуществляли с применением кортикостероидов, признаки улучшения, выявленные рентгенографическими методами, не обеспечивают надежного свидетельства в пользу терапевтического эффекта.
Лечение Токсоплазмозного энцефалита:
При установлении диагноза энцефалита больной должен быть госпитализирован в специализированное (инфекционное) или неврологическое отделение. Назначают строгий постельный режим. Больной нуждается в постоянном наблюдении.
На догоспитальном этапе показано применение дегидратационных средств (лазикс, диакарб).
При выраженных менингеальных и энцефалитических симптомах (сильная головная боль, боль в мышцах, токсикоз, рвота, очаговые симптомы) вводят изотонический раствор натрия хлорида, раствор Рингера-Локка. Одновременно подкожно или внутримышечно вводят витамины группы В, аскорбиновую кислоту (не менее 1,5 г в сутки).
Если стандартная схема лечения с применением хлоридина (по 25 мг в сутки), трисульфапиримидина (по 6 – 8 г) или сульфадизина неэффективна, суточную дозу хлоридина следует увеличить до 50 мг. В случае развития у больного неблагоприятной реакции на сульфаниламидный препарат рекомендуется использовать только пириметамин в дозе 50 мг в сутки. Необходимо применять фолиевую кислоту в дозе до 15 мг в сутки, особенно когда отмечается депрессия костного мозга в результате воздействия хлоридина. Однако если депрессия костного мозга у больных со СПИДом обусловлена иммунными механизмами, профилактический прием фолиевой кислоты не устраняет лейкопению.
Профилактика Токсоплазмозного энцефалита:
Меры по профилактике инвазии включают вмешательство в цикл передачи, и их соблюдение особенно важно для больных с иммунодефицитом и серонегативных беременных женщин. Очень важно, чтобы больные из групп риска знали о том, как можно избежать заражения цистами (плохая кулинарная обработка мяса) и спорулированными ооцистами (при контактах с домашними кошками).
Для уничтожения цист мясо следует прогревать до 60°С или замораживать при – 20°С. (Бытовые морозильные камеры не способны создавать и поддерживать такую температуру.) После приготовления пищи из сырого мяса руки следует тщательно мыть; необходимо также мыть фрукты и овощи, которые могут быть загрязнены ооцистами. Обработка продуктов сухим жаром (66°С) или кипящей водой делает ооцисты неинфективными. Следует избегать контактов с экскрементами кошек.
Данных, позволяющих дать четкие рекомендации относительно использования цельной крови, переливания лейкоцитов или трансплантации органов в случае обнаружения у донора антител против токсоплазм нет. Вместе с тем не следует использовать кровь или продукты крови, полученные от лиц с наличием антител против токсоплазм, для переливания больным с иммуносупрессией, а органы для трансплантации серонегативным реципиентам следует брать от лиц с отрицательными серологическим реакциями на токсоплазмоз.
К каким докторам следует обращаться если у Вас Токсоплазмозный энцефалит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Токсоплазмозного энцефалита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Токсоплазмоз головного мозга – причины возникновения, симптомы и лечение
Ослабленный иммунитет может стать причиной возникновения множества болезней, среди которых выделяют токсоплазмоз. Часто недуг поражает печень, сетчатку глаз, миокард, но основной его целью является центр нервной системы ‒ головной мозг. Узнайте, что такое токсоплазмоз головного мозга, каковы симптомы заболевания, пути заражения и способы лечения.
Toxoplasma gondii ‒ что это
Возбудителем болезни головного мозга является toxoplasma gondii – простейшая одноклеточная паразитарная бактерия, имеющая дугообразный вид, схожий с формой дольки апельсина. Попадая в человеческий организм, toxoplasma gondii размножается в кишечнике и циркулирует в крови. Достигнув внутренних органов, возбудитель провоцирует воспалительный процесс, разрушая клетки и создавая в тканях полости – цисты и псевдоцисты.
Симптомы токсоплазмоза головного мозга
Различают две формы токсоплазмоза – острую и хроническую. Патология не имеет четкой симптоматики, поэтому распознать ее признаки весьма сложно. Острая форма токсоплазмоза мозга встречается редко, поражая людей с очень слабым иммунитетом. Заболевание начинается внезапно, сопровождаясь такими симптомами:
- ознобом, лихорадкой;
- высокой температурой тела;
- мышечной болью;
- тошнотой, рвотой;
- слабостью, снижением трудоспособности;
- увеличением лимфоузлов;
- сильной мигренью;
- потерей чувствительности некоторых областей тела;
- помутнением сознания;
- нарушением движения глаз;
- кожными экзантемами.

Хроническая форма недуга головного мозга может длиться несколько лет бессимптомно, а может систематически проявляться с обострениями и ремиссиями. Выделяют такие симптомы токсоплазмоза мозга в хронической форме:
- раздражительность;
- повышенная утомляемость;
- проблемы с памятью;
- нарушения зрения;
- регулярное повышение температуры;
- депрессию;
- невозможность движения определенных участков тела;
- эндокринные расстройства;
- боли в суставах;
- эпилептические припадки;
- снижение интеллекта.
Причины заражения
Токсоплазмоз мозга делится на два основных вида – приобретенный и врожденный. Часто путем заражения является контакт с домашними животными. Кошки нередко выступают «хозяином» паразита и выделяют его с экскрементами, слюной, молоком. Существуют и другие причины заражения токсоплазмозом:
- касание руками полости рта после контакта с землей;
- употребление плохо проваренного, прожаренного мяса;
- пересадка органов, переливание крови;
- контакт рук с сырым мясом и полостью рта (хозяйки нередко пробуют фарш);
- употребление немытых овощей, зелени, фруктов;
- укус заражёнными насекомыми;
- тесная близость с зараженным острым токсоплазмозом.
Врожденное заболевание передается от инфицированной беременной женщины к ребенку. Если мать заразилась на последнем триместре беременности, патологии у новорожденного могут проявиться в легкой форме. В случаях заражения женщины на ранних сроках вынашивания плода, часто происходят выкидыши. Если же токсоплазмоз возник к концу второго-третьего триместра беременности, ребенок рождается с серьезными отклонениями в работе внутренних органов. Заболевание не передается через плаценту и молоко при вскармливании, если мать была инфицирована еще до беременности.

Диагностика церебрального токсоплазмоза
Клиническая картина болезни очень размыта, поэтому выявить церебральный токсоплазмоз, основываясь только на жалобах больного и учитывая отсутствие выраженных симптомов недуга, почти невозможно. Определить токсоплазмоз головного мозга помогает рентгенография черепа головы, электрокардиограмма, серологические исследования, аллергопробы.
Действенным методом диагностики недуга головного мозга является иммуноферментный анализ. У пациента берут кровь, в которой выявляют антитела iGg и iMg. Наличие iGg обозначает, что пациент выздоравливает или инфекция перетекла в хроническую форму, а iMg указывает на недавнее заражение токсоплазмозом с острым течением болезни. Отрицательный тест на iMg в большинстве случаев свидетельствует об отсутствии инфицирования.
Токсоплазмоз у ВИЧ инфицированных
Иммунитет здоровых людей способен сдерживать развитие инфекции, а вот токсоплазмоз при ВИЧ может привести к серьезным поражениям ЦНС. Ослабленная иммунная система не может сопротивляться болезни – от бессимптомного носительства недуг может привести к летальному исходу. Проблемы с координацией, речью, ходьбой, приступы эпилепсии добавляются у ВИЧ-инфицированных к общим симптомам токсоплазмоза мозга. Решающее значение имеет быстрая диагностика возбудителя на ранних этапах развития токсоплазмы. После прекращения лечения у больных ВИЧ недуг может рецидивировать.
Лечение токсоплазмоза головного мозга
Врач назначает индивидуальное лечение токсоплазмы гондии пациентам с патологией головного мозга в острой форме, ВИЧ-инфицированным, детям и беременным женщинам. Для терапии недуга головного мозга используются антигистаминные средства (Тавегил, Супрастин), антибиотики (Ровамицин, Линкомицина гидрохлорид), химиотерапевтические медикаменты (Фансидар, Делагил). Обязательно применение общеукрепляющего комплекса витаминов.
Народная медицина не сможет полностью заменить традиционную терапию, но пациенты подтверждают эффективность некоторых ее методов. Рекомендуют использовать такие народные способы лечения токсоплазмы гондии, предварительно посоветовавшись с доктором:
- употреблять отвар из молока и зубчиков чеснока;
- выпивать отстоянный чай из полыни, ромашки, горечавки, пижмы, коры крушины;
- принимать измельченные тыквенные семена, залитые молоком;
- есть натертый корень хрена, смешанный со сметаной;
- пить настойку прополиса.

Профилактика
Соблюдение элементарных правил личной гигиены является залогом здоровья. Поскольку домашние животные часто становятся переносчиками паразитов и инфекций, следует тщательно мыть руки после контакта с ними, избегать взаимодействия с уличными кошками. Кроме этого, профилактика токсоплазмоза мозга включает следующие рекомендации:
- не пробовать плохо прожаренное и сырое мясо;
- работая с чужой кровью, следить за стерильностью;
- уточнять качество переливаемой крови;
- хорошо промывать зелень, фрукты, овощи;
- дезинфицировать руки после уборки туалета домашних любимцев, работы с землей;
- тщательно мыть кухонные принадлежности после разделывания мяса;
- уничтожить паразитов в доме, которые могут переносить возбудитель инфекции (мух, тараканов).
Видео: токсоплазмоз
Внимание! Информация, представленная в статье, носит ознакомительный характер. Материалы статьи не призывают к самостоятельному лечению. Только квалифицированный врач может поставить диагноз и дать рекомендации по лечению, исходя из индивидуальных особенностей конкретного пациента.
Токсоплазмоз у человека

Токсоплазмоз – это врожденное или приобретенное заболевание паразитарной природы, поражающее нервную систему, органы ретикулоэндотелиальной системы, зрительный аппарат, скелетные мышцы и миокард.
По сей день эта паразитарная инвазия не теряет своей актуальности и ежегодно, по данным ВОЗ, ею заражаются десятки тысяч человек. Чрезвычайно частая регистрация заболевания связана с тем, возбудитель токсоплазмоза распространен практически повсеместно, причем, с каждым годом опасность инфицирования возрастает на 0,5-1%.
В том случае, когда небольшое количество возбудителя попадает в организм здорового человека, он не представляет большой опасности, так как покрывается плотной оболочкой и превращается в цисту. По оценкам специалистов, порядка полумиллиарда человек на земном шаре имеют антитела к возбудителю этого заболевания.

Что это такое?
Токсоплазмоз — это инфекционное заболевание, вызываемое Toxoplasma gondii. Заболевание может протекать бессимптомно, с проявлениями лимфаденопатии, мононуклеозоподобной симптоматикой, вплоть до поражения центральной нервной системы у иммуноскомпрометированных лиц.
У новорожденных могут быть хориоретиниты, эпиприпадки, умственная отсталость. Диагноз подтверждается серологически, ГЦР и гистологически. Лечение проводится периметамином в сочетании с сульфадиазином или клиндамицином. Глюкокортикоиды применяют при хориоретинитах одновременно с основной терапией.
Возбудитель токсоплазмоза
Возбудитель заболевания — Toxoplasma gondii. Это простейшее отряда кокцидий. Оно подвижно и имеет дугообразную форму. Если взглянуть на этот живой организм под микроскопом, он напоминает дольку апельсина.
Паразит может размножаться половым и бесполым путем. В результате полового процесса, происходящего в кишечнике, образуются цисты. Эти формы очень устойчивы к воздействию факторов внешней среды: не боятся действия низких и высоких температур, высушивания. Вместе с фекалиями эти цисты попадают наружу и приводят к заражению других организмов. Бесполое размножение не приводит к образованию стойких форм паразита.
Можно ли заразиться токсоплазмозом от домашних животных? Да, ведь токсоплазмозом болеют около 60 видов птиц и 300 видов млекопитающих (одомашненных и диких). Однако половой процесс происходит лишь в кишечнике животных семейства кошачьих. За 2 недели заболевания кошка может выделить до 2 миллиардов цист, которые живут во внешней среде до 2 лет.
Формы течения болезни
Токсоплазмоз может быть врожденным и приобретенным, мужчин он поражает реже. При болезни второго типа выделяют три формы течения, о которых подробнее сказано в таблице:
Особенности протекания симптомов
- инкубационный период – несколько недель;
- болезнь протекает тяжело, без своевременного лечения способна привести к смерти;
- продолжительность составляет от недели до нескольких месяцев;
- полноценного выздоровления не происходит, у взрослого человека остаются патологии различной степени тяжести.
- для этой формы характерны постоянные обострения, но протекает она почти без симптомов;
- ремиссии неполные, непродолжительные;
- обострения возникают при ОРВИ, гриппе, приеме иммунодепрессантов, цитостатиков.
- полное отсутствие симптомов;
- токсоплазмоз невозможно выявить.

Симптомы токсоплазмоза
Латентный период инфекции – до двух недель. Симптомы токсоплазмоза у человека в начальном периоде болезни почти не проявляются, либо проходят не замечено. Патогенез заболевания определяет его характер – приобретенный или врожденный, проявляясь острым течением, хроническим и латентным.
- Острое течение болезни характеризуется внезапным началом с выраженной симптоматикой интоксикации организма и лихорадкой, возможным проявлением гепатомегалии (увеличенная печень) и спленомегалии (увеличенная селезенка). Иногда отмечаются кожные высыпания, признаки энцефалита и менингоэнцефалита.
- Течение тяжелое. Осложняется очаговыми или распространенными воспалительными реакциями миокарда, симптоматическим проявлением психоневрологических и когнитивных функциональных нарушений (памяти, умственных функций и т. д) часто со смертельным исходом.
Хроническому течению свойственно длительная вялотекущая картина. Иногда с бессимптомным течением, либо с постепенно нарастающей симптоматикой.
- Хроническим течением интоксикации.
- Длительной субфебрильной температурой (месяц и более).
- Нарушением зрительных функций – развитие прогрессирующей близорукости.
- Симптомами поражения ЦНС (судороги, припадки, истерия, неуравновешенность и мнительность).
- Сбоем в эндокринных функциях – импотенцией, снижением функций щитовидки и надпочечников, изменениями в менструальном цикле.
- Со стороны кардиологических нарушений отмечаются признаки тахикардии, сердечные боли, снижение АД.
- Симптомами поражения ЦНС (судороги, припадки, истерия, неуравновешенность и мнительность).
- У большей половины пациентов с хроническим токсоплазмозом, диагностируется гепатомегалия и спленомегалия. На пальпацию печень отзывается болью. Значительно проявляется ее функциональная патология.
- Увеличением большой группы периферических и мезентериальных лимфоузлов. При прощупывании они вначале мягкие и болезненные, с течением времени болезненность уходит, они уменьшаются, но их структура становиться плотной.
- Мышечными и суставными болями — при мышечных поражениях, кроме воспалительных процессов, в мышечных тканях прощупываются болезненные уплотненные зоны, обусловленные образованием кальцификатов.
- Нарушением функций ЖКТ с проявлением интоксикации, ксеростамии (сухость во рту), апатией к еде, болевым синдромом в зоне эпигастрии, запорами и похудением.
При латентном течении, даже тщательная диагностика способна выявить лишь остаточные старые признаки склерозированных очагов лимфоузлов или кальцификатов в мышечной ткани. Подтвердить диагноз может лишь ПРЦ исследования, либо внутрикожный тест на антитела к токсоплазмозу.
Диагностика
При возникновении тревожных симптомов необходимо как можно скорее обратиться к врачу, чтобы вовремя поставить точный диагноз и блокировать заболевание до того, как микроорганизмы нанесут непоправимый вред организму. Специалисту нужно рассказать обо всех имеющихся признаках токсоплазмоза и про свой образ жизни.
Врач должен пальпировать печень, селезенку и лимфатические узлы – при обостренном токсоплазмозе они увеличиваются. Прослушивание сердца покажет аритмию, а измерение давления – гипотонию. Если имеется риск токсоплазмоза, необходимо сдать венозную кровь на паразитов. Посредством центрифуги будет получена сыворотка (жидкая часть крови), которая будет исследована на наличие специфических антител. При перенесенном процессе будет выявлен иммуноглобулин с маркером G, при остром процессе – с маркером М.
Дополнительно назначаются следующие инструментальные диагностические исследования:
- электрокардиограмма;
- УЗИ брюшной полости;
- рефрактометрия (исследование глаз);
- рентген мягких тканей и легких.
Лечение подбирать можно только после проведения всех необходимых методов диагностики и подтверждения диагноза.
Последствия токсоплазмоза
Наиболее жизненно опасные и тяжелые последствия для здоровья пациента при токсоплазмозе наблюдаются при врожденном генезе заболевания. Часто, инфицирование беременной женщины токсоплазмой в начальном периоде беременности становится причиной антенатальной смертности. Для врожденного токсоплазмоза характерно развитие патоморфологических изменений, прежде всего, в головном мозге, проявляющееся некротизирующим энцефалитом. Ввиду того, что токсоплазменная инфекция склонна к гематогенному и лимфогенному генерализованному распространению, патологические изменения и осложнения заболевания могут проецироваться практически в любой части человеческого организма.
Склонность к осложненному течению токсоплазмоза наблюдается у лиц, страдающих той или иной формой иммунодефицита, и обусловлена активизацией и присоединением вторичного бактериального компонента. Данное течение токсоплазмоза чаще всего встречается в специфической категории ВИЧ-инфицированных пациентов, у которых развивается тяжелая хроническая форма заболевания, нуждающаяся в пролонгированной медикаментозной коррекции.
У относительно здоровых лиц токсоплазмоз не вызывает тяжелых последствий и даже протекает в латентной бессимптомной форме. После перенесенного активного или бессимптомного клинического периода в организме человека происходит формирование стойких иммунных защитных механизмов, предотвращающих вероятность повторного инфицирования токсоплазмой, что особенно важно для женщин, планирующих иметь ребенка.
Как лечить токсоплазмоз?
Для каждого пациента курс лечения токсоплазмоза назначается сугубо индивидуально и длится до тех пор, пока не ликвидируются все клинические проявления болезни, ухудшающие качество жизни человека.
Для того чтобы справиться с недугом, требуются антипаразитарные лекарственные средства, которые чаще всего назначаются в комбинации:
- Пиреметамин;
- Спирамицин;
- Азитромицин;
- Дараприм;
- Сульфадимезин;
- Клиндамицин.
Применяют медикаменты курсами с определенными интервалами в течение длительного срока. Назначают гормональные препараты (глюкокортикоиды) пациентам с наличием поражений органов зрения и нервной системы.
Серьезную угрозу представляет заражение этим недугом для лиц, страдающих иммунодефицитами различного происхождения (напр. ВИЧ-инфекцией) или получающих супрессивную лекарственную терапию. У таких пациентов значительно хуже прогноз, их трудно излечить, им требуются специальные схемы терапии.
При первичном заражении беременной женщины до 17 недель рекомендуют аборт по медицинским показаниям, для плода опасен не только паразит сам по себе, но и медикаменты, применяемые для борьбы с ним. Если это произошло после данного срока, пациентку лечат антипаразитарными препаратами.
Прогноз
Приобретенный токсоплазмоз при адекватном лечении и нормальной работе иммунной системы имеет тенденцию к постепенной регрессии. Выздоровление наступает через 1-4 месяца. После болезни функции пораженных органов могут восстановиться не в полной мере, так как на месте воспалительных очагов формируются зоны рубцевания. В стекловидном теле остается небольшая рубцовая деформация сетчатки.
Рецидивирование поражения глаз и нервной системы имеет вероятность 50%. Необходимо длительное диспансерное наблюдение и профилактика.
В целом прогноз при приобретенном токсоплазмозе остается благоприятным, обеспечивая выздоровление 95% больных. При врожденном токсоплазмозе процент выживаемости новорожденных составляет менее 40%.


