Особенности острого инфаркта миокарда и его симптомы
Острый инфаркт миокарда – омертвение участка сердечной мышцы, вызванное расстройством кровообращения. Инфаркт является одной из главных причин инвалидности и смертности среди взрослого населения.
Причины и механизмы сосудистой несостоятельности сердца
Инфаркт можно считать острой формой ишемической болезни сердца либо ее осложнением.
Особенности работы сердца – постоянные сокращения миокарда – обусловливают очень высокий уровень обменных процессов в его клетках, большое потребление кислорода и питательных веществ. Такой режим деятельности требует бесперебойного притока высокооксигенированной (богатой кислородом) крови, что обеспечивается разветвленной сетью сердечных сосудов, начинающихся от аорты в виде коронарных (венечных) артерий.
Обратной стороной эффективности сердечной мышцы является ее высокая чувствительность к кислородному голоданию. При нарушении питания в миокарде развиваются патологические явления, очень быстро принимающие необратимый характер.
Если недостаток притока крови не носит критический характер, возникает обратимая ишемия (малокровие) участка сердечной мышцы, что проявляется стенокардитическими болями за грудиной. При полном прекращении поступления крови к определенному участку развивается каскад патологических процессов – идет накопление токсических продуктов обмена, которые не выводятся, переход на анаэробный (бескислородный) режим работы с использованием внутренних энергетических запасов клеток.
Собственные запасы энергоносителей (глюкозы и АТФ) очень быстро (примерно за 20 минут) истощаются, и обескровленный участок сердечной мышцы погибает. Это и есть инфаркт миокарда – некроз, размеры которого зависят от уровня перекрытия сосуда (крупной или мелкой ветви), скорости наступления ишемии (при постепенном прекращении подачи крови возможна частичная адаптация), возраста пациента и многих других факторов. Например, острый трансмуральный инфаркт миокарда (с некрозом все толщи сердечной мышцы), имеющий очень тяжелое течение, развивается при окклюзии (перекрытии) крупной ветви коронарного сосуда.
Среди причин нарушения кровоснабжения миокарда чаще всего встречается блок просвета сосуда атеросклеротической бляшкой или тромбом (эти явления могут сочетаться) . Кроме того, возможен резкий спазм коронарных артерий под действием физических (холода) или химических (ядов, лекарств) факторов. Тяжелые анемии, при которых происходит резкое уменьшение содержания в крови гемоглобина, а, следовательно, ее способности к транспорту кислорода, тоже могут служить причиной ишемии миокарда. Несоответствие кровоснабжения возросшим потребностям встречается при резкой гипертрофии сердечной мышцы – кардиомиопатии.
Предрасполагающие факторы развития инфаркта
Некоторые заболевания и патологические состояния являются факторами повышенного риска в плане развития острой ишемии миокарда. К ним относятся:
- Сахарный диабет.
- Гипертоническая болезнь.
- Ишемическая болезнь сердца (ИБС), проявляющаяся приступами стенокардии (особенно ее нестабильные формы).
- Повышенное содержание в крови холестерина и некоторых фракций липопротеинов.
- Чрезмерная масса тела.
- Курение.
- Злоупотребление алкоголем.
- Погрешности в диете (большое потребление соли, животных жиров).
- Сердечная аритмия.
- Длительные стрессовые ситуации.
- Возраст старше 60 лет (хотя в последние годы наблюдается «омоложение» инфаркта).
- Мужской пол (после 70 лет количество мужчин и женщин, страдающих инфарктом, выравнивается).
Классификация ишемического повреждения миокарда
Существуют различные критерии классификации инфаркта. Некоторые из них:
- По размерам зоны повреждения – крупноочаговый и мелкоочаговый.
- По глубине повреждения сердечной мышцы – трансмуральный (на всю толщу сердечной стенки), интрамуральный (некроз в толще стенки), субэндокардиальный (повреждение внутреннего слоя), субэпикардиальный (наружного слоя).
- По топографии – левожелудочковый (передней стенки, задней и боковой стенок, межжелудочковой перегородки), правожелудочковый.
В развитии патологического процесса выделяются несколько периодов, каждый из который имеет свою продолжительность и симптомы.
Предынфарктный период может длиться от нескольких минут до месяцев. Для него характерно учащение приступов стенокардии и усиление их интенсивности.
Острейший период , в котором происходит развитие ишемии и некроз сердечной мышцы, длится до нескольких часов. Может иметь типичный и атипичный вариант течения.
Болевой, или ангинозный вариант, является типичным (около 90% всех случаев). Характеризуется болью за грудиной высокой интенсивности жгучего или давящего характера, которая может иррадиировать (отдавать) в левые конечности, челюсть, шею. Может появиться страх смерти, потливость, побледнение или покраснение кожи лица, одышка. Выраженность боли зависит от величины зоны поражения – крупноочаговый инфаркт вызывает более тяжелые симптомы, чем мелкоочаговый. Боль не купируется приемом нитроглицерина.
Атипичные варианты могут протекать по астматическому типу (иметь симптомы приступа бронхиальной астмы), абдоминальному (с симптомами острого живота), аритмическому (в виде приступа сердечной аритмии), церебральному (с нарушением сознания, головокружением, параличами, расстройством зрения).
Острый период длится около 10 дней. Зона некроза окончательно оформляется и отграничивается, начинается всасывание продуктов распада и формирование рубца. Болевой синдром исчезает или уменьшается. Возможно повышение температуры, явления гипотензии и сердечной недостаточности.
Подострый период (около двух месяцев) – стадия формирования и уплотнения рубца. Болевой синдром отсутствует, состояние постепенно улучшается. Самочувствие в данном периоде во многом определяется характером и объемом изменений, произошедших в сердечной мышце.
Постинфарктный период , или реабилитация (до полугода), характеризуется отсутствием клинических и лабораторных признаков инфаркта (сохраняются изменения на ЭКГ – они останутся пожизненно), однако в этой фазе возможно развитие сердечной недостаточности, стенокардии напряжения и повторного инфаркта.
Осложнения инфаркта миокарда
Острая ишемия миокарда, сама по себе являясь тяжелым состоянием, может еще более утяжеляться присоединением осложнений.
Наиболее частые осложнения:
- Нарушения сердечного ритма (пароксизмальная тахикардия, экстрасистолия, мерцательная аритмия). Такая ситуация, как появление мерцания желудочков с переходом в их фибрилляцию, может стать причиной гибели пациента.
- Сердечная недостаточность связана с нарушением деятельности левого желудочка по перекачиванию крови по сосудам. Она может привести к отеку легких, кардиогенному шоку и смертельному исходу на фоне резкого падения давления и прекращения почечной фильтрации.
- Тромбоэмболия легочной артерии способна привести к пневмонии, инфаркту легкого и смерти.
- Тампонада сердца может произойти при разрыве сердечной мышцы в зоне инфаркта и прорыве крови в полость перикарда. Состояние является опасным для жизни, при котором требуется неотложная помощь.
- Острая аневризма сердца – выбухание участка рубцовой ткани при обширном поражении миокарда. В дальнейшем может стать причиной развития сердечной недостаточности.
- Тромбоэндокардит – отложение фибрина на внутренней поверхности сердца. Его отрыв способно стать причиной инсульта, мезентериального тромбоза (закрытия ветви сосуда, питающего кишечник) с последующим омертвением участка кишки, повреждения почек.
- Постинфарктный синдром – общее название отдаленных осложнений (перикардита, плеврита, артралгии).
В диагностике инфаркта имеют значение данные анамнеза (обстоятельства течения заболевания и предшествующей жизни, выясняемые при опросе больного и его родственников), лабораторных и инструментальных методов исследования.
Выясняются имевшиеся в прошлом приступы болей за грудиной различной частоты и интенсивности, факторы риска (курение, стрессы, хронические болезни). При осмотре возможно выявление избыточного веса, косвенных признаков повышенного давления (капиллярная сеть на лице) и др. Загрудинная боль, длящаяся более 20 минут, считается одним из диагностических критериев инфаркта.
Лабораторные методы исследования при инфаркте выявляют следующие изменения:
- Клиника крови. Лейкоцитоз (увеличение количества лейкоцитов), повышение СОЭ.
- Биохимия крови. Повышение активности ферментов АлТ, АсТ, ЛДГ, креатинкиназы, миоглобина, что является показателем повреждения сердечной мышцы. Возможно изменение уровня электролитов, железа.
Инструментальные методики исследования
- ЭКГ – характерные признаки инфаркта (отрицательный зубец T, патологический комплекс QRS и др.). Снятие кардиограммы в разных отведениях помогают определить локализацию некротического очага (например, передней или задней стенки левого желудочка и т.п.).
- ЭхоКГ – локальное (ограниченное) нарушение сократимости пораженного желудочка.
- Коронарная ангиография – выявляется сужение или перекрытия сосуда, питающего миокард. Следует отметить, что при проведении данного метода исследования его можно использовать и для оказания помощи (после подачи контрастного вещества через тот же катетер в сосуд вводится лекарственный препарат или устанавливается стент-расширитель).
Лечение инфаркта миокарда
Неотложная помощь (проводится непосредственно во время болевого приступа и далее в специализированной клинике):
- Обеспечение больному полного покоя.
- Дача сублингвально (под язык) нитроглицерина и корвалола внутрь.
- Немедленная транспортировка для дальнейшего лечения в отделение кардиологической реанимации (желательно на специализированном реанимационном транспорте).
- Купирование болевого синдрома (применяются наркотические анальгетики и нейролептики).
- Растворение тромба, находящегося в коронарном сосуде, путем введения специальных тромболитических средств (стрептаза, кабикиназа). Метод очень эффективен, но имеет ограниченность по времени – помощь должна быть оказана в течение первого часа после приступа, в дальнейшем процент спасенной массы миокарда стремительно падает.
- Антиаритмические препараты.
- Улучшение обменных процессов в сердечной мышце.
- Снижение объема циркулирующей крови для уменьшения нагрузки на сердце.
- Хирургические методы лечения – баллонная ангиопластика коронарных сосудов, введение стента (трубчатой распорки), аортокоронарное шунтирование (обеспечение обходного кровотока путем наложения шунта на поврежденный сосуд).
- Антикоагулянты (гепарин, аспирин) для уменьшения свертывания крови и профилактики тромбообразования.
Прогноз при инфаркте всегда серьезный и зависит от объема пораженного миокарда, локализации некротического очага (например, при вовлечении в зону повреждения проводящей системы сердца прогноз ухудшается), возраста пациента, сопутствующих заболеваний, своевременности лечения, наличия осложнений и др. Высок процент остаточных явлений и возникновения инвалидности.
После прохождения острого периода пациентам показана реабилитация с постепенным повышением уровня нагрузок. В дальнейшем необходимо врачебное наблюдение, профилактический прием антиангинальных препаратов.
Профилактикой инфаркта служит отказ от вредных привычек, борьба с избыточным весом, рациональный режим питания, труда и отдыха, своевременное лечение при появлении стенокардитических болей.
Что такое субэндокардиальный инфаркт миокарда

Сердечно-сосудистые заболевания являются довольно распространенными и часто встречающимися на сегодняшний день. Они очень серьезны и могут стать большой угрозой не только для оптимального здоровья и активности, но и для жизни больного.
Зачастую подобные заболевания проявляются не сразу, что и делает их особо опасными. Симптоматика на ранних стадиях практически не ощутима, присутствует только небольшой дискомфорт, который может «списываться» больным на самые различные обстоятельства. Пациент не обращается к специалистам, просто не имея представления о наличии серьезного заболевания.
Недуг быстро развивается и стремится к точке невозврата. После ее достижения полностью устранить причины и проявления приступа невозможно даже с помощью высококвалифицированной медицинской помощью.
Довольно часто встречающейся формой заболеваний сердца и сосудов является острый субэндокардиальный инфаркт миокарда. Все больше людей обращаются в медицинские учреждения с данным недугом. Особой проблемой является то, что данная форма инфаркта поражает не только пожилых людей. Она характерна и для молодых, что ранее не встречалось и вовсе. Это говорит только о распространении заболевания и стремительном ухудшении качества здоровья людей до 30 лет с каждым годом.

Зоны поражения сердца и субэндокардиальный инфаркт миокарда на ЭКГ
Особенности субэндокардиального инфаркта миокарда
Если сравнивать инфаркт миокарда с типичными изменениями на ЭКГ и субэндокардиальный вариант, то для последнего характерно:
- до инфаркта больные страдают стенокардией, имеют распространенное поражение коронарных артерий;
- площадь повреждения меньше;
- в зоне разрушения есть больше функционирующих сосудов;
- вокруг очага некроза большая зона жизнеспособных мышечных волокон, но они имеют электрическую нестабильность, что провоцирует аритмии;
- реже развивается недостаточность кровообращения и летальный исход;
- снижение ST и изменение направления Т на ЭКГ;
- отдаленные последствия хуже, чаще бывают рецидивы.
Рекомендуем прочитать статью о заднебазальном инфаркте миокарда. Из нее вы узнаете о причинах развития патологии и ее симптомах, диагностике инфаркта, методах лечения и возможных последствиях при его отсутствии. А здесь подробнее о постинфарктном кардиосклерозе.
Описание заболевания
Данная форма инфаркта миокарда является серьезной патологией. Она выражается в сильном давлении на отдельные участки сердечной мышцы, которая называется миокардом. В следствие этого нарушается оптимальный для здорового человека сердечный ритм, значительно ухудшается обеспечение сердца и других жизненно важных органов кровью.
Основной особенностью субэндокардиального инфаркта миокарда является большая площадь пораженного участка. Воспалительный процесс развивается очень быстро, что приводит к серьезным последствиям.
Причины и факторы риска
Субэндокардиальный инфаркт развивается на фоне таких патологических процессов:
- формируется тромб на холестериновой бляшке, который не полностью останавливает движение крови;
- мелкие части тромба или бляшки закупоривают венечные артерии небольшого диаметра;
- стенки сосудов воспалены из-за повреждения окисленными жирами или присоединения инфекции;
- иммунные клетки на поверхности бляшки выделяют ферменты, которые ее разрушают;
- имеется спазм сосудов (например, при вариантной стенокардии Принцметала);
- нарушаются защитные свойства внутренней оболочки артерий;
- бывает сужение просвета из-за уплотнения стенок сосудов;
- возникает повторный стеноз после стентирования;
- происходит расслоение стенок.

Для того чтобы появились подобные изменения в сосудах сердца, пациент должен входить в одну из категорий риска:
- отягощенная наследственность по ишемии миокарда – кровные родственники имели стенокардию или инфаркт до 55 лет (мужчины), или до 65 — 70 лет по женской линии;
- возраст после 55 лет для женщин и 45 – для мужчин;
- ранняя менопауза у женщин;
- гипертоническая болезнь или симптоматические гипертензии;
- дислипидемия – повышение холестерина и липопротеинов низкой плотности, снижение комплексов с высокой плотностью;
- слабая двигательная активность;
- ожирение, метаболический синдром;
- сахарный диабет, нарушенная толерантность к углеводам;
- избыток животного жира, поваренной соли и дефицит растительной клетчатки;
- курение,
- ежедневное или систематическое употребление алкоголя выше 20 г в пересчете на чистый этанол;
- хронические психоэмоциональные нагрузки или острый стресс;
- частота сердечных сокращений в состоянии покоя выше 90 ударов в минуту;
- повышенная склонность к образованию тромбов;
- возрастание концентрации гомоцистеина в крови;
- холерический темперамент;
- сильное физическое перенапряжение, особенно при низкой тренированности.
Чаще всего инфаркты возникают утром, что связано с повышением давления и свертывающей активности крови, частоты пульса, выбросом гормонов стресса.
Замечено, что при похолодании и любых существенных колебаниях атмосферного давления риск первого инфаркта выше на 10%, а второго – почти на треть.
Клинический случай
74-летняя женщина, страдающая ожирением, была госпитализирована к нам в отделение с повторными эпизодами боли в груди на протяжении последних нескольких дней. Ниже на фото размещен результат ЭКГ, зарегистрированный после нагрузки. Во время записи пленки пациентка начала жаловаться на возникновение дискомфорта в груди.
После введения «Нитроглицерина» пациентке стало лучше, ей была повторно записана ЭКГ.
Коронарография, проведенная пациентке, показала наличие тяжелого стеноза правой венечной артерии.

Проявления на кардиограмме
Субэпикардиальная ишемия на ЭКГ будет видна отрицательными, симметричными и пиковыми Т-зубцами в отведениях, которые соответствуют расположению пораженной области миокарда.Т-волны могут быть динамическими, проявляющимися только во время боли, а также регрессирующими самостоятельно или после введения «Нитроглицерина».
Периоды и симптомы
В течение инфаркта сердечной мышцы выделено несколько периодов, каждый из которых имеет характерные признаки.
Продромальный
Из-за разрушения покрышки атеросклеротической бляшки на ее поверхности образуется кровяной сгусток, он нарушает приток крови к клеткам сердца, что клинически проявляется в виде:
- учащения сердечной боли;
- снижения уровня физической нагрузки, которая вызывает приступ;
- появления болевых ощущений в состоянии покоя;
- для купирования нужна все большая дозировка нитратов.
Эти признаки означают нестабильную стенокардию или предынфарктное состояние. При отсутствии госпитализации и интенсивной терапии просвет артерии перекрывается, развивается инфаркт.
Острейший
В это время отмечаются самые тяжелые признаки инфаркта, возможен смертельный исход, но одновременно начальный период оптимален для растворения тромба и восстановления коронарного кровотока. Симптомы могут быть типичными:
- интенсивная давящая или пронзающая боль в грудной клетке, не меняется при движении и дыхании;
- волнообразное распространение боли на левую половину тела (рука, лопатка, спина, челюсть), иногда бывает и правосторонней, в подложечной области;
- приступ не снимается 3 таблетками Нитроглицерина;
- длительность загрудинной боли – от получаса до нескольких часов;
- сильная слабость;
- холодный пот;
- возбуждение;
- тревожность, страх смерти.
Атипичное течение субэндокардиального инфаркта сопровождается:
- безболевыми эквивалентами – тяжесть или ноющие ощущения в груди, тревога, нарушение сна, общая слабость, разбитость;
- аритмией – перебои ритма, устроение или замедление пульса, головокружение, обморок;
- приступами удушья;
- болезненностью живота, вздутием, тошнотой, рвотными позывами;
- атипичной болью в других частях тела или с иными характеристиками болевого синдрома;
- нарушением мозгового кровообращения – обморочное состояние, головная боль, тошнота, рвота, слабость в левой руке;
- отсутствием симптомов (диагностируется по ЭКГ ретроспективно).

Острый
Миокард разрушен, поэтому боль стихает. Бывают приглушенные неприятные ощущения за грудиной. Из-за распада клеток в кровь поступают ферменты, вызывающие повышение температуры тела, усиление слабости и потливости. Падает артериальное давление. Возможен повторный инфаркт или расширение зоны первого. Важно соблюдение постельного режима.
Подострый
Основные симптомы связаны со снижением сократительной способности сердечной мышцы – отеки на ногах, застой крови в легких, одышка. При неосложненном течении нормализуется ритм сердца, температура тела, показатели кровообращения – артериальное давления и частота пульса. Начинается образование в зоне повреждения рубца.
Период рубцевания
Волокна соединительной ткани становятся более прочными, улучшается состояние пациентов, не возникает боли, или стенокардия имеет стабильное течение.
Смотрите на видео о симптомах инфаркта миокарда и его лечении:
Совет специалиста
Известно, что субэндокардиальная ишемия затруднительна для диагностики и не так часто фиксируется на ЭКГ, поскольку возникает на ранних этапах нарушения кровоснабжения сердечной мышцы и пациент еще не предъявляет никаких жалоб. Более того, необходимо проводить дополнительные обследования, поскольку есть некоторые патологии с такими же признаками на кардиограмме:
- субэпикардиальная ишемия задней стенки миокарда (правые отведения);
- гиперкалиемия (калий в крови выше 6 мэкв/л) — зубцы T острые, укорочен интервал QT;
- алкоголизм (признаки алкогольной кардиомиопатии еще могут не проявляться);
- когда перегружен левый желудочек в диастолу, например при аортальной регургитации, на пленке нередко появляются высокие зубцы T в левых отведениях;
- вариант нормы при ваготонии — асимметричный, высокий T.
Осложнения
Возникают при крупных очагах инфаркта, нарушении электролитного состава крови, продолжающейся ишемии или дисбалансе отделов вегетативной нервной системы. Проявляются в виде:
- чередования тахикардии и замедленного ритма;
- нарушения проводимости сердечного импульса;
- экстрасистол;
- тяжелых форм нарушения ритма – полная атриовентрикулярная блокада и фибрилляция желудочков с остановкой сердца;
- недостаточность кровообращения по право- и левожелудочковому типу, комбинированная;
- кардиогенный шок;
- аневризма;
- разрыв сосочковой мышцы (митральная недостаточность), стенки сердца, перегородки;
- тромбоэмболия;
- перикардит изолированный или с плевритом, артритом, пневмонитом (синдром Дресслера);
- психические расстройства;
- атония мочевого пузыря (чаще при гипертрофии простаты).
ЭКГ и другие методы диагностики
Так как очаг расположен под внутренней оболочкой сердца, то зубец Q не формируется, а следующие признаки можно обнаружить в грудных отведениях, первом стандартом и от левой руки:
- снижение ST куполообразное, обращенное вершиной вниз;
- изменение направления Т или двухфазная конфигурация;
- уменьшенная амплитуда R.
Эксперт в области кардиологии
Встречаются случаи нормальной ЭКГ при субэндокардиальном инфаркте. У таких пациентов может быть типичные симптомы инфаркта и изменение анализов крови. Наиболее сложный вариант – атипичная клиническая форма и отсутствие ЭКГ-признаков. Если не провести лабораторную диагностику, то подозрение в отношении инфаркта возникают крайне редко.
Изменения кардиоспецифических ферментов имеют динамику появления и исчезновения:
- первые часы повышен миоглобин, пик – 6 — 10 часов, нормализация к концу суток;
- с 3 часа до 6 возрастает КФК-МВ и тропонин, достигают максимума к 20 часу, креатинфосфокиназа снижается на 2 — 3 сутки, тропонин – на 7 — 12 день.
Если повышение не достигает 50 — 100 процентов, а снижения в соответствующее время нет, то диагноз инфаркта миокарда может быть сомнителен. Коронарография проводится для определения проходимости коронарных артерий, как правило, перед выбором хирургического метода реваскуляризации.

Лечение субэндокардиального инфаркта миокарда
Терапия при подозрении на инфаркт миокарда начинается на этапе неотложной медицинской помощи, продолжается в стационаре в условиях реанимации или отделения интенсивной терапии. Используют:
- ингаляции кислорода;
- нитраты (Изокет, Перлинганит);
- обезболивающие (Морфин, Дроперидол, Фентанил);
- антиагреганты (Аспирин – первая доза 300 мг, Клопидогрел, Коплавикс, Брилинта);
- антикоагулянты (Арикстра, Клексан, Ангиокс);
- бета-блокаторы при тахикардии и гипертонии (Беталок, Эгилок).
Для восстановления кровотока в первые часы развития инфаркта может быть проведен тромболизис (медикаментозное растворение тромба) или баллонное расширение коронарной артерии с последующим стентированием. Множественное поражение венечных сосудов является показанием к аортокоронарному шунтированию.
Инфаркт миокарда: клиника, диагностика, лечение
Острый инфаркт миокарда (ИМ) — клинический синдром, возникающий в результате повреждения сердечной мышцы при несоответствии между потребностью миокарда в кислороде и возможностью его доставки. При этом возникает некроз кардиомиоцитов в зоне поврежде
Острый инфаркт миокарда (ИМ) — клинический синдром, возникающий в результате повреждения сердечной мышцы при несоответствии между потребностью миокарда в кислороде и возможностью его доставки. При этом возникает некроз кардиомиоцитов в зоне повреждения одновременно, что отличает данный процесс от других форм миокардиального повреждения.
Этилогия и патофизиология. Факторами риска являются гиперхолестеринемия, сахарный диабет, артериальная гипертензия, малоподвижный образ жизни, семейный анамнез, табакокурение и другие.
Основным в процессе принято считать атеросклероз коронарных артерий, включающий в себя разрыв или деэндотелизацию атеросклеротической бляшки, тромбоз, вазоконстрикцию, часто на фоне воспаления. Важную роль также играет нарушение свертываемости крови, уменьшение коронарного кровотока и недостаточная его компенсация коллатеральным кровообращением, нарушение обмена простагландинов, функции калликреин-кининовой системы, иммунологические нарушения. Независимо от причины, ИМ характеризуется наступлением необратимой гибели клеток миокарда. Зона инфаркта, которая изначально охватывает субэндокардиальный слой миокарда, начинает распространяться на более глубокие слои, направляясь к эпикарду. Даже при тотальной окклюзии коронарного сосуда, снабжающего зону инфаркта, наблюдается некоторый антеградный кровоток, что может позволить сохраниться в зоне поражения жизнеспособным кардиомиоцитам, поэтому считается, что существует временной период до 6–12 часов, когда возможно повлиять на размер зоны некроза путем увеличения кровотока в поврежденном участке.
У более 50% больных тотальная коронарная окклюзия развивается в области ранее существующей атеросклеротической бляшки. Тотальная окклюзия чаще развивается в проксимальных сегментах крупных артерий, что впоследствии на ЭКГ проявляется патологическими зубцами Q. При отсутствии тотальной тромботической окклюзии коронарного сосуда чаще возникает Q-необразующий ИМ (по ЭКГ).
Развитие ИМ сопровождается нарушением систолической и диастолической функции и ремоделированием левого желудочка (ЛЖ). Нарушение систолической функции обусловлено тем, что некротизированный участок миокарда не участвует в сокращении сердца, тогда как в неповрежденной ближайшей зоне имеется компенсаторная гиперкинезия. Диастолическая дисфункция связана со снижением эластичности и растяжимости миокарда. В результате диастола ЛЖ неполноценна, миокард недостаточно релаксируется, повышается конечное диастолическое давление. Данные нарушения возникают при поражении менее 10% массы миокарда левого желудочка. Ремоделирование ЛЖ обусловлено истончением миокарда и снижением тонуса миокарда в области некроза, компенсаторным расширением полости ЛЖ, развитием состояния гибернации в периинфарктной зоне, активизацией циркулирующей и местной ренин-ангиотензиновой и симпатоадреналовой системы, гиперпродукцией эндотелина. Ремоделирование сердца после ИМ может носить адаптивный и дезадаптивный характер. Адаптивный характер проявляется в уменьшении размеров ЛЖ, поддержании удовлетворительной сократительной способности ЛЖ, стабилизации миокардиального стресса. Сохраняется гемодинамически выгодная форма ЛЖ, поддерживается удовлетворительная сократительная способность ЛЖ и стабилизация миокардиального стресса. Дезадаптивный характер процесса ремоделирования ЛЖ заключается в прогрессированной дилатации ЛЖ с переходом к гемодинамически невыгодной сферической форме сердца, что приводит к развитию рестриктивного типа диастолического наполнения ЛЖ. Этот тип дисфункции является мощным предиктором сердечно-сосудистой смертности.
Клиническая картина. Проявления ИМ имеют множество вариантов. От бессимптомного течения и эпизодического дискомфорта в области сердца до развернутого болевого приступа с различными нарушениями ритма и проводимости. Чаще описываются ощущения «давления», «тяжести» и «жжения» в центральной части грудной клетки с иррадиацией в плечевой пояс, руку, челюсть, эпигастральную область. Больной беспокоен, прикладывает руку к грудине (симптом Левайна). Для пожилого больного с множественной сопутствующей патологией ИМ часто проявляется в признаках сердечной недостаточности (нарастание одышки, отеков, появление сердцебиения, атипичность стенокардитической боли).
Физикальные исследования варьируют от полной нормы до выраженных отклонений (расширение верхушечного толчка, появление 3 и 4 тона, ослабление тонов, появление влажных хрипов в легких и др.). Ни один из этих признаков не подтверждает, но и не исключает наличие ИМ. Диагностика ИМ основана на выявлении маркеров повреждения сердечной мышцы.
Маркеры повреждения кардиомиоцитов. В настоящее время наиболее убедительным маркером является тропонин. Он имеет более высокую чувствительность к ИМ, чем МВ-фракции креатинфосфокиназы (МВ-КФК). Современные методы анализа позволяют наделять тропонин практически абсолютной кардиоспецифичностью, но, учитывая это качество, тропонин может быть повышен и при неишемическом повреждении миокарда. Поэтому только комплексный подход (клинические данные, эхокардиографические и др.) позволяют доказать острую ишемию миокарда и развитие ИМ. Уровень тропонина повышается в первые 4–6 часов и держится повышенным в пределах 8–12 дней. Длительность выявления маркера позволяет диагностировать ИМ в поздние сроки, без исследования лактатдегидрогеназы (ЛДГ). Для более точного ориентирования в сроках ИМ целесообразно исследовать «короткоживущие» маркеры некроза. «Ранним» маркером некроза миокарда является повышение активности МВ-КФК. Активность МВ-КФК повышается в первые часы повреждения миокарда и превышает нормальные показатели между 6–12 часами болезни, достигая пика к 18–24 часу заболевания, а к 48 часу показатели маркера возвращаются к нормальным. Необходимо помнить о других причинах повышения МВ-КФК: повреждение скелетной мускулатуры, хронические миопатии, почечная недостаточность, гипотиреоз за счет снижения клиренса, а также то, что соотношение МВ-КФК и общей КФК не считается критерием диагностики ИМ.
Электрокардиография. Наиболее значимыми признаками ИМ являются изменения сегмента ST (подъем с выпуклостью вверх). При нижней локализации ИМ следует фиксировать ЭКГ на правой половине грудной клетки в отведениях V3R или V4R. Для огибающей окклюзии характерны изменения в так называемых задних отведениях (V7–V9), чаще в виде появления патологического зубца Q. При этом вышеуказанные признаки нельзя считать 100% обязательными. В большинстве случаев типичные изменения ЭКГ отсутствуют, что может быть обусловлено наличием нарушения внутрижелудочковой проводимости или изолированной депрессией сегмента ST.
Эхокардиография (ЭхоКГ). Диагностическая точность ЭхоКГ зависит от качества получаемого изображения. Отсутствие патологии при ЭхоКГ не может служить основанием для исключения ишемической болезни сердца или некроза сердечной мышцы. ЭхоКГ не позволяет отличить свежий очаг асинергии от зоны постинфарктного кардиосклероза. Исследование незаменимо для исключения осложнений ИМ и сопутствующей патологии.
Лечение. Для достижения максимального положительного результата лечение должно начинаться как можно раньше, начиная с первого часа заболевания, что позволит иметь значительно лучший прогноз. Как можно раньше должна быть проведена реперфузионная терапия путем тромболизиса или первичной ангиопластики. Доказано, что рано начатое лечение приводит к существенному снижению смертности при всех формах ИМ. Первичная ангиопластика на инфаркт-ассоциированной артерии в первый час заболевания позволяет восстановить естественную перфузию миокарда в зоне повреждения Чем позже проведена реперфузия, тем выше смертность. В настоящее время доступность ангиопластики остается невысокой.
В 1996 году Европейским обществом кардиологов и Американской коллегией предложены рекомендации по лечению больных острым инфарктом миокарда, состоящие из ряда принципиальных позиций.
1. Болевой синдром имеет важнейшее значение для течения ИМ. Чем выраженнее и продолжительнее болевой синдром, тем больше опасность развития тяжелых осложнений. При отсутствии противопоказаний со стороны гемодинамики для купирования ангинозного приступа можно использовать сублингвальную форму нитроглицерина (НТГ). В отдельных случаях это позволяет получить регресс острых ишемических изменений на ЭКГ. При этом следует с осторожностью использовать НТГ при нижней локализации ИМ, т. к. может развиться тяжелая артериальная гипотония. НТГ также может вызвать сосудистый коллапс и резкое урежение сердечного ритма (вазовагальная реакция). При получении эффекта от сублингвального НТГ можно применить внутривенную инфузию данного препарата в низких дозах (5–10 мкг/мин). Применение НТГ не исключает использования анальгетиков. Не рекомендовано использование мощных вазодилататоров (например, антагонистов кальция) из-за возникновения тяжелой гипотонии и рефлекторной тахикардии. При отсутствии быстрого обезболивающего эффекта от НТГ назначают наркотические анальгетики — морфин гидрохлорид в/в до 10 мг с повторением введения препарата до полного купирования болевого синдрома. Помимо основного эффекта морфин способствует уменьшению пред- и постнагрузки на сердце, уменьшает давление в сосудах малого круга кровообращения. Из побочных эффектов основными являются гипотония и относительная брадикардия, угнетение дыхательного центра, тошнота и рвота. С целью обезболивания используют также Промедол.
Для усиления обезболивающего эффекта используют сочетание морфина и нейролептика, чаще дроперидола, обладающего также мощным противорвотным эффектом. Для больных пожилого возраста данные схемы нужно использовать с осторожностью из-за сопутствующей патологии, т. к. часто возможны нарушения функции дыхания. Для данной возрастной группы больных рекомендуется применение комбинации наркотического анальгетика и транквилизатора, например, Фентанила 0,005% 2 мл и Седуксена 0,5% 2 мл.
Большим достижением в обезболивании некупирующегося ангинозного приступа стала эпидуральная блокада. Широкое применение затруднено из-за развития специфических осложнений и наличия технических трудностей при ее выполнении.
Применение ингаляционных средств наркоза в настоящее время используется редко, только по определенным показаниям (проведение кардиоверсии, искусственная вентиляция легких, выполнение болезненных манипуляций).
2. Восстановление кровотока (реканализация) по инфаркт-ассоциированной артерии существенно уменьшает размеры зоны поражения миокарда. Эффективность тромболитической терапии (ТЛТ) прямо зависит от времени начала лечения. Желательно, чтобы время обращения за помощью и начало ТЛТ не превышало 90 минут. Показанием к ТЛТ считается наличие смещения сегмента ST вверх от изоэлектрической линии более 0,1 мВ не менее чем в двух смежных отведениях ЭКГ или блокады ножки пучка Гиса у больных, поступивших в первые 12 часов после появления симптомов ИМ. Однако при сохранении боли и указанных выше изменений на ЭКГ считается целесообразным проведение ТЛТ и в более поздние сроки (вплоть до 24 часов после начала заболевания). Под блокадой ножки пучка Гиса подразумевается вновь возникшая или предположительно вновь возникшая полная блокада левой ножки пучка Гиса, затрудняющая интерпретацию ЭКГ. Наиболее доступным с доказанной эффективностью считается препарат стрептокиназа. Препарат активизирует плазминоген непрямым способом. Препарат не следует назначать пациентам, которые перенесли ранее тяжелую стрептококковую инфекцию или которым данный препарат вводился в течение последних 5–6 месяцев. Быстрое введение стрептокиназы может вызывать резкое снижение артериального давления. Рекомендуемая доза стрептокиназы составляет 1500000 ЕД в течение часа.
Урокиназа является прямым активатором плазминогена, имеет короткий период полувыведения, вызывает более быстрое восстановление проходимости инфаркт-ассоциированной артерии, чем эквивалентная доза стрептокиназы. Рекомендуемая доза 2000000 ЕД болюсно и 3000000 ЕД в/в капельно в течение 90 минут.
Тканевой активатор плазминогена (ТАП) считается фибрин-специфичным активатором плазминогена. По сравнению со стрептокиназой и урокиназой ТАП способствует более раннему восстановлению проходимости инфаркт-ассоциированной артерии, возможно, именно этот фактор обусловлено снижает смертность при его использовании. Режим назначения ТАП 100 мг в/в в течение 3 часов: 10 мг болюсно, далее 50 мг в течение первого часа и еще 40 мг в течение последующих 2 часов. При массе тела пациента менее 65 кг назначается препарат в дозе 1,25 мг/кг (за 3 часа), при этом 10% от общей дозы должны быть введены в виде первичного болюса. Применение более высоких доз (больше 100 мг) ТАП ассоциировано с риском внутричерепного кровотечения.
С течением времени были синтезированы и другие ТАП с несколько иным молекулярным строением: ретеплаза, тенектеплаза.
Противопоказания к применению ТЛТ определяются риском возникновения серьезных кровотечений, в особенности внутричерепных. Существуют абсолютные противопоказания: активное внутреннее кровотечение, любой сосудистый эпизод в течение последних 2 месяцев, новообразование центральной нервной системы, тяжелая травма, хирургическое вмешательство в течение 3 месяцев, беременность, тяжелая артериальная гипертензия. К относительным противопоказаниям относят подозрение на расслоение аорты, сердечно-сосудистую реанимацию в течение 2 недель, злокачественные новообразования, язвенную болезнь в стадии обострения, нарушения гемостаза, системные заболевания, эндокардит и ряд других заболеваний. Следует индивидуально решать вопрос по проведению ТЛТ у больных старшего возраста, в связи с наличием большого количества сопутствующей патологии.
Сопутствующее лечение
Аспирин необходимо назначать всем больным с подозрением на ИМ, при отсутствии противопоказаний. Его положительное влияние на выживаемость, частоту реинфарктов и ишемических инсультов продемонстрировано как при проведении ТЛТ, так и в ее отсутствие. При сочетании Аспирина с ТЛТ эффективность последней значительно возрастает. Доказано, что Аспирин ингибирует агрегацию тромбоцитов и ускоряет фибринолиз. Поэтому всем больным ИМ следует назначать Аспирин немедленно в дозе 160–325 мг (разжевывать).
Гепарин при внутривенном введении совместно с активаторами плазминогена способствует ускорению проходимости инфаркт-ассоциированной артерии, особенно при использовании ТАП. При использовании стрептокиназы внутривенная инфузия гепарина не является столь необходимой. Стандартная схема гепаринтерапии предлагает первоначальное болюсное введение 5000 ЕД нефракционированного гепарина, а затем инфузию со скоростью 1000 ЕД/час, пока активированное частичное тромбопластиновое время (АЧТВ) не увеличится в 1,5–2 раза по сравнению с исходным. В связи с трудностями точной титрации данной формы гепарина, рекомендуется использовать низкомолекулярные гепарины (НМГ) с расчетом дозы на кг веса пациента.
β-блокаторы снижают риск повторного ИМ у больных, пролеченных тромболитической терапией. β-блокаторы снижают риск смерти, модулируют нейрогуморальные и гормональные системы, замедляют ремоделирование сердечно-сосудистой системы, вызывают нормализацию функционального состояния тромбоцитов. Рекомендуется применять препараты данной группы в первые 12 часов после начала ИМ у всех больных, не имеющих противопоказаний (бронхиальная астма, сахарный диабет, брадикардия, гипотония). Используются суточные доза метопролола, пропранолола.
Ингибиторы ангиотензин-превращающего фермента (иАПФ). Сердечная недостаточность (СН) является частым осложнением и одной из основных причин смертности в острый период ИМ и в отдаленные сроки после его развития. Возникновение и прогрессирование СН у больных, перенесших ИМ, связано с процессом ремоделирования миокарда ЛЖ, патофизиологический процесс которого запускается уже в первые часы заболевания. Повреждение клеточных и структурных компонентов миокарда и расширение зоны инфаркта предрасполагает к дилатации и дисфункции ЛЖ, которая определяет высокую смертность больных ИМ. Изменения в структуре ЛЖ в первые 3 дня, а в последующем пролиферация фибробластов и синтез коллагена приводят к прогрессированию ремоделирования сердца. Активным участником этих процессов являетcя ангиотензин II, вызывающий спазм коронарных артерий, увеличение работы сердца, повышение потребления миокардом кислорода, а в последующем пролиферацию фибробластов. Таким образом, появились теоретические основания для использования иАПФ при ИМ. Ингибиторы АПФ, уменьшая синтез ангиотензина II, вызывающего вазоконстрикцию как артериального, так и венозного сосудистого русла, способствуют нормализации центральной и периферической гемодинамики, тем самым предотвращают развитие кардиогенного шока, снижая нагрузку на сердце существенно, подавляют процесс ремоделирования ЛЖ. Однако применение иАПФ в остром периоде ИМ ограничивается риском снижения системного артериального давления (АД). В связи с этим, несмотря на доказанную эффективность иАПФ, не утратил своей актуальности поиск безопасных препаратов данной группы, пригодных для применения с первых суток ИМ в сочетании с ТЛТ. К препаратам, не вызывающим резкого снижения АД, относится лизиноприл (Диротон). Эффективность Диротона как средства, препятствующего ремоделированию ЛЖ и развитию СН, а также уменьшающего риск смерти после развития ИМ, показана в условиях эксперимента и клиники. В отличие от большинства иАПФ Диротон не нуждается в биотрансформации в печени для образования активных метаболитов, а также не содержит сульфгидрофильной группы, являющейся причиной ряда побочных эффектов. Отсутствие печеночного метаболизма у Диротона позволяет рекомендовать его больным с патологией печени. Диротон уменьшает риск взаимодействия с другими лекарственными препаратами, которые подвергаются биотрансформации в печени. Исследование эффективности Диротона у пациентов с ИМ и в раннем постинфарктном периоде показало снижение смертности, уменьшение СН. Диротон доказал свою эффективность также у больных пожилого возраста.
Антиаритмические препараты. Обычно речь идет о применении Лидокаина, который ранее назначался всем с профилактической целью купирования желудочковых нарушений ритма. Впоследствии оказалось, что реканализация инфаркт-ассоциированной артерии уменьшает вероятность развития таких аритмий, и доказано, что рутинное применение препарата способствует увеличению смертности. Лидокаин следует назначать только при желудочковой тахикардии или фибрилляции желудочков.
Магния сульфат (магнезия сульфат) может применяется при наличии лабораторно доказанной гипомагнемии или других специфических показаний (например, полиморфная желудочковая тахикардия).
Н. В. Журавлева, кандидат медицинских наук
О. А. Поворинская
РНИИ геронтологии, Москва
Современные подходы к лечению острого инфаркта миокарда
Для цитирования: Староверов И.И. Современные подходы к лечению острого инфаркта миокарда. РМЖ. 1999;15:724.
Российский кардиологический научно-производственный комплекс Минздрава РФ, Москва
Сегодня инфаркт миокарда (ИМ) остается таким же серьезным заболеванием, как и несколько десятилетий назад. Вот только один из примеров, доказывающих тяжесть этой болезни: около 50% больных умирают до того, как успевают встретиться с врачом. Вместе с тем совершенно очевидно, что риск ИМ для жизни и здоровья стал значительно ниже. После того, как 35 лет назад были разработаны основные принципы палат интенсивного наблюдения за коронарными больными и эти палаты начали реально работать в практике здравоохранения, существенно повысилась эффективность лечения и профилактики нарушений ритма и проводимости сердца больных ИМ и снизилась госпитальная летальность. В 70-е годы она составляла более 20%, однако в последние 15 лет, после того как была доказана роль тромбоза в патогенезе острого ИМ и показано благоприятное влияние тромболитической терапии, в целом ряде клиник летальность сократилась в 2 раза и более. Надо сказать, что основные принципы и рекомендации по лечению острого ИМ, впрочем, как и для большинства других серьезных патологий, основываются не только на опыте и знаниях отдельных клиник, направлений, школ, но и на результатах крупных многоцентровых исследований, подчас проводящихся одновременно во многих сотнях больниц в разных странах мира. Конечно, это позволяет врачу в стандартных клинических ситуациях быстрее находить правильное решение.
Основными задачами лечения острого ИМ можно назвать следующие: купирование болевого приступа, ограничение размеров первичного очага поражения миокарда и, наконец, профилактика и лечение осложнений. Типичный ангинозный приступ, развивающийся у подавляющего числа больных при ИМ, связан с ишемией миокарда и продолжается до тех пор, пока не происходит некроз тех кардимиоцитов, которые должны погибнуть. Одним из доказательств именно этого происхождения боли служит быстрое ее исчезновение, при восстановлении коронарного кровотока (например, на фоне тромболитической терапии).
Купирование болевого приступа
Сама по себе боль, воздействуя на симпатическую нервную систему, может существенно увеличивать частоту сердечных сокращений, артериальное давление (АД), а также работу сердца. Именно эти факторы обусловливают необходимость как можно быстрее купировать болевой приступ. Целесообразно дать больному нитроглицерин под язык. Это может ослабить боль в том случае, если больной не получал ранее нитроглицерин в связи с этим приступом. Нитроглицерин может быть в форме таблеток или аэрозоля. Не нужно прибегать к его применению при систолическом АД ниже 90 мм рт.ст.
Во всем мире для купирования болевого приступа используются морфин который вводят внутривенно дробно от 2 до 5 мг каждые 5–30 мин по необходимости до полного (по возможности) купирования боли. Максимальная доза составляет 2–3 мг на 1 кг массы тела больного. Внутримышечного введения морфина следует избегать, так как результат в этом случае непредсказуем. Побочные действия крайне редки (в основном, это гипотония, брадикардия) и довольно легко купируются путем придания ногам возвышенного положения, введения атропина, иногда плазмозамещающей жидкости. У пожилых людей нечасто встречается угнетение дыхательного центра, поэтому у них морфин следует вводить в уменьшенной (даже половинной) дозе и с осторожностью. Антагонистом морфина является налоксон, который также вводят внутривенно, он снимает все побочные явления, в том числе угнетение дыхания, вызванное опиатами. Не исключается применение и других наркотических анальгетиков, например промедола и иных препаратов этого ряда. Предположение о том, что нейролептанальгезия (сочетание фентанила и дроперидола) обладает рядом преимуществ, не получило клинического подтверждения. Попытки замены морфина комбинацией ненаркотических анальгетиков и нейролептиков в этой ситуации неоправданны.
Тромболетическая терапия
Основным патогенетическим методом лечения ИМ является восстановление проходимости окклюзированной коронарной артерии. Чаще всего для достижения этого используют либо тромболитическую терапию, либо механическое разрушение тромба при транслюминальной коронарной ангиопластике. Для большинства клиник нашей страны наиболее реалистично сегодня применение первого способа.
Процесс некроза развивается у человека крайне быстро и в основном заканчивается, как правило, уже через 6–12 ч от начала ангинозного приступа, поэтому чем быстрее и полноценнее удается восстановить кровоток по тромбированной артерии, тем более сохранной будет функциональная способность миокарда левого желудочка и в конечном итоге меньше летальность. Оптимальным считается начало введения тромболитических препаратов через 2–4 ч от начала болезни. Успех лечения будет большим, если удастся сократить промежуток времени до начала тромболитической терапии, что может быть осуществлено двумя путями: первый – раннее выявление и госпитализация больных в стационар и быстрое принятие решения о соответствующем лечении, второй – начало терапии на догоспитальном этапе. В наших исследованиях показано, что начало тромболитической терапии на догоспитальном этапе позволяет добиться выигрыша во времени, в среднем около 2,5 ч. Такой способ тромболитической терапии, если он проводится врачами специализированной бригады кардиологической помощи, является относительно безопасным. При отсутствии противопоказаний тромболитическую терапию целесообразно проводить всем больным в первые 12 ч болезни. Эффективность тромболитической терапии выше (снижение летальности на 42–47%), если она начата в течение 1-го часа болезни. При сроках более 12 ч применение тромболитических препаратов проблематично и должно решаться с учетом реальной клинической ситуации. Особенно показана тромболитическая терапия пожилым людям, пациентам с передним ИМ, а также в тех случаях, когда ее начинают достаточно рано. Обязательное условие для начала тромболитической терапии – наличие элеваций сегмента ST на ЭКГ или признаков блокады ножек пучка Гиса. Тромболитическая терапия не показана, если элевации сегмента ST отсутствуют, независимо от того, как выглядит конечная фаза QRS на ЭКГ – депрессии, отрицательные Т или отсутствие каких-либо изменений. Раннее начало терапии тромболитиками позволяет спасти до 30 больных из 1000 леченых.
Сегодня основным путем введения тромболитических препаратов является внутривенный. Все используемые препараты, тромболитики первого поколения, такие как стрептокиназа (1 500 000 ЕД в течение 1 ч) – урокиназа (3 000 000 ЕД в течение 1 ч), второго поколения – тканевой активатор плазминогена (100 мг болюсом плюс инфузия), проурокиназа (80 мг болюсос плюс инфузия 1 ч) – являются высокоэффективными тромболитиками.
Риск терапии тромболитиками общеизвестен – это возникновение кровотечений, из наиболее опасных – кровоизлияние в мозг. Частота геморрагических осложнений невелика, например количество инсультов при применении стрептокиназы не превышает 0,5%, а при использовании тканевого активатора плазминогена – 0,7–0,8%. Как правило, в случае серьезных геморрагий вводят свежезамороженную плазму и, конечно, прекращают введение тромболитика. Стрептокиназа может вызывать аллергические реакции, которые, как правило, удается предотвратить профилактическим введением кортикостероидов – преднизолона или гидрокортизона. Другое осложнение – гипотония, которая чаще наблюдается при использовании препаратов, созданных на основе стрептокиназы, нередко она сопровождается брадикардией. Обычно это осложнение удается купировать после прекращения инфузии тромболитика и введения атропина и адреналина, иногда требуется применение плазмозаменителей и инотропных средств. Сегодня абсолютными противопоказаниями к тромболитической терапии считаются подозрение на расслоение аорты, активное кровотечение и предшествующий геморрагический инсульт.
В среднем тромболитические препараты получает всего лишь одна треть больных ИМ, а в нашей стране эта цифра существенно ниже. Тромболитики не вводят в основном в связи с поздним поступлением больных, наличием противопоказаний или неопределенностью изменений на ЭКГ. Летальность среди больных, не получающих тромболитики, остается по-прежнему высокой и составляет от 15 до 30%.
b–адреноблокаторы
В 1-е сутки после ИМ повышается симпатическая активность, поэтому использование b-адреноблокаторов, которые снижают потребление кислорода миокардом, уменьшают работу сердца и напряжение стенки желудочка, стало обоснованием их применения у этой категории больных. Ряд крупных многоцентровых исследований, в которых изучалась эффективность внутривенного введения b-блокаторов в 1-е сутки ИМ, показал, что они снижают летальность за 1-ю неделю примерно на 13–15%. Эффект несколько выше, если лечение начинается в первые часы болезни, и отсутствует, если использовать эти препараты со 2–3-го дня заболевания. b-блокаторы уменьшают и количество повторных инфарктов в среднем на 15–18%. Механизм влияния b-блокаторов на летальность – это уменьшение случаев фибрилляции желудочков и разрывов сердца.
Лечение b-блокаторами начинают с внутривенного введения (метопролол, атенолол, пропранолол) – 2–3 раза или столько, сколько потребуется, чтобы оптимально снизить частоту сердечных сокращений. В последующем переходят на прием препаратов внутрь: метопролол 50 мг каждые 6 ч в первые 2 сут, атенолол по 50 мг каждые 12 ч в течение суток, а затем подбирают дозу индивидуально для каждого больного. Основные показания к применению b-блокаторов – признаки симпатической гиперактивности, такие как тахикардия при отсутствии признаков сердечной недостаточности, гипертония, болевой синдром, наличие ишемии миокарда. b-Блокаторы, несмотря на наличие противопоказаний к их применению, например брадикардии (число сердечных сокращений меньше 50 в 1 мин), гипотонии (систолическое АД ниже 100 мм рт.ст.), наличие блокад сердца и отека легких, а также бронхоспазма, применяются тем не менее у подавляющего числа больных ИМ. Однако способность препаратов уменьшать летальность не распространяется на группу b-блокаторов с собственной симпатомиметической активностью. Если больной начал лечиться b-блокаторами, прием препарата следует продолжать до тех пор, пока не появятся серьезные противопоказания.
Применение антиагрегантов и антикоагулянтов
Применение при остром ИМ дезагрегантов, в частности ацетилсалициловой кислоты, способствует уменьшению тромбоза, причем максимальный эффект препарата достигается достаточно быстро после приема первоначальной дозы 300 мг и стабильно поддерживается при ежедневном приеме ацетилсалициловой кислоты в небольших дозах – от 100 до 250 мг/сут. При исследованиях, проведенных у многих тысяч больных оказалось, что применение ацетилсалициловой кислоты снижает 35-дневную летальность на 23%. Противопоказана ацетилсалициловая кислота при обострении язвенной болезни, при его непереносимости, а также при бронхиальной астме, провоцируемой этим препаратом. Длительное применение препарата существенно снижает частоту повторныех инфарктов – до 25%, поэтому прием ацетилсалициловой кислоты рекомендуется на неопределенно долгое время.
Еще одна группа препаратов, воздействующих на тромбоциты, это блокаторы гликопротеина IIВ/IIIА тромбоцитов. В настоящее время известна и доказана эффективность применения двух представителей данного класса – это абсиксимаб и тирофебан. По механизму действия эти препараты выгодно отличаются от ацетилсалициловой кислоты, так как блокируют большинство известных путей активации тромбоцитов. Препараты препятствуют образованию первичного тромбоцитарного тромба, причем действие их иногда бывает достаточно продолжительным – до полугода. Мировой опыт пока еще невелик, в нашей стране работа с этими препаратами только начинается. Из антитромботических препаратов по-прежнему широко используется антикоагулянт гепарин, который в основном назначают для профилактики повторных инфарктов, для предупреждения тромбозов и тромбоэмболий. Схемы и дозы введения его хорошо известны. Дозу подбирают так, чтобы частичное тромбопластиновое время увеличилось в 2 раза по сравнению с нормой. Средняя доза – это 1000 ЕД/ч в течение 2–3 дней, подкожное введение гепарина рекомендуется при медленной активизации пациентов.
В настоящее время имеются данные об использовании низкомолекулярных гепаринов, в частности эноксипарина и фрагмина. Основные их преимущества состоят в том, что они фактически не требуют лабораторного контроля за показателями свертываемости крови и специальной аппаратуры, например инфузионных насосов, для их введения, а главное – они существенно эффективнее чем нефракционированные гепарины. Не потеряло своей значимости применение непрямых антикоагулянтов, особенно при венозных тромбозах, выраженной сердечной недостаточности, наличии тромба в левом желудочке.
Антагонисты кальция
В качестве стандартной терапии ИМ антагонисты кальция в настоящее время фактически не используются, так как не оказывают благоприятного влияния на прогноз, а применение их с научной точки зрения малообоснованно.
Внутривенное введение нитратов при ИМ в первые 12 ч заболевания уменьшает размер очага некроза, влияет на основные осложнения ИМ, включая летальные исходы и частоту развития кардиогенного шока. Применение их снижает летальность до 30% в первые 7 дней болезни, это наиболее очевидно при инфарктах передней локализации. Прием нитратов внутрь начиная с 1-х суток заболевания не приводит ни к улучшению, ни к ухудшению прогноза к 30-му дню болезни. Внутривенное введение нитратов должно быть стандартной терапией для всех пациентов, поступивших в первые часы болезни, с передним ИМ и систолическим АД выше 100 мм рт.ст. Начинают введение нитроглицерина с невысокой скоростью, например 5 мкг/мин, постепенно увеличивают ее, достигая уменьшения систолического давления на 15 мм рт.ст. У больных с артериальной гипертонией снижение АД возможно до 130–140 мм рт.ст. Как правило, терапию нитратами проводят в течение 24 ч, если не появляется необходимости продолжения этой терапии, в частности при сохраняющихся болях, связанных с ишемией миокарда, или признаках сердечной недостаточности.
Ингибиторы АПФ
В последнее десятилетие в лечении больных ИМ прочно заняла свое место большая группа ингибиторов ангиотензинпревращающего фермента (иАПФ). Это в первую очередь определяется тем, что данные препараты способны приостанавливать расширение, дилатацию левого желудочка, истончение миокарда, т.е. воздействовать на процессы, приводящие к ремоделированию миокарда левого желудочка и сопровождающиеся серьезным ухудшением сократительной функции миокарда и прогноза. Как правило, лечение иАПФ начинают через 24–48 ч от момента развития ИМ, чтобы снизить вероятность артериальной гипертонии. В зависимости от исходно нарушенной функции левого желудочка терапия может продолжаться от нескольких месяцев до многих лет. Установлено, что лечение каптоприлом в дозе 150 мг/сут у пациентов без клинических признаков недостаточности кровообращения, но при наличии фракции выброса ниже 40% существенно улучшало прогноз. В группе леченых смертность была ниже на 19%, на 22% было меньше случаев сердечной недостаточности, требовавшей лечения в условиях стационара. Таким образом, АПФ (каптоприл 150 мг/сут, рамиприл 10 мг/сут, лизиноприл 10 мг/сут и др.) целесообразно назначать большинству больных ИМ, независимо от его локализации и наличия или отсутствия сердечной недостаточности. Однако эта терапия более эффективна при сочетании клинических признаков сердечной недостаточности и данных инструментальных исследований (низкая фракция выброса). В этом случае риск летального исхода снижается на 27%, т.е. это предотвращает смертельные исходы у каждых 40 из 1000 леченых больных в течение года.
Уже во время пребывания больного в стационаре целесообразно детально исследовать его липидный спектр. Сам по себе острый ИМ несколько уменьшает содержание свободного холестерина в крови. При наличии данных о существенных изменениях этого показателя, например при уровне общего холестерина выше 5,5 ммоль/л, целесообразно рекомендовать больному не только гиполипидемическую диету, но и прием препаратов, в первую очередь статинов.
Таким образом, в настоящее время врач располагает значительным арсеналом средств, позволяющих помочь больному ИМ и свести к минимуму риск возникновения осложнений. Конечно, основной путь достижения этой цели – применение тромболитических препаратов, но вместе с тем использование b-блокаторов, аспирина, АПФ и нитратов может существенным образом повлиять на прогноз и исход заболевания.
Эналаприл:
| Приложения к статье |
| Основные задачи лечения острого инфаркта миокарда: 1) купирование болевого приступа 2) ограничение размеров первичного очага поражения миокарда 3)профилактика и лечение осложнений |
| При отсутствии противопоказаний тромболитическую терапию целесообразно проводить всем больным в первые 12 ч болезни |
| Внутривенное введение нитратов должно быть терапией для всех пациентов с передним инфарктом миокарда и систолическим АД выше 100 мм рт.ст. |
| СХЕМА ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА |
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Инфаркт миокарда
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Инфаркт миокарда: причины появления, симптомы, диагностика и способы лечения.
Определение
Инфаркт миокарда (ИМ) – это омертвление участка сердечной мышцы вследствие недостаточного ее кровоснабжения с развитием характерной клинической картины.
Причины появления инфаркта миокарда
Сердце – полый мышечный орган, имеющий форму конуса. Стенки сердца состоят из трех слоев. Внутренний слой – эндокард – выстилает полости сердца изнутри, и его выросты образуют клапаны сердца. Средний слой – миокард – состоит из сердечной мышечной ткани. Наружный слой – перикард. Сердце человека имеет четыре камеры: два предсердия и два желудочка. В правое предсердие поступает кровь из тканей самого сердца и всех частей тела (по верхней и нижней полым венам). В левое предсердие впадают четыре легочные вены, несущие артериальную кровь из легких. Из правого желудочка выходит легочный ствол, по которому венозная кровь поступает в легкие. Из левого желудочка выходит аорта, несущая артериальную кровь в сосуды большого круга кровообращения. Кислород к миокарду сердца доставляется по коронарным артериям.
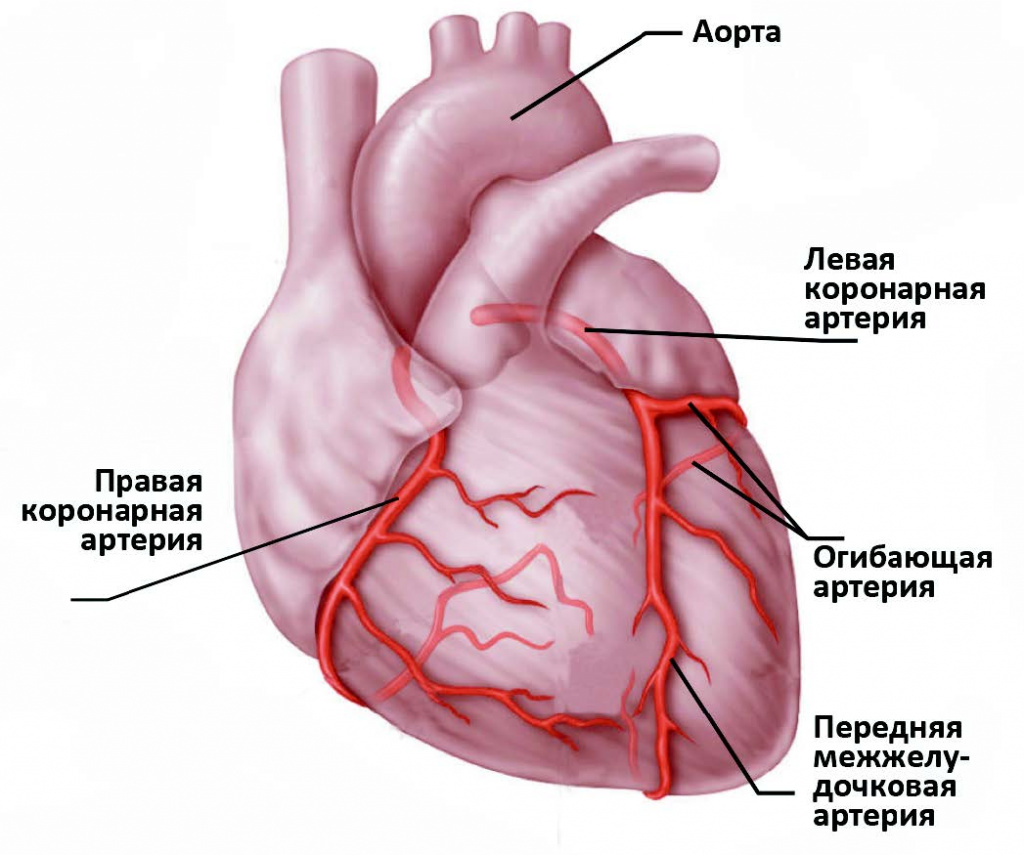
Сердце очень чувствительно к недостатку кровоснабжения (дефициту кислорода). В случае закупорки крупной коронарной артерии и при отсутствии эффективного альтернативного кровообращения по другим сосудам уже через 30 минут в пораженном участке начинается гибель кардиомиоцитов (мышечных клеток сердца).
Нарушение кровообращения вследствие атеросклеротического поражения коронарных артерий в 97-98% случаев имеет основное значение в возникновении инфаркта миокарда.
Атеросклерозом может поражаться как одна коронарная артерия, так и все три. Степень и протяженность сужения артерии могут быть различными. При повышении артериального давления склерозированный внутренний слой сосуда (эндотелий) легко повреждается, кровь проникает внутрь бляшки, активируется процесс свертывания крови и формируется тромб, который может частично или полностью закупорить сосуд.
Где может формироваться тромб:
- на месте разрыва уязвимой (нестабильной) атеросклеротической бляшки;
- на дефекте (эрозии) эндотелия коронарной артерии, не обязательно локализованном на поверхности атеросклеротической бляшки;
- в месте гемодинамически незначимого сужения коронарной артерии.
Развивающийся некроз миокарда может быть различных размеров, а некроз, проходящий через все слои сердца (трансмуральный) может стать причиной разрыва миокарда.
Образование очагов некроза в миокарде сопровождается изменением размера, формы и толщины стенки сердца, а сохранившийся миокард испытывает повышенную нагрузку и подвергается гипертрофии с увеличением объема и массы.
Такие сопутствующие состояния как: анемия, воспаление, инфекция, лихорадка, метаболические или эндокринные расстройства (в частности, гипертиреоз) могут спровоцировать или утяжелить ишемию миокарда.
К факторам риска развития инфаркта миокарда относятся:
- гиперлипидемия (нарушение нормального соотношения липидов крови);
- курение,
- сахарный диабет,
- артериальная гипертензия,
- абдоминальное ожирение,
- психосоциальные причины (стресс, депрессия и т.д.),
- низкая физическая активность,
- несбалансированное питание и потребление алкоголя.
Классификация инфаркта миокарда
I. Острый инфаркт миокарда.
- Острый трансмуральный инфаркт передней стенки миокарда.
- Острый трансмуральный инфаркт нижней стенки миокарда.
- Острый трансмуральный инфаркт миокарда других уточненных локализаций.
- Острый трансмуральный инфаркт миокарда неуточненной локализации.
- Острый инфаркт миокарда неуточненный.
- Повторный инфаркт передней стенки миокарда.
- Повторный инфаркт нижней стенки миокарда.
- Повторный инфаркт миокарда другой уточненной локализации.
- Повторный инфаркт миокарда неуточненной локализации.
- Гемоперикард.
- Дефект межпредсердной перегородки.
- Дефект межжелудочковой перегородки.
- Разрыв сердечной стенки без гемоперикарда.
- Разрыв сухожильной хорды.
- Разрыв сосочковой мышцы.
- Тромбоз предсердия, ушка предсердия и желудочка сердца.
- Другие текущие осложнения острого инфаркта миокарда.
- Коронарный тромбоз, не приводящий к инфаркту миокарда.
- Синдром Дресслера – постинфарктный склероз.
- Другие формы острой ишемической болезни сердца.
- Острая ишемическая болезнь сердца неуточненная.
Симптомы инфаркта миокарда
При инфаркте миокарда в результате нарушения кровообращения в пораженном участке сердца накапливаются продукты обмена, которые раздражают рецепторы миокарда и коронарных сосудов, что проявляется острой болью. Болевой приступ приводит к выбросу адреналина и норадреналина корой надпочечников.
Боль при типичном течении инфаркта миокарда является основным его признаком. Она возникает за грудиной, иногда может отдавать в левую руку, левое плечо, горло, нижнюю челюсть, в подложечную область.
По интенсивности и длительности такая боль в значительной степени превосходит обычный приступ стенокардии. Боль не снимается приемом нитроглицерина. Длительность болевого синдрома может быть различной – от 1 часа до нескольких суток. Иногда инфаркт миокарда сопровождается резкой слабостью, головокружением, головной болью, рвотой, потерей сознания. Больной выглядит бледным, губы синеют, наблюдается потливость.
В первые сутки развития инфаркта миокарда может регистрироваться тахикардия (учащенное сердцебиение), нарушение ритма, повышение температуры до 37-38℃.
Выделяют следующие клинические варианты:
- астматический – протекает как приступ бронхиальной астмы (присутствуют одышка, затрудненное дыхание, чувство нехватки воздуха);
- гастралгический – характеризуется болями в области желудка с распространением в загрудинное пространство, может быть отрыжка, икота, тошнота, многократная рвота, вздутие живота;
- аритмический – возникают нарушения ритма сердца, угрожающие жизни;
- церебральная – характеризуется нарушением мозгового кровообращения (наблюдаются тошнота, головокружение, нарушение сознания с развитием обморока);
- бессимптомный – инфаркт миокарда без типичного болевого приступа. В связи с несоблюдением постельного режима и отсутствием должного лечения протекает неблагоприятно.
Существуют четкие критерии диагностики инфаркта миокарда:
- клиническая картина инфаркта миокарда;
- картина инфаркта миокарда по данным ЭКГ;
- наличие новых участков миокарда со сниженным кровообращением или нарушение сократимости миокарда по данным инструментальных исследований;
- выявление тромбоза коронарных артерий по данным ангиографии.
-
определение уровня биохимических маркеров повреждения кардиомиоцитов в крови;
Высокочувствительное исследование тропонина-I применяется в современных алгоритмах диагностики острого инфаркта миокарда, а также повреждений миокарда в широком спектре иных клинических обстоятельств, таких как мониторинг состояния пациентов в критических состояниях, оценки периоперационного риска, прогноз кардиорисков у пациентов с сердечно-сосудистыми заболеваниями, контроль химиотерапии. Тест-системы вч TnI ARCHITECT (Abbott) одобрены также для оценки кардиорисков у условно-здоровых лиц при профилактическим скрининге
Инфаркт миокарда и нестабильная стенокардия

Инфаркт миокарда – неотложное заболевание сердца, которое чаще всего вызывается внезапной закупоркой коронарной артерии тромбом. Подозрение на инфаркт миокарда кардиологи называют – острым коронарным синдромом (ОКС). По данным электрокардиографии (ЭКГ) выделяют ОКС с повреждением сердечной мышцы, либо начальная фаза без гибели сердечной мышцы, которая называется нестабильной стенокардией. Восстановление кровообращения в коронарной артерии при инфаркте миокарда в течение ближайших 6 часов устраняет последствия и такой подход очень эффективен, потому что даёт надежду на полное выздоровление. Первые признаки инфаркта миокарда должны стать поводом для экстренной госпитализации в специализированный центр.
Подход к лечению в Инновационном сосудистом центре
Современная технология лечения ОКС и нестабильной стенокардии подразумевает коронарографию, ангиопластику и стентирование поражённой артерии. Эта тактика с успехом применяется у нас в клинике. В нашей клинике есть чёткое понимание того, что спасение жизни при инфаркте зависит от времени, когда было восстановлено коронарное кровоснабжение. Поэтому принимая машины скорой помощи, мы организуем экспресс-диагностику и подготовку больного к коронарографии в течение 5 минут. Среднее время восстановления коронарного кровотока после поступления больного в клинику составляет менее 20 минут. Отличительные особенности, подготовка наших специалистов и организация работы клиники позволяет сохранять очень низкий уровень летальности при инфаркте миокарда.
Причины инфаркта миокарда
Сердце требует своего постоянного снабжения кислородом и питательными веществами, как и любая мышца в организме. Для обеспечения этой потребности необходима хорошая проходимость двух крупных артерий и их ветвей, которые доставляют обогащённую кислородом кровь к сердечной мышце. Это система правой и левой коронарных артерий. Если одна из этих артерий или ветвей внезапно блокируются, то часть сердца испытывает недостаток кислорода. Это состояние называется “ишемией миокарда”. Если ишемия продолжается долго, то может возникнуть гибель мышечной ткани сердца. Это сердечный приступ, известный как инфаркт миокарда – буквально “смерть сердечной мышцы”.
Атеросклероз коронарных артерий (ишемическая болезнь сердца) является фоновым состоянием для большинства инфарктов миокарда . Непосредственной причиной возникновения инфаркта миокарда обычно бывает тромб, образующийся в суженом участке сосуда и полностью перекрывающий кровоток.
Инфаркт миокарда – классификация причин :
Тип 1 – спонтанный, вследствие первичного коронарного события, такого как разрыв, растрескивание или расслоение атеросклеротической бляшки
Тип 2 – инфаркт развивается вследствие уменьшения кровообращения сердца вследствие вторичных причин, таких как спазм коронарной артерии, коронарной эмболия, анемия, аритмия, гипертензия или гипотензия.
Тип 3 – внезапная неожиданная сердечная смерть, включая остановку сердца, часто с симптомами ишемии миокарда. Только патологоанатом может ответить на вопрос, как и отчего происходит развитие массивного инфаркта миокарда при внезапной смерти.
Тип 4 – связанный с коронарной ангиопластикой или стентированием:
Тип 4а – развитие инфаркта миокарда вследствие чрескожного коронарного вмешательства.
Тип 4б – инфаркт, связанный с тромбозом стента.
Тип 5 – развитие инфаркта миокарда, связанного с аортокоронарным шунтированием.
Клинические синдромы при инфаркте
- Сердечная недостаточность, когда сердце не справляется с перекачиванием необходимого объёма крови из гибели части мышечных клеток.
- Аритмии или другие нарушения сердечного ритма из-за гибели проводящих путей.
- Внезапная сердечная смерть, когда сердце перестаёт биться из-за блокады проводящих путей.
- Кардиогенный шок – рефлекторная реакция организма с низким артериальным давлением, которая может привести к повреждению почек, печени и головного мозга.
Атипичные формы инфаркта
Помимо характерной для инфаркта сдавливающей боли за грудиной, выделяют ещё несколько форм инфаркта, которые могут напоминать другие заболевания или протекать бессимптомно. К ним относятся:
- Гастритический инфаркт. Начинается болью в верхней половине живота похожей на обострение гастрита. Нередко при ощупывании живота, отмечается болезненность и напряжённость мышц передней брюшной стенки. Иногда симптоматика напоминает прободную язву.
- Астматический инфаркт. Симптоматика напоминает приступ бронхиальной астмы. Она проявляется надсадным сухим кашлем, чувством заложенности в груди, одышкой. Бывает при поражении передней стенки левого желудочка.
- Безболевой вариант инфаркта, который может проявиться ощущением неопределённого дискомфорта в грудной клетке, потоотделением и общей слабостью.
Классификация инфаркта
По ЭКГ обычно выделяют на два варианта: с подъёмом сегмента ST (ЅТEMI) и без подъёма сегмента ST (NSTEMI). Подъём сегмента ST на электрокардиограмме и последующим изменением специфических лабораторных показателей свидетельствует о формировании очага гибели сердечной мышцы. Термин “Острый коронарный синдром” часто используется для определения тактики первичной врачебной помощи и включает в себя все варианты острого нарушения коронарного кровообращения.
Осложнения
Осложнения инфаркта связаны с повреждением участков сердца, проводящих путей, тромбозами полостей сердца. Развитие инфаркта значит гибель того или иного структурного элемента сердца.
Примерно у 90% больных отмечаются различные формы нарушений сердечного ритма (аритмии) во время или сразу после события. У 25% пациентов, нарушение ритма проявляются в течение первых 24 часов. В этой группе больных риск серьёзных аритмий, таких как фибрилляция желудочков, является наибольшим в течение первого часа, а затем постепенно сокращается. Врач должен правильно оценивать эти аритмии, так как некоторые из них могут привести к остановке сердца, поэтому необходим постоянный мониторинг ЭКГ у больных с ишемией миокарда.
- Повреждения миокарда и структуры сердца.
Гибель ткани сердца вследствие прекращения кровоснабжения может привести к распаду этой ткани и повреждению структуры сердца. Чаще всего наблюдаются 3 основных механических осложнений инфаркта:
- Спонтанный разрыв стенки желудочка.
- Разрыв межжелудочковой перегородки значит, что развивается нарушение внутрисердечных потоков крови и гемодинамики.
- Отрыв сосочковой мышцы разрыв с развитием впоследствии тяжёлой недостаточности митрального клапана.
- Постинфарктные аневризмы левого желудочка.
Аневризма левого желудочка это локализованный участок миокарда с аномальными выпячиванием и деформацией во время систолы и диастолы, который появляется вследствие замещения миокарда рубцовой тканью. Аневризма опасна скоплением тромботических масс в её просвете с последующей эмболией (переносом) их с током крови в другие органы. При аневризме увеличивается объём левого желудочка, а значит проявляется его относительная функциональная недостаточность.
- Тромботические осложнения
При инфаркте в левом желудочке нередко возникает пристеночный тромб, особенно часто он развивается после инфарктов, произошедших в области передней стенки левого желудочка. Частота этого осложнения при инфаркте составляет 20-60 %, что приводит к высокому риску отрыва и переноса тромба с током крови (эмболии). Антикоагулянтная терапия может существенно уменьшить риск развития тромбоза и эмболии.
Клинические синдромы, связанные с повреждением миокарда после инфаркта
- Перикардит
Воспаление околосердечной сумки (перикарда) наблюдается примерно у 10% пациентов после перенесённого инфаркта со значительным повреждением миокарда. Перикардит обычно лечится противовоспалительными препаратами или при большом скоплении жидкости может проводится пункция перикарда для облегчения состояния пациента.
- Постинфарктный аутоиммунный синдром (синдром Дресслера)
До эпохи тромболизиса и коронарной ангиопластики этот синдром возникал у 5 % больных после сердечного приступа. С внедрением реперфузии развитие синдрома Дресслера происходит реже. Отличительные клинические признаки включают лихорадку, боль в груди и симптомы перикардита возникают через 2-3 недели после лечения инфаркта миокарда . Лечение включает в себя противовоспалительные препараты и гормоны. Клинические проявления синдрома обуславливают значимую сердечную недостаточность, развивающуюся после инфаркта.
Прогноз
Острый инфаркт миокарда приводит в результате к 30% смертности, а половина смертей происходят до прибытия в больницу. В течение первого года после острого сердечного приступа умирают 5-10% выживших. Приблизительно половина всех пациентов подвергаются повторной госпитализации в течение 1 года после предыдущего события. Большое значение для прогноза имеет объём поражённой ткани миокарда. Он сильно варьирует и во многом зависит от степени инфаркта, остаточной функции левого желудочка, и будет ли проведено восстановление кровообращения в миокарде.
Лучший прогноз связан со следующими факторами:
- Успешная ранняя реперфузия (с подъёмом сегмента ST с помощью тромболизиса или чрескожное коронарное вмешательство (ангиопластика и стентирование) в течение 90 минут.
- Сохранилась функция левого желудочка в результате быстрого восстановления кровоснабжения миокарда.
- Адекватная терапия с бета-адреноблокаторами, аспирином, клопидогрелем и ингибиторами АПФ в остром периоде.
Неблагоприятный прогноз связан со следующими факторами:
- Преклонный возраст
- Сахарный диабет
- Поражения в других бассейнах (сонные и периферические артерии)
- Задержка или неудачное коронарное вмешательство.
- Плохо сохранилась функция левого желудочка
Преимущества лечения в клинике
Диагностика
 Симптомы инфаркта миокарда
Симптомы инфаркта миокарда
Стенокардия (пациент испытывает сжимающие боли за грудиной): самый первый признак поражения коронарных артерий и симптом грядущего инфаркта миокарда. Большинство пациентов отмечают предшествующие приступы стенокардии, которая даёт аналогичную боль в груди. Разница в основном в продолжительности болевого синдрома: при стенокардии кровообращение восстанавливается, боль отступает в течение нескольких минут, а миокард не повреждается.
При инфаркте поток крови критически снижен или полностью заблокирован, боль длится дольше и сердечная мышца может погибнуть в ближайшие часы. Затянувшийся приступ стенокардии должен заставить срочно вызвать скорую помощь! Около 25% всех инфарктов происходит без предшествующей стенокардии, но могут сопровождаться снижением давления и появлением одышки.
Для выявления проблем с кровообращением миокарда необходимо выполнить электрокардиографию (ЭКГ). Так как инфаркт – это гибель участков ткани сердца и его проводящих путей, то развиваются нарушения его функции.
Основные симптомы инфаркта миокарда связаны с болью и острой сердечной недостаточностью :
- Боль в груди, чувство наполнения и/или сдавливания в груди.
- Боль в челюсти, зубная, головная боль.
- Нехватка дыхания, которую больной чувствует из-за отёка лёгких.
- Тошнота, рвота, общее ощущение давления под ложечкой (вверху в центре живота).
- Потливость, одышка .
- Изжога и/или расстройство пищеварения, кишечника.
- Боль в руке (наиболее часто в левой, но может и в правой руке).
- Боль в верхней части спины, которую пациент испытывает при заднем инфаркте.
- Общее болезненное ощущение (неясное ощущение недомогания) и нарушения сердцебиения.
Диагностика инфаркта складывается из методов определения характера инфаркта и формы повреждения миокарда и определения причин этого повреждения. Для диагностики используются следующие методы:
- Электрокардиограмма (ЭКГ).
Электрическая активность сердца регистрируется с помощью электродов, прикреплённых к коже. Определённые отклонения в электрической активности сердца могут помочь специалистам определить зоны ишемии миокарда и уточнить диагноз.
Это ультразвуковое исследование сердца. Она позволяет выявить зоны нефункционирующего миокарда при его гибели и в результате определить функциональный резерв сердца — фракцию выброса.
Контрастное вещество вводится в кровеносные сосуды сердца. Затем рентгеновский аппарат делает серию снимков (ангиография), показывая проходимость этих коронарных артерий. Это исследование позволяет определить причину ишемии миокарда и принять меры для нормализации кровотока по коронарным артериям.
- Лабораторная диагностика.
Наиболее чувствительным и специфичным маркёром гибели клеток миокарда является повышение концентрации тропонинов I и Т. В норме эти тропонины в крови не определяются. Возникновение некроза кардиомиоцитов сопровождается сравнительно быстрым и значительным увеличением концентрации тропонинов I и Т уже через 2–6 ч после сердечного приступа.
Лечение

Лечение ишемии миокарда предполагает улучшение притока крови к сердечной мышце. Консервативная терапия инфаркта миокарда малоэффективна, чтобы открыть заблокированные коронарные артерии может быть использован внутривенный тромболизис.
Своевременное эндоваскулярное вмешательство – коронарная ангиопластика и стентирование восстанавливают проходимость коронарных сосудов и предотвращают развитие инфаркта, снижая летальность при ОКС до 2% с 40% при обычном лечении. Улучшение непосредственных и отдалённых исходов является отличительной чертой эндоваскулярных вмешательств по сравнению с консервативной терапией.
Большинство инфарктов развивается в течение нескольких часов, поэтому не стоит ждать, чтобы появились все признаки и последствия сердечного приступа. Чаще всего сердечный приступ сопровождается болью в грудной клетке, которая не проходит после приёма нитроглицерина, однако бывают и безболевые формы, особенно у больных с сахарным диабетом. Инфаркт требует немедленной медицинской помощи. Для того чтобы максимально сохранить жизнеспособную сердечную мышцу и предотвратить дальнейшее ухудшение пациенту надо дать аспирин и нитроглицерин.
Если через 15 минут после нитроглицерина и получаса после возникновения боль в грудной клетке не отступила, то необходимо срочно вызывать скорую помощь. В зависимости от вида инфаркта проводятся различные лечебные мероприятия.
- Лечение инфаркта миокарда с подъёмом ЅТ (STEMI)
Основное лечение для инфаркта с подъёмом сегмента ST может включать тромболизис или чрескожное коронарное вмешательство (ЧКВ). Первичное чрескожное коронарное вмешательство является методом выбора для лечения инфаркта с подъёмом ЅТ, если оно может быть выполнено своевременно. Если ЧКВ не может быть выполнено в течение 90 до 120 минут, то с целью оказания первой помощи рекомендуется проведение тромболизиса. Если пациент имеет симптомы инфаркта в течение от 12 до 24 часов, то показаний для тромболизиса меньше, позже тромболизис не рекомендуется.
ЧКВ – главный метод лечения острого инфаркта миокарда, позволяющий восстановить кровоток в инфаркт-связанной артерии. Чем раньше будет проведена ангиопластика и стентирование закрытой коронарной артерии, тем больше шансов на благоприятный исход.
- Инфаркт миокарда без подъёма сегмента ST
При отсутствии подъёма сегмента ST, диагноз уточняется с помощью анализа крови на тропонин. Положительный тест на тропонин может появиться через 3-6 часов после развития острого коронарного синдрома и свидетельствует о том, что имеется очаг некроза миокарда. Такой инфаркт называется “острый коронарный синдром без подъёма сегмента ST (NSTEMI). В этом случае у врача есть время, чтобы специалисты провели дополнительные обследования больного, которые определят необходимость вмешательства на коронарных артериях. Если принято решение о необходимости реваскуляризации, то коронарография проводится в ближайшие часы после поступления пациента. Если принято решение о консервативном лечении, то применяются дезагреганты (клопидогрель, тромбо асс) и патогенетическая лекарственная терапия, отказ от вредных привычек, изменение образа жизни и режима физической активности.

 Симптомы инфаркта миокарда
Симптомы инфаркта миокарда
